Ingrediente active: Acid zoledronic
Aclasta 5 mg soluție perfuzabilă
Indicații De ce se utilizează Aclasta? Pentru ce este?
Aclasta conține substanța activă acid zoledronic. Acesta aparține unui grup de medicamente numite bifosfonați și este utilizat pentru a trata femeile și bărbații adulți în postmenopauză cu osteoporoză sau osteoporoză cauzată de tratamentul cu corticosteroizi utilizați pentru a trata inflamația și boala Paget a oaselor la adulți.
Osteoporoza
Osteoporoza este o boală care determină subțierea și slăbirea oaselor și este frecventă la femei după menopauză, dar poate apărea și la bărbați.În momentul menopauzei, ovarele încetează să producă hormonul feminin estrogen, care contribuie la păstrarea stării de sănătate a oasele. După menopauză apare pierderea osoasă, oasele devin mai slabe și se rup mai ușor. Osteoporoza poate apărea și la bărbați și femei, datorită utilizării pe termen lung a steroizilor, care poate afecta rezistența osoasă. Mulți pacienți cu osteoporoză nu prezintă simptome, dar sunt încă expuși riscului de fractură osoasă, deoarece osteoporoza le-a făcut oasele mai fragile. Reducerea nivelurilor de hormoni sexuali circulanți, în principal estrogeni convertiți din androgeni, joacă, de asemenea, un rol în pierderea osoasă mai graduală observată la bărbați. Atât la femei, cât și la bărbați, Aclasta întărește oasele și face riscul de fractură mai puțin probabil. Aclasta este, de asemenea, utilizat la pacienții care au avut recent o fractură de șold din cauza unor traume minore, cum ar fi o cădere și, prin urmare, prezintă un risc de fracturi osoase.
Boala Paget a osului
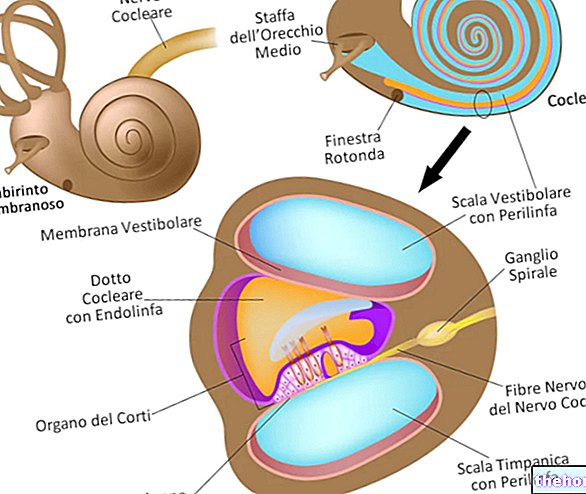
Este normal ca osul îmbătrânit să fie îndepărtat și înlocuit cu os nou. Acest proces se numește remodelare osoasă. În boala Paget, remodelarea osoasă este prea rapidă și se formează oase noi într-un mod dezordonat, ceea ce o face mai slabă decât în mod normal. Dacă boala nu este tratată, oasele se pot deforma și deveni dureroase și se pot rupe. Aclasta acționează pentru a readuce la normal procesul de remodelare osoasă, asigurând formarea osoasă normală, restabilind astfel rezistența osoasă.
Contraindicații Când nu trebuie utilizat Aclasta
Urmați cu atenție toate instrucțiunile pe care vi le-a dat medicul, farmacistul sau asistenta înainte de a vi se administra Aclasta.
Aclasta nu trebuie să vi se administreze:
- dacă sunteți alergic la acidul zoledronic, la alți bifosfonați sau la oricare dintre celelalte componente ale acestui medicament
- dacă aveți hipocalcemie (adică dacă nivelul de calciu din sânge este prea scăzut)
- dacă aveți probleme renale severe
- dacă sunteți gravidă.
- dacă alăptați.
Precauții pentru utilizare Ce trebuie să știți înainte de a lua Aclasta
Discutați cu medicul dumneavoastră înainte de a vi se administra Aclasta:
- dacă sunteți tratat cu orice medicament care conține acid zoledronic, care este, de asemenea, substanța activă din Aclasta (acidul zoledronic este utilizat la pacienții adulți cu anumite tipuri de cancer pentru a preveni complicațiile osoase sau pentru a reduce cantitatea de calciu)
- dacă aveți probleme cu rinichii sau ați avut vreodată vreodată
- dacă nu puteți lua un supliment zilnic de calciu
- dacă ați avut o parte sau toate glandele paratiroide din gât îndepărtate prin intervenție chirurgicală.
- dacă vi s-au eliminat secțiuni din intestin.
Un efect nedorit numit osteonecroză a maxilarului (leziuni osoase ale maxilarului) a fost raportat în experiența de după punerea pe piață la pacienții tratați cu Aclasta (acid zoledronic) pentru tratamentul osteoporozei. Osteonecroza maxilarului. Poate apărea și după oprirea tratamentului.
Este important să încercați să preveniți apariția osteonecrozei maxilarului, deoarece este o afecțiune dureroasă care poate fi dificil de tratat.Pentru a reduce riscul de apariție a osteonecrozei maxilarului, trebuie să luați câteva precauții.
Înainte de a primi tratament cu Aclasta, discutați cu medicul dumneavoastră, farmacistul sau asistenta medicală dacă:
- aveți probleme cu gura sau dinții, cum ar fi sănătatea dentară slabă, boli ale gingiilor sau ați planificat o „extracție a dinților
- nu beneficiați de îngrijire dentară de rutină sau nu ați făcut un control dentar de mult timp
- sunteți fumător (deoarece acest lucru poate crește riscul de probleme dentare)
- ați fost anterior tratați cu un bifosfonat (utilizat pentru tratarea sau prevenirea tulburărilor osoase);
- luați medicamente numite corticosteroizi (cum ar fi prednisolon sau dexametazonă)
- are cancer.
Medicul dumneavoastră vă poate cere să vă supuneți unui examen dentar înainte de a începe tratamentul cu Aclasta.
În timpul tratamentului cu Aclasta, trebuie să mențineți o igienă orală bună (care include periajul regulat al dinților) și să faceți controale dentare de rutină. Dacă purtați proteze dentare, trebuie să vă asigurați că acestea sunt bine fixate. Dacă urmează tratament dentar sau urmează să fie supus unei intervenții chirurgicale dentare (de exemplu, extracții dentare), vă rugăm să spuneți medicului dumneavoastră și să spuneți medicului dentist că sunteți tratat cu Aclasta. Spuneți imediat medicului dumneavoastră și medicului dentist dacă aveți probleme cu gura sau dinții, cum ar fi slăbirea, durerea, umflarea sau răni nevindecătoare sau descărcarea, deoarece acestea pot fi semne de osteonecroză a maxilarului.
Test de monitorizare
Medicul dumneavoastră trebuie să ia o probă de sânge pentru a vă verifica funcția rinichilor (niveluri de creatinină) înainte de fiecare perfuzie de Aclasta. Este important să beți cel puțin două pahare de lichide (de exemplu apă) în câteva ore înainte de tratamentul cu Aclasta, conform instrucțiunilor îngrijitorului.
Copii și adolescenți
Aclasta nu este recomandat sub vârsta de 18 ani. Utilizarea Aclasta la copii și adolescenți nu a fost studiată
Interacțiuni Ce medicamente sau alimente pot modifica efectul Aclasta
Spuneți medicului dumneavoastră, farmacistului sau asistentei medicale dacă luați, ați luat recent, s-ar putea să luați orice alte medicamente.
Este important ca medicul dumneavoastră să cunoască toate medicamentele pe care le luați, mai ales dacă luați deja alte medicamente care pot fi dăunătoare rinichilor (de exemplu aminoglicozide) sau diuretice („medicamente pentru a urina”) care pot provoca deshidratare.
Avertismente Este important să știm că:
Sarcina și alăptarea
Nu trebuie să vi se administreze Aclasta dacă sunteți gravidă sau alăptați, credeți că ați putea fi gravidă sau intenționați să rămâneți gravidă.
Adresați-vă medicului dumneavoastră, farmacistului sau asistentei medicale pentru recomandări înainte de a lua acest medicament.
Conducerea vehiculelor și utilizarea utilajelor
Dacă vă amețiți în timp ce luați Aclasta, nu conduceți vehicule și nu folosiți utilaje până nu vă simțiți mai bine.
Aclasta conține sodiu
Acest medicament conține mai puțin de 1 mmol sodiu (23 mg) per flacon de 100 ml Aclasta, deci, în esență, „fără sodiu”.
Doză, metodă și timp de administrare Cum se utilizează Aclasta: Doze
Urmați cu atenție toate instrucțiunile pe care vi le-a dat medicul sau asistenta dvs. Dacă aveți dubii, consultați medicul sau asistenta.
Osteoporoza
Doza uzuală este de 5 mg, administrată de medicul sau asistenta dumneavoastră ca perfuzie unică în venă pe an. Perfuzia va dura cel puțin 15 minute.
În cazul unei fracturi recente de șold, se recomandă administrarea Aclasta la două sau mai multe săptămâni după intervenția chirurgicală pentru fractură de șold.
Este important să luați suplimente de calciu și vitamina D (de exemplu, tablete) conform instrucțiunilor medicului dumneavoastră.
Pentru osteoporoză, Aclasta funcționează timp de un an. Medicul dumneavoastră vă va anunța când vă veți întoarce pentru următoarea doză.
Boala Paget
Pentru tratamentul bolii Paget, Aclasta trebuie prescris numai de către medici cu experiență în tratamentul bolii Paget a osului.
Doza uzuală este de 5 mg, administrată de medicul sau asistenta medicală într-o perfuzie inițială în venă. Infuzia va dura cel puțin 15 minute. Aclasta poate funcționa mai mult de un an și medicul dumneavoastră vă va informa dacă aveți nevoie de un alt tratament.
Medicul dumneavoastră vă poate sfătui să luați suplimente de calciu și vitamina D (de exemplu, comprimate) timp de cel puțin primele zece zile după administrarea Aclasta. Este important să urmați cu atenție acest sfat, astfel încât nivelul de calciu din sânge să nu fie prea scăzut în perioada următoare perfuziei. Medicul dumneavoastră vă va informa despre posibilele simptome asociate cu hipocalcemia.
Aclasta cu alimente și băuturi
Asigurați-vă că beți suficiente lichide (cel puțin unul sau două pahare) înainte și după tratamentul cu Aclasta conform indicațiilor medicului dumneavoastră. Acest lucru va ajuta la prevenirea deshidratării. Puteți mânca normal în ziua tratamentului cu Aclasta. Acest lucru este deosebit de important la pacienții care iau diuretice (pastile de urinare) și la pacienții vârstnici (cu vârsta de 65 de ani sau peste).
Dacă uitați o doză de Aclasta
Contactați medicul sau spitalul cât mai curând posibil pentru a face o nouă întâlnire.
Înainte de a întrerupe tratamentul cu Aclasta
Dacă luați în considerare întreruperea tratamentului cu Aclasta, vă rugăm să veniți la următoarea întâlnire și să discutați acest lucru cu medicul dumneavoastră. Medicul dumneavoastră vă poate sfătui și decide cât timp să continuați tratamentul.
Dacă aveți orice întrebări suplimentare cu privire la acest medicament, adresați-vă medicului dumneavoastră, farmacistului sau asistentei medicale.
Efecte secundare Care sunt efectele secundare ale Aclasta
Ca toate medicamentele, acest medicament poate provoca reacții adverse, deși nu apar la toate persoanele.
Efectele secundare legate de prima perfuzie sunt foarte frecvente (apar la mai mult de 30% dintre pacienți), dar sunt mai puțin frecvente după perfuziile ulterioare. Cele mai multe reacții adverse, cum ar fi febra și frisoanele, durerea la nivelul mușchilor sau articulațiilor și cefaleea, apar în primele trei zile după administrarea Aclasta. Simptomele sunt de obicei ușoare până la moderate și dispar în termen de trei zile. Medicul dumneavoastră vă poate recomanda un analgezic ușor, cum ar fi ibuprofen sau acetaminofen, pentru a reduce aceste reacții adverse. Șansa de a avea efecte secundare scade odată cu dozele ulterioare de Aclasta.
Unele reacții adverse pot fi grave
Frecvente (pot afecta până la 1 din 10 persoane)
Ritmul cardiac neregulat (fibrilație atrială) a fost observat la pacienții tratați cu Aclasta pentru osteoporoză postmenopauză. În prezent nu este clar dacă Aclasta este cauza acestui ritm cardiac neregulat, însă trebuie să spuneți medicului dumneavoastră dacă după administrarea Aclasta prezintă astfel de simptome.
Mai puțin frecvente (pot afecta până la 1 din 100 de persoane)
Umflături, roșeață, durere și mâncărime a ochilor sau sensibilitate a ochilor la lumină.
Foarte rare (pot afecta până la 1 din 10000 de persoane)
Discutați cu medicul dumneavoastră dacă aveți dureri de urechi, scurgeri de urechi și / sau infecție a urechii. Aceste episoade ar putea fi semne de leziuni osoase la nivelul urechii. Cu frecvență necunoscută (frecvența nu poate fi estimată din datele disponibile) Durere în gură și / sau maxilară, umflături sau răni în gură sau maxilar care nu se vindecă, descărcare, amorțeală sau senzație de greutate în maxilar sau slăbirea unui dinte ; acestea ar putea fi semne de degenerare osoasă severă a maxilarului (osteonecroză). Spuneți imediat medicului dumneavoastră și medicului dentist dacă aveți astfel de simptome în timpul tratamentului cu Aclasta sau după oprirea tratamentului.
Pot apărea tulburări ale rinichilor (de exemplu, o cantitate scăzută de urină). Medicul dumneavoastră va trebui să extragă sânge pentru a vă verifica funcția renală înainte de fiecare perfuzie de Aclasta. Este important să beți cel puțin unul sau două pahare de lichide (de exemplu, apă) în câteva ore înainte de tratamentul cu Aclasta, conform instrucțiunilor medicului dumneavoastră.
Dacă aveți oricare dintre aceste reacții adverse, spuneți imediat medicului dumneavoastră.
Aclasta poate provoca și alte reacții adverse
Foarte frecvente (pot afecta mai mult de 1 din 10 persoane)
Febră
Frecvente (pot afecta până la 1 din 10 persoane)
Cefalee, amețeli, stare de rău, vărsături, diaree, dureri de corp, dureri osoase și / sau articulare, dureri la spate, brațe sau picioare, simptome asemănătoare gripei (de exemplu oboseală, frisoane, dureri articulare și musculare), frisoane, senzație de oboseală și lipsa de interes, slăbiciune, durere, stare de rău, umflături și / sau durere la locul perfuziei.
La pacienții cu boala Paget, au fost raportate simptome de calciu scăzut din sânge, cum ar fi spasme musculare sau amorțeală sau furnicături, în special în zona din jurul gurii.
Mai puțin frecvente (pot afecta până la 1 din 100 de persoane)
Gripă, infecții ale căilor respiratorii superioare, scăderea numărului de celule roșii din sânge, pierderea poftei de mâncare, insomnie, somnolență, care pot include scăderea vigilenței și conștiinței, furnicături sau amorțeli, oboseală extremă, tremor, pierderea temporară a conștienței, infecție oculară sau iritație sau inflamație cu durere și roșeață, senzație de amețeală, tensiune arterială crescută, înroșire, tuse, dificultăți de respirație, dureri de stomac, dureri abdominale, constipație, gură uscată, arsuri la stomac, erupții cutanate, transpirație excesivă, mâncărime, roșeață a pielii, dureri de gât, mușchi, os și / sau rigiditate articulară, umflături articulare, spasme musculare, dureri de umăr, dureri musculare toracice și toracice, inflamații articulare, slăbiciune musculară, rezultate anormale teste renale, dorință anormală frecventă de a urina, umflarea mâinilor, gleznelor sau picioarelor, sete, durere de dinți, mare rația de gust.
Rare (pot afecta până la 1 din 1000 de persoane)
Rareori, în special la pacienții tratați pe termen lung pentru osteoporoză, poate apărea o fractură neobișnuită a femurului. Contactați medicul dumneavoastră dacă aveți durere, slăbiciune sau disconfort la nivelul coapsei, șoldului sau inghinei, deoarece poate fi o „indicație timpurie a unei posibilă fractură a femurului.
Nu se cunoaște (frecvența nu poate fi estimată din datele disponibile)
reacții alergice severe, inclusiv amețeli și dificultăți de respirație, umflare în principal a feței și gâtului, scăderea tensiunii arteriale, deshidratare secundară simptomelor post-perfuzie, cum ar fi febră, vărsături și diaree.
Raportarea efectelor secundare
Dacă manifestați orice reacții adverse, adresați-vă medicului dumneavoastră, farmacistului sau asistentei medicale.Acestea includ orice posibile reacții adverse nemenționate în acest prospect. De asemenea, puteți raporta reacțiile adverse direct prin intermediul sistemului național de raportare enumerat în Anexa V. Reacțiile adverse pe care le puteți ajuta furnizați mai multe informații despre siguranța acestui medicament.
Expirare și reținere
Medicul dumneavoastră, farmacistul sau asistenta sunt sfătuiți cu privire la modul de păstrare corect Aclasta.
- Nu lăsați acest medicament la vederea și îndemâna copiilor.
- Nu utilizați acest medicament după data de expirare înscrisă pe cutie și flacon după EXP.
- Sticla nedeschisă nu necesită condiții speciale de depozitare.
- După deschiderea flaconului, produsul trebuie utilizat imediat pentru a evita contaminarea microbiană. Dacă nu este utilizat imediat, timpul și condițiile de depozitare în timpul utilizării sunt responsabilitatea utilizatorului și în mod normal nu ar trebui să depășească 24 de ore la 2 ° C - 8 ° C. Așteptați ca soluția luată din frigider să atingă temperatura camerei înainte de utilizare.
Alte informații
Ce conține Aclasta
Substanța activă este acidul zoledronic. Fiecare flacon de 100 ml de soluție conține 5 mg de acid zoledronic (sub formă de monohidrat). Un ml de soluție conține 0,05 mg de acid zoledronic (sub formă de monohidrat).
Celelalte componente sunt manitol, citrat de sodiu și apă pentru preparate injectabile.
Cum arată Aclasta și conținutul ambalajului
Aclasta este o soluție limpede și incoloră. Se livrează în flacoane de plastic de 100 ml sub formă de soluție gata de infuzat. Este livrat în cutii care conțin o sticlă pentru ambalaj unic sau în cutii cu doze multiple care conțin cinci ambalaje, câte o sticlă fiecare. Este posibil ca nu toate mărimile de ambalaj să fie comercializate.
Prospect sursă: AIFA (Agenția italiană pentru medicamente). Conținut publicat în ianuarie 2016. Este posibil ca informațiile prezente să nu fie actualizate.
Pentru a avea acces la cea mai actualizată versiune, este recomandabil să accesați site-ul web AIFA (Agenția italiană pentru medicamente). Declinare de responsabilitate și informații utile.
01.0 DENUMIREA PRODUSULUI MEDICAMENTAL
SOLUȚIE ACLASTA 5 MG PENTRU PERFUZIE
02.0 COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ
Fiecare flacon cu 100 ml soluție conține 5 mg acid zoledronic (sub formă de monohidrat).
Fiecare ml de soluție conține 0,05 mg acid zoledronic (sub formă de monohidrat).
Pentru lista completă a excipienților, vezi secțiunea 6.1.
03.0 FORMA FARMACEUTICĂ
Soluție perfuzabilă
Soluție clară și incoloră.
04.0 INFORMAȚII CLINICE
04.1 Indicații terapeutice
Tratamentul osteoporozei
• la femeile aflate în postmenopauză
• la bărbații adulți
cu risc crescut de fracturi, inclusiv cele cu un traumatism ușor recent fractură de șold.
Tratamentul osteoporozei asociate terapiei sistemice pe termen lung cu glucocorticoizi
• la femeile aflate în postmenopauză
• la bărbații adulți
cu risc crescut de fractură.
Tratamentul bolii osoase Paget la adulți.
04.2 Doze și mod de administrare
Dozare
Pacienții trebuie să fie hidrați în mod adecvat înainte de administrarea Aclasta. Acest lucru este deosebit de important pentru vârstnici (≥65 ani) și pentru pacienții tratați cu diuretic.
Se recomandă combinarea administrării Aclasta cu un supliment adecvat de calciu și vitamina D.
Osteoporoza
Pentru tratamentul osteoporozei postmenopauzale, osteoporozei la om și pentru tratamentul osteoporozei asociate terapiei sistemice pe termen lung cu glucocorticoizi, doza recomandată este o perfuzie intravenoasă unică de Aclasta 5 mg administrată o dată pe zi. Durata optimă a tratamentului cu bifosfonați pentru osteoporoză este de nu a fost stabilit. Necesitatea unui tratament continuu trebuie reevaluată periodic la fiecare pacient, în funcție de beneficiile și riscurile potențiale ale Aclasta, în special după 5 sau mai mulți ani de utilizare. La pacienții cu o fractură recentă de șold cu traume ușoare, se recomandă administrarea prin perfuzie de Aclasta la cel puțin două săptămâni după vindecarea fracturii de șold (vezi pct. 5.1). La pacienții cu o fractură ușoară recentă a șoldului, se recomandă o doză de încărcare de 50.000 până la 125.000 UI. Vitamina D, administrată oral sau intramuscular, înainte de prima perfuzie de Aclasta.
Boala Paget
Pentru tratamentul bolii Paget, Aclasta trebuie prescris numai de către medici cu experiență în tratamentul bolii Paget a osului. Doza recomandată este o perfuzie intravenoasă unică de Aclasta 5 mg. Pacienții cu boala Paget sunt sfătuiți să asigure un supliment adecvat de calciu corespunzător a cel puțin 500 mg de calciu elementar de două ori pe zi timp de cel puțin 10 zile după administrarea Aclasta (vezi pct. 4.4).
Retratarea bolii Paget: În boala Paget, s-a observat o perioadă prelungită de remisie la pacienții care au răspuns la tratamentul inițial cu Aclasta. Retratarea la pacienții recidivanti constă într-o „perfuzie intravenoasă suplimentară de Aclasta 5 mg după un interval de un an sau mai mult de la tratamentul inițial. Sunt disponibile date limitate despre retratarea bolii Paget (vezi pct. 5.1).
Populații speciale
Pacienți cu insuficiență renală
Aclasta este contraindicat la pacienții cu clearance-ul creatininei
Nu este necesară ajustarea dozei la pacienții cu clearance-ul creatininei ≥35 ml / min.
Pacienți cu insuficiență hepatică
Nu este necesară ajustarea dozei (vezi pct. 5.2).
Vârstnici (≥65 ani)
Deoarece biodisponibilitatea, distribuția și eliminarea au fost similare la subiecții vârstnici și mai tineri, nu este necesară ajustarea dozei.
Populația pediatrică
Siguranța și eficacitatea Aclasta la copii și adolescenți cu vârsta sub 18 ani nu au fost stabilite. Nu există date disponibile.
Mod de administrare
Utilizare intravenoasă.
Aclasta se administrează printr-o linie de perfuzie cu o membrană de ventilare și se administrează încet la o rată de perfuzie constantă. Timpul de perfuzare nu trebuie să fie mai mic de 15 minute. Pentru informații despre modul în care se administrează Aclasta, vezi pct. 6.6.
Pacienții tratați cu Aclasta trebuie să primească prospectul și cardul de reamintire a pacientului.
04.3 Contraindicații
- Hipersensibilitate la substanța activă, la orice bifosfonat sau la oricare dintre excipienții enumerați la punctul 6.1.
- Pacienți cu hipocalcemie (vezi pct. 4.4).
- Insuficiență renală severă cu clearance al creatininei
- Sarcina și alăptarea (vezi pct. 4.6).
04.4 Avertismente speciale și precauții adecvate pentru utilizare
Funcția renală
Utilizarea Aclasta la pacienții cu insuficiență renală severă (insuficiență renală cu eliminare a creatininei la această populație.
Insuficiența renală a fost observată după administrarea Aclasta (vezi pct. 4.8) în special la pacienții cu disfuncție renală preexistentă sau cu alți factori de risc, inclusiv vârsta înaintată, utilizarea concomitentă a medicamentelor nefrotoxice, terapia diuretică concomitentă (vezi pct. 4.5) sau deshidratare după administrarea Aclasta. Insuficiența renală a fost observată la pacienți după administrare unică. Insuficiența renală care implică necesitatea dializei sau cu un rezultat fatal a apărut rar la pacienții cu insuficiență renală subiacentă sau cu oricare dintre factorii de risc descriși mai sus. Pentru a minimiza riscul de reacții adverse renale, trebuie luate în considerare următoarele măsuri de precauție:
• Înainte de fiecare perfuzie de Aclasta, clearance-ul creatininei din greutatea corporală trebuie calculat utilizând formula Cockcroft-Gault.
• Creșterea tranzitorie a creatininei serice poate fi mai accentuată la pacienții cu insuficiență renală subiacentă.
• La pacienții cu risc trebuie luată în considerare monitorizarea periodică a creatininei serice.
• Aclasta trebuie utilizat cu precauție atunci când este administrat concomitent cu alte medicamente care pot afecta funcția renală (vezi pct. 4.5).
• Pacienții, în special pacienții vârstnici și cei care iau diuretice, trebuie să fie hidrați în mod adecvat înainte de administrarea Aclasta.
• O singură perfuzie de Aclasta nu trebuie să depășească 5 mg, iar durata perfuziei să fie de cel puțin 15 minute (vezi pct. 4.2).
Hipocalcemie
Hipocalcemia preexistentă trebuie tratată cu administrare adecvată de calciu și vitamina D înainte de inițierea tratamentului cu Aclasta (vezi pct. 4.3). Alte modificări ale metabolismului mineral trebuie, de asemenea, tratate în mod adecvat (de exemplu, rezerva paratiroidiană redusă, malabsorbția intestinală a calciului). Pentru acești pacienți, medicii trebuie să evalueze posibilitatea monitorizării clinice.
Rotația osoasă ridicată este o caracteristică a bolii osoase Paget. Datorită apariției rapide a efectului acidului zoledronic asupra fluctuației osoase, se poate dezvolta hipocalcemie tranzitorie, uneori simptomatică, atingând nivelurile maxime de obicei în decurs de 10 zile de la perfuzia cu Aclasta (vezi pct. 4.8).
Se recomandă combinarea administrării Aclasta cu un supliment adecvat de calciu și vitamina D. În plus, pacienții care suferă de boala Paget sunt sfătuiți să asigure un supliment adecvat de calciu corespunzător a cel puțin 500 mg de calciu de două ori pe zi cel puțin în 10 zile după administrarea Aclasta (vezi pct. 4.2). Pacienții trebuie informați cu privire la posibilele simptome cauzate de hipocalcemie și trebuie monitorizați corespunzător din punct de vedere clinic în perioada de risc.La pacienții cu boala Paget se recomandă măsurarea calciului seric înainte de perfuzia cu Aclasta. S-au raportat rareori dureri osoase, articulare și / sau musculare severe și invalidante la pacienții cărora li s-au administrat bifosfonați, inclusiv acid zoledronic (vezi pct. 4.8).
Osteonecroza mandibulei / maxilarului
Osteonecroza maxilarului a fost raportată în experiența de după punerea pe piață la pacienții tratați cu Aclasta (acid zoledronic) pentru osteoporoză (vezi pct. 4.8). Inițierea tratamentului sau un nou curs de tratament trebuie amânat la pacienții cu leziuni deschise nevindecate ale țesuturilor moi ale cavității bucale.Înainte de a începe tratamentul cu Aclasta la pacienții cu factori de risc concomitenti, se recomandă o examinare dentară cu proceduri dentare preventive și o evaluare individuală a raportului beneficiu-risc La evaluarea riscului pentru un pacient de a dezvolta osteonecroză a maxilarului, trebuie luate în considerare următoarele:
- Potența de a inhiba resorbția osoasă a medicamentului (risc mai mare pentru moleculele foarte puternice), calea de administrare (risc mai mare pentru administrarea parenterală) și doza cumulativă.
- Cancer, comorbidități (de exemplu: anemie, coagulopatii, infecție), fumat.
- Terapii concomitente: corticosteroizi, chimioterapie, inhibitori ai angiogenezei, radioterapie cap și gât.
- Igiena orală deficitară, boala parodontală, protezele prost fixate, istoricul bolilor dentare, procedurile dentare invazive, de exemplu: extracțiile dentare.
Toți pacienții trebuie încurajați să mențină o igienă orală bună, să se supună controalelor dentare de rutină și să raporteze imediat orice simptome orale, cum ar fi mobilitatea dinților, durere, umflarea sau nevindecarea rănilor sau descărcarea de gestiune în timpul tratamentului cu acid zoledronic. În cursul tratamentului, procedurile dentare invazive trebuie efectuate cu precauție și evitate în imediata apropiere a tratamentului cu acid zoledronic.
Programul de management pentru pacienții care dezvoltă osteonecroză a maxilarului ar trebui stabilit în strânsă colaborare între medicul curant și un dentist sau chirurg oral competent în osteonecroză a maxilarului. Trebuie luată în considerare întreruperea temporară a tratamentului cu acid zoledronic până când starea se rezolvă și factorii de risc concomitenti sunt atenuați acolo unde este posibil.
Osteonecroza canalului auditiv extern
Osteonecroza canalului auditiv extern a fost raportată împreună cu utilizarea bifosfonaților, predominant în asociere cu terapii pe termen lung. Factorii de risc posibili pentru osteonecroza canalului auditiv extern includ utilizarea de steroizi și chimioterapie și / sau factori de risc local, cum ar fi ca infecție sau traume. Osteonecroza canalului auditiv extern trebuie luată în considerare la pacienții tratați cu bifosfonați care prezintă simptome ale urechii, inclusiv infecții cronice ale urechii.
Fracturi atipice ale femurului
Au fost raportate fracturi atipice subtrocanteriene și ale femurului, în special la pacienții tratați cu bifosfonați pe termen lung pentru osteoporoză. Aceste fracturi transversale sau oblice scurte pot apărea oriunde în femur, chiar sub trohanterul mai mic până deasupra liniei supracondiliene. apar spontan sau după un traumatism minim și unii pacienți prezintă dureri de coapsă sau inghină, adesea asociate cu dovezi imagistice de fracturi de stres, săptămâni sau luni înainte de apariția unei fracturi de șold. Fracturile sunt adesea bilaterale; prin urmare, la pacienții tratați cu bifosfonat care au suferit o fractură a arborelui femural, femurul contralateral ar trebui examinat. De asemenea, a fost raportată vindecarea limitată a acestor fracturi.La pacienții cu suspiciune de fractură femurală atipică, întreruperea tratamentului cu bifosfonați ar trebui luată în considerare în așteptarea unei evaluări a pacientului pe baza raportului beneficiu-risc individual.
În timpul tratamentului cu bifosfonați, pacienții trebuie sfătuiți să raporteze orice durere la nivelul coapsei, șoldului sau inghinei și orice pacient care prezintă astfel de simptome trebuie evaluat pentru prezența unei fracturi incomplete a femurului.
General
Incidența simptomelor post-perfuzie care apar în primele trei zile după administrarea Aclasta poate fi redusă prin administrarea de paracetamol sau ibuprofen imediat după administrarea Aclasta.
Sunt disponibile și alte produse care conțin acid zoledronic ca substanță activă pentru indicații oncologice.Pacienții tratați cu Aclasta nu trebuie tratați concomitent cu aceste produse sau cu orice alt bifosfonat, deoarece efectele combinate ale acestor substanțe sunt necunoscute. Acest medicament conține mai puțin de 1 mmol sodiu (23 mg) per flacon de 100 ml Aclasta, deci, în esență, „fără sodiu”.
04.5 Interacțiuni cu alte medicamente și alte forme de interacțiune
Nu au fost efectuate studii de interacțiune cu alte medicamente. Acidul zoledronic nu este metabolizat sistemic și nu afectează in vitro activitatea enzimelor citocromului P450 uman (vezi pct. 5.2) .Acidul zoledronic nu se leagă extensiv de proteinele plasmatice (aproximativ 43-55% din medicament este legat) și, prin urmare, interacțiunile rezultate din deplasarea medicamentelor cu legare ridicată a proteinelor.
Acidul zoledronic este eliminat prin excreție renală. Aveți grijă dacă acidul zoledronic este administrat în asociere cu medicamente care pot avea un impact semnificativ asupra funcției renale (de exemplu aminoglicozide sau diuretice care pot provoca deshidratare) (vezi pct. 4.4).
La pacienții cu insuficiență renală, expunerea sistemică la medicamente administrate concomitent și excretate în principal prin rinichi poate fi crescută.
04.6 Sarcina și alăptarea
Femeile aflate la vârsta fertilă
Aclasta nu este recomandat la femeile aflate la vârsta fertilă.
Sarcina
Aclasta este contraindicat în timpul sarcinii (vezi pct. 4.3). Nu există date adecvate privind utilizarea acidului zoledronic la femeile gravide. Studiile efectuate la animale cu acid zoledronic au arătat toxicitate asupra funcției de reproducere, inclusiv malformații (vezi pct. 5.3). Nu se cunoaște riscul potențial pentru oameni.
Timp de hrănire
Aclasta este contraindicat în timpul alăptării (vezi pct. 4.3) Nu se știe dacă acidul zoledronic este excretat în laptele uman.
Fertilitate
Acidul zoledronic a fost evaluat la șobolani pentru potențialele efecte adverse asupra fertilității părinților și generației F1. Acest lucru a dus la efecte farmacologice accentuate considerate a fi legate de inhibarea mobilizării scheletice a calciului de către compus, rezultând hipocalcemie în timpul peripartului, un efect de clasă bifosfonat , distocie și încetarea precoce a studiului. Prin urmare, aceste rezultate nu permit determinarea unui efect definitiv al Aclasta asupra fertilității la om.
04.7 Efecte asupra capacității de a conduce vehicule și de a folosi utilaje
Reacțiile adverse, cum ar fi amețelile, pot afecta capacitatea de a conduce vehicule sau de a folosi utilaje.
04.8 Efecte nedorite
Rezumatul profilului de siguranță
Procentul total de pacienți care au prezentat reacții adverse a fost de 44,7%, 16,7% și 10,2% după prima, a doua și, respectiv, a treia perfuzie. Incidența reacțiilor adverse individuale după prima perfuzie a fost: febră (17,1%), mialgie (7,8%), boală asemănătoare gripei (6,7%), artralgie (4,8%) și cefalee (5,1%) Incidența acestor reacții a scăzut semnificativ cu doze anuale succesive de Aclasta. Majoritatea acestor reacții au apărut în primele trei zile după administrarea Aclasta. Majoritatea acestor reacții au fost ușoare până la moderate și s-au rezolvat în termen de trei zile de la apariția evenimentului. Într-un studiu mai mic în care profilaxia reacțiilor adverse a fost efectuată așa cum este descris mai jos, procentul pacienților care au prezentat reacții adverse a fost mai mic (19,5%, 10,4 %, 10,7% după prima, a doua și, respectiv, a treia perfuzie).
Tabelul reacțiilor adverse
Reacțiile adverse din Tabelul 1 sunt enumerate în funcție de clasa de sisteme și organe MedDRA și categoria de frecvență. Categoriile de frecvență sunt definite folosind următoarea convenție: foarte frecvente (≥1 / 10); frecvente (≥1 / 100,
tabelul 1
# Observat la pacienții care iau concomitent glucocorticoizi.
* Frecvente numai în boala Paget.
** Pe baza rapoartelor post-marketing. Frecvența nu poate fi estimată din datele disponibile.
† Identificat în timpul experienței post-marketing.
Descrierea reacțiilor adverse selectate
Fibrilatie atriala
În HORIZON - Pivotal Fracture Trial [PFT] (vezi pct. 5.1), incidența generală a fibrilației atriale a fost de 2,5% (96 din 3.862) și 1,9% (75 din 3.852) la pacienții tratați, respectiv cu Aclasta și placebo Rata evenimentelor adverse grave de fibrilație atrială a crescut la pacienții care au luat Aclasta (1,3%) (51 din 3862) comparativ cu pacienții cărora li sa administrat placebo (0,6%) (22 din 3852). Mecanismul din spatele incidenței crescute a fibrilației atriale este necunoscut. În studiile de osteoporoză (PFT, HORIZON - Recurrent Fracture Trial [RFT]), incidența combinată a fibrilației atriale a fost comparabilă între Aclasta (2,6%) și placebo (2,1%). Pentru evenimentele adverse grave de fibrilație atrială, incidența combinată a fost de 1,3% pentru Aclasta și 0,8% pentru placebo.
Efecte de clasă:
Insuficiență renală
Acidul zoledronic a fost asociat cu insuficiență renală evidențiată de deteriorarea funcției renale (adică creșterea creatininei serice) și, în cazuri rare, de insuficiență renală acută. După administrarea acidului zoledronic, în principal la pacienții cu disfuncție renală preexistentă sau cu factori de risc suplimentari ( de exemplu, vârsta înaintată, pacienții cu cancer supuși chimioterapiei, utilizarea concomitentă a medicamentelor nefrotoxice, terapia diuretică concomitentă, deshidratare severă) a fost observată insuficiență renală. În majoritatea cazurilor acești pacienți erau tratați cu o doză de 4 mg la fiecare 3-4 săptămâni, dar modificarea a fost detectată și după o singură administrare.
În studiile clinice privind osteoporoza, modificările clearance-ului creatininei (măsurate anual înainte de administrare) și incidența insuficienței renale și a insuficienței au fost comparabile atât în grupurile de tratament cu Aclasta, cât și în cele tratate cu placebo pe parcursul a trei ani. S-a observat o creștere tranzitorie a creatininei serice în primele 10 zile la 1,8% dintre pacienții tratați cu Aclasta comparativ cu 0,8% dintre pacienții tratați cu placebo.
Hipocalcemie
În studiile clinice de osteoporoză, aproximativ 0,2% dintre pacienți au prezentat o scădere considerabilă a concentrațiilor plasmatice de calciu (mai puțin de 1,87 mmol / l) după administrarea Aclasta. Nu au fost observate cazuri simptomatice de hipocalcemie.
În studiile privind boala Paget, s-a observat hipocalcemie simptomatică la aproximativ 1% dintre pacienți, cu retragere în toate cazurile.
Pe baza valorilor de laborator, nivelurile de calciu tranzitorii asimptomatice sub intervalul de referință normal (mai puțin de 2,10 mmol / L) au apărut la 2,3% dintre pacienții tratați cu Aclasta într-un studiu clinic amplu comparativ cu 21% dintre pacienții tratați cu Aclasta în studiile privind boala Paget. frecvența hipocalcemiei a fost mult mai mică în urma perfuziilor ulterioare.
Suplimentarea adecvată cu vitamina D și calciu a fost administrată tuturor pacienților înrolați în studiul de osteoporoză postmenopauză, studiului clinic de prevenire a fracturilor după fractura de șold și studiile privind boala Paget (vezi și secțiunea 4.2). nivelurile de vitamina D nu au fost măsurate în mod obișnuit, dar majoritatea pacienților au primit o doză de încărcare de vitamina D înainte de administrarea Aclasta (vezi punctul 4.2).
Reacții locale
Într-un studiu clinic amplu, au fost raportate reacții locale la locul perfuziei (0,7%), cum ar fi roșeață, umflături și / sau durere, după administrarea acidului zoledronic.
Osteonecroza mandibulei / maxilarului
Cazuri de osteonecroză (ale maxilarului) au fost raportate în principal la pacienții cu cancer tratați cu produse care inhibă resorbția osoasă, inclusiv acidul zoledronic (vezi pct. 4.4). un pacient tratat cu Aclasta și unul tratat cu placebo. Cazurile de osteonecroză a maxilarului au fost raportate în experiența de după punerea pe piață a Aclasta.
Raportarea reacțiilor adverse suspectate
Raportarea reacțiilor adverse suspectate care apar după autorizarea medicamentului este importantă, deoarece permite monitorizarea continuă a raportului beneficiu / risc al medicamentului. Profesioniștii din domeniul sănătății sunt rugați să raporteze orice reacție adversă suspectată prin intermediul sistemului național de raportare.
04.9 Supradozaj
Experiența clinică cu supradozaj acut este limitată.Pacienții care au fost tratați cu doze mai mari decât cele recomandate trebuie monitorizați cu o atenție deosebită.un supliment oral de calciu și / sau gluconat de calciu intravenos.
05.0 PROPRIETĂȚI FARMACOLOGICE
05.1 Proprietăți farmacodinamice
Grupa farmacoterapeutică: medicamente pentru tratamentul bolilor osoase, bifosfonați, codul ATC: M05BA08
Mecanism de acțiune
Acidul zoledronic aparține clasei de bifosfonați care conțin azot și acționează în principal asupra țesutului osos.Este un inhibitor al procesului de resorbție osoasă mediată de osteoclasti.
Efecte farmacodinamice
Acțiunea selectivă a bifosfonaților asupra osului se datorează afinității lor ridicate pentru osul mineralizat.Tinta moleculară principală a acidului zoledronic este enzima farnesil pirofosfat sintetază în osteoclast. Durata lungă de acțiune a acidului zoledronic este atribuită afinității sale de legare ridicate pentru situsul activ al farnesil pirofosfatului (FPP) sintetază și afinității sale puternice față de osul mineralizat.
Tratamentul cu Aclasta a redus rapid rata fluctuației osoase de la niveluri postmenopauzale ridicate, cu scăderea markerilor de resorbție observată în ziua 7 și a markerilor de formare în săptămâna 12. Ulterior, markerii osoși s-au stabilizat în intervalele premenopauzale. Nu a existat o reducere progresivă a markerilor de rotație osoasă cu dozare anuală repetată.
Eficacitate clinică în tratamentul osteoporozei postmenopauzale (PFT)
Eficacitatea și siguranța Aclasta 5 mg o dată pe an timp de 3 ani consecutivi a fost demonstrată la femeile aflate în postmenopauză (7.736 femei cu vârsta cuprinsă între 65 și 89 de ani) cu: Densitate minerală osoasă (BMD) scor T col femural ≤ -1,5 și cel puțin două pre -fracturi vertebrale ușoare sau una moderată existente; sau Scorul femural al gâtului femural ≤ -2,5 cu sau fără dovezi ale fracturilor vertebrale preexistente. 85% dintre pacienți au urmat primul tratament cu bifosfonați. Femeile evaluate pentru incidența fracturilor vertebrale nu au primit terapie concomitentă cu osteoporoză, care a fost administrată femeilor evaluate pentru fracturi de șold și toate fracturile. Terapia concomitentă pentru osteoporoză a inclus: calcitonină, raloxifen, tamoxifen, terapie de substituție hormonală, tibolonă, dar a exclus alți bifosfonați. Toate femeile au primit 1.000 până la 1.500 mg de calciu elementar și 400 până la 1.200 UI supliment zilnic.
Efect asupra fracturilor vertebrale morfometrice
Aclasta a redus semnificativ incidența uneia sau mai multor fracturi vertebrale noi pe parcursul a trei ani și încă din studiul din primul an (vezi Tabelul 2).
Tabelul 2 Rezumatul eficacității în fracturile vertebrale la 12, 24 și 36 de luni
Pacienții cu vârsta de 75 de ani sau peste tratați cu Aclasta au prezentat o reducere cu 60% a riscului de fracturi vertebrale comparativ cu pacienții tratați cu placebo (p
Efect asupra fracturilor de șold
Aclasta a demonstrat un efect consecvent pe parcursul a 3 ani, rezultând o reducere de 41% a riscului de fracturi de șold (IC 95%, 17% până la 58%). grupul placebo. Reducerea riscului a fost de 51% la pacienții care au primit primul tratament cu bifosfonați și de 42% la pacienții cărora li s-a administrat concomitent terapia cu osteoporoză.
Efect asupra tuturor fracturilor clinice
Toate fracturile clinice au fost examinate pe baza dovezilor radiografice și / sau clinice. Un rezumat al rezultatelor este prezentat în Tabelul 3.
Tabelul 3 Compararea tratamentelor în incidența variabilelor majore ale fracturii clinice pe parcursul a 3 ani
Efect asupra densității minerale osoase (BMD)
Aclasta a crescut semnificativ coloana lombară, șoldul și raza distală DMO în raport cu tratamentul cu placebo în toate punctele de timp (6, 12, 24 și 36 de luni). Tratamentul cu Aclasta a arătat o creștere cu 6,7% a DMO coloanei lombare, 6,0% șold total, 5,1% gât femural și 3,2% rază distală comparativ cu placebo în cei 3 ani de tratament.
Histologie osoasă
La 152 de pacienți postmenopauzi cu osteoporoză tratați cu Aclasta (N = 82) și placebo (N = 70), biopsiile osoase au fost obținute din creasta iliacă la 1 an după a treia doză anuală. Analiza histomorfometrică a arătat o reducere cu 63% a fluctuației osoase. Osteomalacia, fibroza chistică și formarea de os țesut. Cu excepția unui caz, markerul de tetraciclină a fost găsit în toate cele 82 de biopsii efectuate la pacienții tratați cu Aclasta. Tomografia microcomputerizată (µCT) a demonstrat o creștere a volumului osului trabecular și menținerea arhitecturii osului trabecular. "Osul trabecular la pacienți tratat cu Aclasta comparativ cu grupul placebo.
Marker de rotire a oaselor
Evaluări ale fosfatazei alcaline specifice osului (BALP), propeptidei serice de colagen N-terminal de tip I (P1NP) și telopeptidelor serice beta-C (b-CTx) în subgrupuri de 517-1246 pacienți la intervale periodice pe parcursul studiului. Tratamentul cu o doză anuală de 5 mg Aclasta a redus semnificativ BALP cu 30% față de valoarea inițială la 12 luni, care a fost menținut la 28% sub valoarea inițială la 36 luni. P1NP a scăzut semnificativ cu 61% sub nivelul inițial de 12 luni și a rămas cu 52% sub nivelul inițial de 36 de luni. B-CTx a fost redus semnificativ cu 61% față de valoarea inițială la 12 luni și a rămas cu 55% sub nivelul inițial la 36 luni. De-a lungul perioadei de timp observate, markerii de rotație osoasă au rămas în intervalul de pre-menopauză la sfârșitul fiecărui an. Dozarea repetată nu a condus la reduceri suplimentare ale markerilor de rotație osoasă.
Efect pe înălțime
În studiul de trei ani asupra osteoporozei, înălțimea în picioare a fost măsurată anual cu ajutorul unui stadiometru. Grupul tratat cu Aclasta a prezentat o reducere a staturii cu aproximativ 2,5 mm mai mică decât grupul placebo (95% CI: 1,6 mm, 3,5 mm) [p = 0,0001].
Zile de handicap
Comparativ cu placebo, Aclasta a redus semnificativ zilele medii de activitate redusă și zilele de odihnă la pat din cauza durerii lombare cu 17,9 zile și respectiv 11,3 zile, reducând totodată zilele medii de activitate redusă. 2,9 zile și respectiv 0,5 zile, comparativ cu placebo (p = 0,01).
Eficacitate clinică în tratamentul osteoporozei la pacienții cu risc crescut de fracturi după o fractură recentă de șold (RFT)
Incidența fracturilor clinice, vertebrale, non-vertebrale și a fracturilor de șold incluse a fost evaluată la 2.127 bărbați și femei cu vârsta cuprinsă între 50-95 de ani (vârsta medie 74,5 ani), cu o fractură recentă (în decurs de 90 de zile) de șold din cauza unui traumatism ușor care a fost urmat cu tratament de studiu (Aclasta) timp de 2 ani în medie. La aproximativ 42% dintre pacienți, scorul T al gâtului femural a fost mai mic de -2,5 și la aproximativ 45% dintre pacienți au avut un scor T al gâtului femural mai mare de -2,5. Aclasta a fost administrat anual până la confirmarea fracturilor clinice la cel puțin 211 de pacienți din populația studiată. Nivelurile de vitamina D nu au fost măsurate în mod obișnuit, dar o doză de încărcare de vitamina D (50.000 până la 125.000 UI pe cale orală sau intramusculară) a fost administrată majorității pacienților cu 2 săptămâni înainte de perfuzie. Toți participanții au luat 1.000 până la 1.500 mg de calciu elementar plus 800 până la 1.200 UI supliment de vitamina D. zilnic. 95% dintre pacienți au primit perfuzia la două sau mai multe săptămâni după repararea fracturii de șold și timpul mediu până la perfuzie. Aproximativ șase săptămâni după repararea fracturii de șold. studiu.
Efect asupra tuturor fracturilor clinice
Ratele de incidență ale principalelor variabile clinice de fractură sunt prezentate în Tabelul 4.
Tabelul 4 Comparație între tratamente în incidența principalelor variabile de fractură clinică
Studiul nu a fost conceput pentru a măsura diferențe semnificative în fracturile de șold, dar s-a observat o tendință în favoarea reducerii noilor fracturi de șold. În grupul tratat cu Aclasta, mortalitatea cauzată de toate cauzele a fost de 10% (101 pacienți) comparativ cu 13% (141 pacienți) din grupul placebo. Aceasta corespunde unei reduceri a riscului de mortalitate prin toate cauzele de 28% (p = 0,01).
Incidența vindecării întârziate a fracturilor de șold a fost comparabilă între Aclasta (34 [3,2%]) și placebo (29 [2,7%]).
Efect asupra densității minerale osoase (BMD)
În studiul HORIZON-RFT, tratamentul cu Aclasta a crescut semnificativ DMO totală a șoldului și gâtului femural comparativ cu tratamentul placebo în toate punctele de timp. Tratamentul cu Aclasta a arătat o creștere de 5,4%. .
Eficacitate clinică la om
În studiul HORIZON-RFT, 508 bărbați au fost randomizați și 185 de pacienți au fost evaluați pentru BMD în luna 24. O creștere similară semnificativă cu 3,6% a BMD total comparabilă a șoldului a fost observată în luna 24 la pacienții tratați cu Aclasta. Efectele observate la femeile aflate în postmenopauză în studiul HORIZON-PFT. Studiul nu a fost dimensionat pentru a demonstra o reducere a fracturilor clinice la om; incidența fracturilor clinice a fost de 7,5% la bărbații tratați cu Aclasta comparativ cu 8,7% la placebo. "Bărbat (studiu CZOL446M & SUP2; 308) DMO în luna 24 față de valoarea inițială a fost mai mică după o „perfuzie anuală de Aclasta comparativ cu alendronatul administrat săptămânal.
Eficacitatea clinică în osteoporoză indusă de terapia sistemică pe termen lung cu glucocorticoizi control pe 833 bărbați și femei cu vârste cuprinse între 18 și 85 de ani (vârsta medie pentru bărbați 56,4 ani; pentru femei 53,5 ani) tratați cu> 7,5 mg / zi de prednison pe cale orală (sau echivalent). Pacienții au fost stratificați după durata tratamentului cu glucocorticoizi înainte de randomizare (≤3 luni versus> 3 luni). Durata studiului a fost de un an. Pacienții au fost randomizați la Aclasta 5 mg perfuzie simplă sau risedronat oral 5 mg zilnic timp de un an. Toți au primit 1.000 mg de calciu elementar zilnic plus un supliment de 400 până la 1.000 UI vitamina D. cia a fost demonstrată cu un design de non-inferioritate la risedronat prin prezentarea secvențială a modificării procentuale a DMO coloanei vertebrale la luna 12 față de valoarea inițială în subpopulațiile de tratament și, respectiv, de prevenire. Majoritatea pacienților au continuat să ia glucocorticoizi pe durata unui an de studiu.
Efect asupra densității minerale osoase (BMD)
Creșterile DMO în coloana vertebrală și gâtul femural în luna 12 au fost semnificativ mai mari în grupul de tratament cu Aclasta comparativ cu risedronatul (p
Eficacitatea clinică în tratamentul bolii Paget a osului Aclasta a fost studiată la pacienți de sex masculin și feminin cu vârsta peste 30 de ani, cu boală Paget osoasă ușoară până la moderată (nivel mediu seric de fosfatază alcalină 2, de 6-3,0 ori mai mare decât vârsta limita normală la înscrierea la studiu) confirmată prin examen radiologic.
Eficacitatea unei perfuzii de 5 mg acid zoledronic versus risedronat 30 mg zilnic administrat timp de 2 luni a fost demonstrată în două studii comparative cu durata de 6 luni. După 6 luni, Aclasta a prezentat rate de 96% (169/176) și 89% (156/176) de răspuns terapeutic și normalizarea fosfatazei alcaline serice (SAP) comparativ cu 74% (127/171) și 58% (99 / 171) obținut cu risedronat (întotdeauna p
Cu rezultatele cumulate, s-a observat o scădere similară a severității durerii și a scorurilor de interferență a durerii peste 6 luni de la momentul inițial pentru Aclasta și risedronat.
Pacienții care au fost clasificați ca respondenți la tratament la sfârșitul studiului de bază de 6 luni au fost considerați eligibili pentru a fi incluși în perioada extinsă de evaluare. Dintre cei 153 de pacienți tratați cu Aclasta și 115 pacienți tratați cu risedronat care au intrat în perioada de observație extinsă a studiului, după o perioadă medie de urmărire de 3,8 ani după administrare, proporția pacienților care au finalizat studiul a prelungit observația din cauza necesității pentru retratare (judecata clinică) a fost mai mare pentru risedronat (48 de pacienți, 41,7%) decât pentru acidul zoledronic (11 pacienți, 7,2%). Timpul mediu până la terminarea perioadei de observație prelungită din cauza necesității retratării Paget din doza inițială a fost mai lung pentru acidul zoledronic (7,7 ani) decât pentru risedronat (5,1 ani).
Șase pacienți care au obținut un răspuns terapeutic la 6 luni după tratamentul cu Aclasta și care au avut apoi recidiva bolii în timpul perioadei prelungite de evaluare au fost retrași cu Aclasta după un timp mediu de 6,5 ani între inițială și reprocesare. Cinci din cei 6 pacienți au avut niveluri serice de fosfatază alcalină în intervalul normal în luna a 6-a (Ultima observație purtată înainte, LOCF).
Histologia osoasă a fost evaluată la 7 pacienți cu boala Paget la 6 luni după tratamentul cu 5 mg acid zoledronic. Aceste rezultate au fost în acord cu markerul biochimic al dovezilor de normalizare a fluctuației osoase.
Agenția Europeană a Medicamentului a renunțat la obligația de a prezenta rezultatele studiilor cu Aclasta în toate subgrupurile de copii și adolescenți pentru boala Paget a oaselor, osteoporoză la femeile aflate în postmenopauză cu risc crescut de fractură, osteoporoză la bărbații cu risc crescut de fractură și prevenirea fracturilor clinice după o fractură de șold la bărbați și femei (vezi pct. 4.2 pentru informații despre utilizarea la copii și adolescenți).
05.2 Proprietăți farmacocinetice
Infuziile simple și multiple de 5 și 15 minute de 2, 4, 8 și 16 mg acid zoledronic la 64 de pacienți au prezentat următoarele date farmacocinetice, indiferent de doză.
Distribuție
După începerea perfuziei cu acid zoledronic, concentrațiile plasmatice ale substanței active au crescut rapid, ajungând la vârf la sfârșitul perioadei de perfuzie, urmată de o scădere rapidă.
Eliminare
După administrarea intravenoasă, acidul zoledronic este eliminat printr-un proces în trei etape: dispariție rapidă cu un curs bifazic din circulația sistemică, cu perioade de înjumătățire de ½a 0,24 și t½b 1,87 ore, urmată de o fază lungă de eliminare cu timp de înjumătățire de eliminare terminal de t½g 146 ore. Nu s-a observat nicio acumulare de substanță activă în plasmă după doze multiple administrate la fiecare 28 de zile. absorbție osoasă și excreție renală. Acidul zoledronic nu este metabolizat și este excretat nemodificat prin rinichi. În primele 24 de ore, 39 ± 16% din doza administrată este recuperată în urină, în timp ce restul este legat în principal de țesutul osos. Această absorbție în os este comună pentru toți bifosfonații și este probabil o consecință a analogiei structurale cu pirofosfatul. Ca și în cazul altor bifosfonați, timpul de retenție al acidului zoledronic în oase este foarte lung. De la os medicamentul este eliberat foarte lent în circulația sistemică și apoi eliminat prin rinichi. Clearance-ul total al corpului este de 5,04 ± 2,5 l / h, indiferent de de doză și nu este influențată de sex, vârstă, rasă sau greutatea corporală. Variația clearance-ului plasmatic al acidului zoledronic între și la indivizi a fost de 36% și respectiv 34%. Creșterea timpului de perfuzie de la 5 la 15 minute a dus la o scădere cu 30% a concentrației de acid zoledronic la sfârșitul perfuziei, dar nu a avut niciun efect asupra zonei sub curba concentrației plasmatice versus timp.
Relații farmacocinetice / farmacodinamice
Nu s-au efectuat studii de interacțiune cu alte medicamente și acid zoledronic. Deoarece acidul zoledronic nu este metabolizat la om și s-a constatat că substanța are o capacitate mică sau deloc de inhibitor al metabolismului cu acțiune directă și / sau ireversibilă. Dependent de enzimele P450 , acidul zoledronic este puțin probabil să reducă clearance-ul metabolic al substanțelor metabolizate prin intermediul sistemelor enzimatice citocromului P450. Acidul zoledronic nu este legat în mod extensiv de proteinele plasmatice (legat de aproximativ 43-55%) și legătura este independentă de concentrație. Prin urmare, interacțiunile rezultate din deplasarea medicamentelor puternic legate de proteine sunt improbabile.
Populații speciale (vezi pct. 4.2)
Insuficiență renală
Clearance-ul renal al acidului zoledronic a fost corelat cu clearance-ul creatininei, deoarece clearance-ul renal reprezintă 75 ± 33% din clearance-ul creatininei, care a fost în medie de 84 ± 29 ml / min la 64 de pacienți studiați (interval 22 - 143 ml / min). creșterile observate în ASC (0-24 ore), între aproximativ 30% și 40% în cazul insuficienței renale ușoare până la moderate, comparativ cu pacienții cu funcție renală normală și absența acumulării de medicamente după doze multiple, indiferent de funcția renală, sugerează că nu există doză sunt necesare ajustări ale acidului zoledronic la insuficiența renală ușoară (Clcr = 50-80 ml / min) și moderată până la clearance-ul creatininei de 35 ml / min. Utilizarea Aclasta la pacienții cu insuficiență renală severă (clearance-ul creatininei
05.3 Date preclinice de siguranță
Toxicitate acuta
Doza maximă neletală pentru administrare intravenoasă unică a fost de 10 mg / kg greutate corporală la șoarece și 0,6 mg / kg la șobolan. În studiile de perfuzie cu doză unică la câini, 1,0 mg / kg (de 6 ori expunerea terapeutică recomandată la om pe baza ASC) administrată timp de 15 minute a fost bine tolerată, fără efecte renale.
Toxicitate subcronică și cronică
În studiile de perfuzie intravenoasă, tolerabilitatea renală a acidului zoledronic a fost stabilită la șobolani cu administrare de 0,6 mg / kg ca perfuzii de 15 minute la intervale de 3 zile, pentru un total de șase perfuzii (pentru o doză cumulativă corespunzătoare nivelurilor ASC de aproximativ 6 de 5 ori expunerea terapeutică umană) în timp ce cinci perfuzii de 15 minute de 0,25 mg / kg administrate la intervale de 2-3 săptămâni (o doză cumulativă corespunzătoare de 7 ori l "expunere terapeutică umană) au fost bine tolerate la câini. În studiile pe bolus intravenos, dozele care au fost bine tolerate au scăzut odată cu creșterea duratei studiului: dozele de 0,2 și 0,02 mg / kg pe zi au fost bine tolerate timp de 4 săptămâni la șobolani și respectiv câini, dar numai dozele de 0,01 mg / kg și 0,005 mg / kg au fost bine tolerate în șobolani și, respectiv, câini, atunci când sunt administrați timp de 52 de săptămâni.
Administrarea repetată pe termen lung, la expuneri cumulative suficient de mari decât expunerea maximă așteptată la om, a produs efecte toxicologice în alte organe, inclusiv tractul gastro-intestinal și ficatul, și la locul administrării intravenoase. Nu se cunoaște relevanța clinică a acestor constatări. Cea mai frecventă constatare în studiile cu doze repetate este creșterea țesutului osos spongios în metafizele oaselor lungi la animale în curs de dezvoltare la aproape toate dozele, reflectând activitatea farmacologică anti-resorptivă a produsului.
Toxicitate reproductiva
Studiile de teratologie au fost efectuate pe două specii, ambele utilizând administrare subcutanată. Teratogenitatea a fost observată la șobolani la doze ≥0,2 mg / kg și a dus la malformații externe, viscerale și scheletice. Distocie a fost observată la cea mai mică doză testată la șobolan (0,01 mg / kg greutate corporală). Nu s-au observat efecte teratogene sau embrionare / fetale la iepuri, deși toxicitatea maternă a fost marcată la doza de 0,1 mg / kg din cauza nivelurilor scăzute de calciu seric.
Mutagenitate și potențial cancerigen
Acidul zoledronic nu a fost mutagen în testele de mutagenitate efectuate, iar testele de carcinogenitate nu au furnizat dovezi ale potențialului cancerigen.
06.0 INFORMAȚII FARMACEUTICE
06.1 Excipienți
Manitol
Citrat de sodiu
Apă pentru preparate injectabile
06.2 Incompatibilitate
Acest medicament nu trebuie să intre în contact cu soluții care conțin calciu. Aclasta nu trebuie amestecat sau administrat intravenos cu alte medicamente.
06.3 Perioada de valabilitate
Sticlă nedeschisă: 3 ani
După deschidere: 24 de ore la 2 ° C - 8 ° C
Din punct de vedere microbiologic, produsul trebuie utilizat imediat. Dacă nu este utilizat imediat, timpul și condițiile de păstrare în timpul utilizării sunt responsabilitatea utilizatorului și în mod normal nu ar trebui să depășească 24 de ore la 2 ° C - 8 ° C.
06.4 Precauții speciale pentru depozitare
Acest medicament nu necesită condiții speciale de păstrare.
Pentru condițiile de depozitare a medicamentului după prima deschidere, vezi pct. 6.3.
06.5 Natura ambalajului imediat și conținutul ambalajului
100 ml soluție într-o sticlă din plastic transparent (polimer cicloolefinic) închis cu un dop din cauciuc bromobutilic acoperit cu fluoropolimer și un capac din aluminiu / polipropilenă cu element de închidere.
Aclasta este livrat în ambalaje unice care conțin o sticlă sau în ambalaje multiple formate din cinci ambalaje, fiecare conținând o sticlă.
Este posibil ca nu toate mărimile de ambalaj să fie comercializate.
06.6 Instrucțiuni de utilizare și manipulare
Doar pentru o singură utilizare.
Soluția trebuie utilizată numai dacă este limpede, fără particule sau decolorare.
Dacă se păstrează în frigider, lăsați soluția să atingă temperatura camerei înainte de administrare. Tehnicile aseptice trebuie urmate în timpul preparării perfuziei. Produsul medicinal neutilizat și deșeurile derivate din acest medicament trebuie eliminate în conformitate cu reglementările locale.
07.0 DEȚINĂTORUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
Novartis Europharm Limited
Parcul de afaceri Frimley
Camberley GU16 7SR
Regatul Unit
08.0 NUMĂRUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
EU / 1/05/308/001
EU / 1/05/308/002
037105018
09.0 DATA PRIMEI AUTORIZAȚII SAU REÎNNOIREA AUTORIZAȚIEI
Data primei autorizații: 15 aprilie 2005
Data ultimei reînnoiri: 19 aprilie 2015