Ingrediente active: brivudină
Brivirac 125 mg comprimate
De ce se utilizează Brivirac? Pentru ce este?
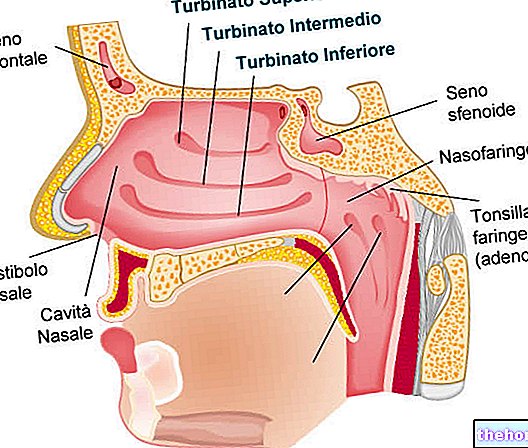
Brivirac conține substanța activă brivudină. Brivirac are un efect antiviral și previne multiplicarea virusului care provoacă Focul Sfântului Antonie (virusul varicelo-zoster).
Brivirac este utilizat la adulții care nu prezintă anomalii ale sistemului imunitar (apărarea corpului) pentru tratamentul precoce al focului Sf. Antonie (herpes zoster).
Contraindicații Când nu trebuie utilizat Brivirac
Nu luați Brivirac
- dacă sunteți alergic (hipersensibil) la substanța activă brivudină
- dacă sunteți alergic (hipersensibil) la oricare dintre celelalte componente ale Brivirac (vezi pct. 6)
- dacă sunteți gravidă sau alăptați
- dacă aveți sub 18 ani.
În special, NU luați Brivirac:
- dacă luați medicamente anticanceroase (chimioterapie), în special dacă sunteți tratat cu:
- 5-fluorouracil (numit și 5-FU, o substanță activă aparținând grupului numit 5-fluoropirimidine)
- creme, unguente, picături oftalmice sau orice altă formă de medicament de uz extern care conține 5-fluorouracil
- ingrediente active transformate de organism în 5-fluorouracil, cum ar fi:
- capecitabină
- floxuridină
- tegafur
- orice alt ingredient activ din grupa 5-fluoropirimidină
- asociații ale ingredientelor active menționate anterior
- dacă sistemul imunitar (de exemplu, apărarea organismului împotriva infecțiilor) este grav compromis; de exemplu. dacă sunteți tratat cu:
- medicamente anticanceroase (chimioterapie) sau
- medicamente imunosupresoare (adică medicamente care suprimă sau scad funcția sistemului imunitar)
- dacă luați un medicament care conține flucitozină pentru a trata o infecție fungică.
- dacă luați un medicament pentru negi care conține o substanță activă din grupul 5-fluoropirimidină.
Precauții pentru utilizare Ce trebuie să știți înainte de a lua Brivirac
Discutați cu medicul dumneavoastră sau farmacistul înainte de a lua Brivirac.
Nu luați Brivirac împreună cu medicamente care conțin 5-FU sau alte 5-fluoropirimidine (vezi secțiunile „Nu luați Brivirac” și „Alte medicamente și Brivirac”).
Nu luați Brivirac dacă erupția cutanată sa dezvoltat deja complet (apariția crustelor). În caz de îndoială, adresați-vă medicului dumneavoastră.
Adresați-vă medicului dumneavoastră pentru recomandări înainte de a lua Brivirac dacă aveți boli hepatice cronice (de exemplu, hepatită cronică).
Nu trebuie să luați Brivirac mai mult de 7 zile, deoarece prelungirea duratei tratamentului dincolo de timpul recomandat de 7 zile crește riscul apariției hepatitei (vezi și secțiunea 4).
Copii și adolescenți
Nu administrați Brivirac copiilor și adolescenților cu vârsta cuprinsă între 0 și 18 ani, deoarece siguranța și eficacitatea nu au fost studiate la această grupă de vârstă.
Interacțiuni Ce medicamente sau alimente pot modifica efectul Brivirac
Spuneți medicului dumneavoastră sau farmacistului dacă luați, ați luat recent sau s-ar putea să luați orice alte medicamente, inclusiv medicamente eliberate fără prescripție medicală.
VĂ RUGĂM SĂ REȚINEȚI:
Avertisment special pentru pacienții tratați cu produse care conțin 5-fluorouracil sau alte 5-fluoropirimidine (vezi și caseta roșie de mai sus):
Brivirac nu trebuie utilizat concomitent cu niciun medicament de chimioterapie care conține oricare dintre următoarele substanțe active, deoarece efectele nocive ale acestor medicamente pot fi mult crescute și pot fi fatale:
- 5-fluorouracil, inclusiv forme care trebuie utilizate local
- capecitabină
- floxuridină
- tegafur
- alte 5-fluoropirimidine
- combinații ale oricăreia dintre substanțele de mai sus cu alte ingrediente active.
Nu luați Brivirac împreună cu medicamente care conțin substanța activă flucitozină utilizată pentru tratamentul infecțiilor fungice. Nu luați Brivirac și contactați imediat medicul dumneavoastră dacă:
- urmează un tratament bazat pe oricare dintre medicamentele de mai sus
- veți fi tratat cu oricare dintre medicamentele de mai sus în termen de 4 săptămâni după terminarea tratamentului cu Brivirac.
Dacă ați luat accidental Brivirac concomitent cu oricare dintre medicamentele enumerate mai sus:
- opriți administrarea ambelor medicamente
- consultați imediat un medic. Poate fi necesar să mergeți la spital pentru tratament.
Simptomele și semnele toxicității 5-fluorouracilului datorate interacțiunilor de mai sus includ:
- stare de rău; diaree; inflamația gurii și / sau a mucoasei interioare a gurii; scăderea numărului de celule albe din sânge și depresie a măduvei osoase; erupții cutanate și roșeață pe tot corpul, cu pielea dureroasă la atingere, urmată de vezicule mari care duc la zone extinse de exfoliere a pielii (necroliză epidermică toxică) (vezi și secțiunea 4).
- Experiența după punerea pe piață indică o posibilă interacțiune a brivudinei cu medicamente dopaminergice împotriva bolii Parkinson, care poate favoriza apariția unui atac de coree (mișcări anormale, involuntare, asemănătoare dansului, în special ale brațelor, picioarelor și feței). Brivirac cu alimente și băuturi Puteți lua Brivirac cu sau fără alimente.
Avertismente Este important să știm că:
Sarcina și alăptarea
Adresați-vă medicului dumneavoastră sau farmacistului pentru recomandări înainte de a utiliza orice medicament.
Nu utilizați Brivirac în timpul sarcinii.
Nu utilizați Brivirac dacă alăptați. Substanța activă din Brivirac poate trece la copilul dumneavoastră prin laptele matern.
Conducerea vehiculelor și utilizarea utilajelor
Amețeli și somnolență au fost observate la unii pacienți care au luat Brivirac, deși mai puțin frecvente. Dacă observați aceste reacții adverse, nu conduceți vehicule, nu folosiți utilaje sau faceți lucrări fără sprijin sigur. Adresați-vă medicului dumneavoastră pentru sfaturi.
Brivirac conține lactoză
Acest medicament conține lactoză. Dacă medicul dumneavoastră v-a spus că aveți intoleranță la unele zaharuri, contactați medicul înainte de a lua acest medicament.
Doză, metodă și timp de administrare Cum se utilizează Brivirac: Doze
Luați întotdeauna acest medicament așa cum v-a spus medicul dumneavoastră. Dacă nu sunteți sigur, consultați medicul sau farmacistul.
Doza recomandată este:
1 comprimat Brivirac 125 mg o dată pe zi timp de 7 zile.
Luați comprimatul Brivirac aproximativ la aceeași oră în fiecare zi.
Brivirac poate fi luat cu sau fără alimente.
Înghițiți comprimatul întreg cu o cantitate suficientă de lichid, de ex. un pahar de apă.
Ar trebui să începeți tratamentul cât mai curând posibil, ceea ce înseamnă că, dacă este posibil, ar trebui să începeți să luați Brivirac:
- în termen de 3 zile de la apariția primelor semne cutanate ale focului Sf. Antonie (erupție cutanată) sau
- în termen de 2 zile de la apariția primelor vezicule.
Completați tratamentul de 7 zile chiar dacă vă simțiți mai bine mai devreme.
Dacă simptomele persistă sau se agravează în timpul săptămânii de tratament, vă rugăm să vă adresați medicului dumneavoastră.
Administrarea dozei obișnuite de Brivirac reduce riscul de a dezvolta nevralgie postherpetică la pacienții cu vârsta peste 50 de ani. Nevralgia postpetică este durerea persistentă care se dezvoltă în zona afectată anterior de zona zoster după ce erupția cutanată s-a îmbunătățit.
Durata tratamentului
Acest medicament este destinat utilizării pe termen scurt. Trebuie administrat doar timp de 7 zile. Nu luați acest medicament pentru un al doilea curs de tratament.
Utilizare la copii și adolescenți
Nu luați Brivirac dacă aveți vârsta sub 18 ani.
Dacă uitați să luați Brivirac
Dacă uitați să luați comprimatul la ora obișnuită, luați-l imediat ce vă amintiți. Luați următoarea tabletă a doua zi, cam la aceeași oră cu ziua precedentă. ciclu de tratament.zile.
Nu luați o doză dublă pentru a compensa un comprimat uitat.
Dacă uitați în mod repetat să luați doza zilnică, vă rugăm să spuneți medicului dumneavoastră.
Dacă încetați să luați Brivirac
Nu încetați să luați Brivirac fără a vă consulta mai întâi medicul. Pentru ca tratamentul să fie pe deplin eficient, medicamentul trebuie luat timp de 7 zile. Dacă aveți orice întrebări suplimentare cu privire la utilizarea acestui medicament, adresați-vă medicului dumneavoastră sau farmacistului.
Supradozaj Ce trebuie făcut dacă ați luat prea mult Brivirac
Dacă luați mai multe comprimate decât trebuie, contactați medicul dumneavoastră. El va decide dacă sunt necesare măsuri suplimentare.
Efecte secundare Care sunt efectele secundare ale Brivirac
Ca toate medicamentele, acest medicament poate provoca reacții adverse, deși nu apar la toate persoanele.
Încetați să luați Brivirac și spuneți imediat medicului dumneavoastră dacă aveți o reacție alergică cu semne și simptome, inclusiv mâncărime sau piele roșie (erupție cutanată), transpirație crescută, umflare (a mâinilor, picioarelor, feței, limbii, buzelor, pleoapelor sau laringelui), dificultate în respirație (vezi și secțiunea 4) Aceste simptome pot fi severe și necesită asistență medicală urgentă.
Următoarele reacții adverse au fost observate frecvent (pot afecta până la 1 din 10 pacienți):
- greață (stare de rău).
Următoarele reacții adverse au fost observate mai puțin frecvent (pot afecta până la 1 din 100 de pacienți):
- o scădere a numărului unui tip de celule albe din sânge (granulocite)
- o creștere a numărului anumitor tipuri de celule albe din sânge (eozinofile, limfocite, monocite)
- o scădere a numărului de celule roșii din sânge (anemie)
- reacții alergice, inclusiv:
- mâncărime a pielii (mâncărime)
- roșeață a pielii (erupție eritematoasă)
- transpirație crescută
- umflarea: mâinilor, picioarelor, feței, limbii, buzelor, pleoapelor, laringelui (edem laringian)
- tuse, dificultăți de respirație și / sau dificultăți de respirație
- lipsa poftei de mâncare
- anxietate
- insomnie, somnolență
- durere de cap
- ameţeală
- ameţeală
- senzații anormale, cum ar fi arsură, amorțeală, senzație de furnicături, cel mai frecvent la nivelul brațelor și picioarelor (parestezie)
- creșterea tensiunii arteriale
- indigestie (dispepsie), vărsături, dureri de stomac
- diaree
- exces de gaz în stomac sau intestine (flatulență)
- constipație
- boală hepatică cronică cu acumulare de grăsime (ficat gras)
- creșterea nivelului sanguin al anumitor substanțe produse de ficat (creșterea enzimelor hepatice)
- slăbiciune, oboseală (oboseală)
- simptome asemănătoare gripei (stare de rău, febră, dureri și frisoane)
Următoarele reacții adverse au fost rareori observate (pot afecta până la 1 din 1000 de pacienți):
- tensiune arterială scăzută
- scăderea numărului de trombocite în sânge
- halucinații, delir
- stare confuzională
- tremur
- simțul gustului modificat
- Durere la ureche
- inflamația ficatului (hepatită), creșterea bilirubinei în sânge
- dureri osoase
Au fost raportate și următoarele reacții adverse, deși frecvența lor nu este cunoscută (frecvența nu poate fi estimată din datele disponibile):
- pierderea echilibrului
- inflamație a vaselor de sânge (vasculită)
- insuficiență hepatică cu debut rapid
- inflamație localizată a pielii care apare în același loc pentru o anumită perioadă de timp (erupție cutanată fixă), inflamație a pielii cu exfoliere (dermatită exfoliativă), erupție cutanată severă pe întreaga suprafață a corpului și în interiorul gurii datorită reacției alergice (eritem multiform) , ulcerații ale pielii, gurii, ochilor și zonelor genitale (sindromul Stevens Johnson).
Raportarea efectelor secundare
Dacă manifestați orice reacții adverse, adresați-vă medicului dumneavoastră sau farmacistului, inclusiv orice reacții adverse posibile care nu sunt enumerate în acest prospect. De asemenea, puteți raporta reacțiile adverse direct prin intermediul sistemului național de raportare la adresa: http://www.agenziafarmaco.gov.it/it/responsabili.Raportând reacțiile adverse, puteți contribui, de asemenea, la furnizarea de informații suplimentare privind siguranța acestui medicament.
Expirare și reținere
A nu se lăsa la îndemâna și vederea copiilor.
Nu utilizați acest medicament după data de expirare înscrisă pe cutie și blister. Data de expirare se referă la ultima zi a lunii respective.
Păstrați blisterul în cutie pentru a proteja medicamentul de lumină.
Nu aruncați niciun medicament prin apele uzate sau deșeurile menajere. Întrebați farmacistul cum să aruncați medicamentele pe care nu le mai utilizați. Acest lucru va ajuta la protejarea mediului.
Termen limită "> Alte informații
Ce conține Brivirac
Ingredientul activ este brivudina.
1 comprimat Brivirac conține 125 mg brivudină.
Celelalte ingrediente sunt:
- celuloză microcristalină
- lactoză monohidrat
- povidonă K 24-27
- stearat de magneziu
Cum arată Brivirac și conținutul ambalajului
Comprimatele Brivirac 125 mg sunt rotunde, plate, albe sau aproape albe, cu margini teșite.
Comprimatele sunt conținute într-un blister într-o cutie.
Brivirac este disponibil în ambalaje care conțin 1 și 7 comprimate și în ambalaje multiple, inclusiv 5 cutii, fiecare conținând 7 comprimate.
Este posibil ca nu toate mărimile de ambalaj să fie comercializate.
Prospect sursă: AIFA (Agenția italiană pentru medicamente). Conținut publicat în ianuarie 2016. Este posibil ca informațiile prezente să nu fie actualizate.
Pentru a avea acces la cea mai actualizată versiune, este recomandabil să accesați site-ul web AIFA (Agenția italiană pentru medicamente). Declinare de responsabilitate și informații utile.
01.0 DENUMIREA MEDICAMENTULUI -
BRIVIRAC 125 MG COMPRIMATE
02.0 COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ -
1 comprimat conține 125 mg de brivudină.
Excipient cu efect cunoscut: lactoză monohidrat. Fiecare comprimat conține 37 mg lactoză monohidrat.
Pentru lista completă a excipienților, vezi secțiunea 6.1
03.0 FORMA FARMACEUTICĂ -
Comprimat
Comprimate plate albe sau aproape albe, cu margini teșite.
04.0 INFORMAȚII CLINICE -
04.1 Indicații terapeutice -
Tratamentul precoce al infecțiilor cu herpes zoster acut la adulții imunocompetenți.
04.2 Doze și mod de administrare -
Dozare
Adulți: un comprimat Brivirac o dată pe zi timp de șapte zile.
Tratamentul trebuie să înceapă cât mai curând posibil, de preferință în termen de 72 de ore de la debutul primelor manifestări cutanate (de obicei o „erupție de debut”) sau 48 de ore de la debutul primului blister. Comprimatele trebuie luate aproximativ la aceeași oră în fiecare zi. Dacă simptomele persistă sau se agravează în timpul celor 7 zile de tratament, pacientul trebuie sfătuit să solicite asistență medicală. Produsul este destinat utilizării pe termen scurt.
Acest tratament reduce, de asemenea, riscul de a dezvolta nevralgie postherpetică la pacienții cu vârsta peste 50 de ani la doza normală indicată mai sus (1 comprimat de Brivirac o dată pe zi timp de 7 zile).
După un prim curs de terapie (7 zile) nu trebuie efectuat un al doilea curs.
Populații speciale
Pacienți vârstnici
Nu este necesară ajustarea dozelor la pacienții cu vârsta peste 65 de ani.
Pacienți cu insuficiență renală sau hepatică
Ca o consecință a insuficienței renale sau hepatice, nu sunt observate modificări semnificative ale expunerii sistemice la brivudină; de aceea nu este necesară ajustarea dozei la pacienții cu insuficiență renală moderată până la severă și la pacienții cu insuficiență hepatică moderată până la severă (vezi și paragraful 5.2).
Populația pediatrică
Brivirac este contraindicat la copii cu vârsta cuprinsă între 0 și 18 ani, deoarece siguranța și eficacitatea în această grupă de vârstă nu au fost stabilite (vezi pct. 4.3).
Mod de administrare
Utilizare orală.
Aportul de alimente nu afectează semnificativ absorbția brivudinei (vezi pct. 5.2).
04.3 Contraindicații -
Brivirac nu trebuie administrat în caz de hipersensibilitate la substanța activă sau la oricare dintre excipienții enumerați la pct. 6.1.
Pacienții supuși chimioterapiei antineoplazice
Utilizarea Brivirac este contraindicată la pacienții supuși chimioterapiei pentru cancer, mai ales dacă este tratat cu 5-fluorouracil (5 FU), inclusiv preparatele sale topice, pro-medicamentele sale (de exemplu, capecitabină, floxuridină, tegafur) și combinații care conțin aceste substanțe active sau alte 5-fluoropirimidine (vezi și pct. 4.4 și 4.5).
Pacienții supuși terapiei antifungice cu flucitozină
Utilizarea Brivirac este contraindicată la pacienții supuși terapiei antifungice cu flucitozină, deoarece este un medicament pro-5-fluorouracil (5 FU).
Pacienți imunocompromiși
Utilizarea Brivirac este contraindicată la pacienții imunocompromiși, cum ar fi pacienții supuși chimioterapiei antineoplazice, terapiei imunosupresoare.
Copii
Siguranța și eficacitatea Brivirac la copii nu au fost stabilite, prin urmare utilizarea sa nu este indicată.
Sarcina și alăptarea
Brivirac este contraindicat în timpul sarcinii sau alăptării (vezi și pct. 4.6).
04.4 Avertismente speciale și precauții adecvate pentru utilizare -
Brivirac și 5-fluorouracil, inclusiv preparatele sale topice sau pro-medicamentele sale (de exemplu, capecitabină, floxuridină, tegafur) sau combinații care conțin aceste substanțe active și alte 5-fluoropirimidine (de exemplu, flucitozină) nu trebuie administrate simultan și un interval minim de 4 trebuie respectate săptămâni înainte de începerea tratamentului cu medicamente cu 5-fluoropirimidină. Ca o măsură de precauție suplimentară, activitatea enzimei DPD trebuie monitorizată înainte de a începe orice tratament cu medicamente cu 5-fluoropirimidină la pacienții cărora li s-a administrat recent Brivirac (vezi și pct. 4.5 și 4.8).
Brivirac nu trebuie utilizat dacă manifestările cutanate s-au dezvoltat deja pe deplin.
Brivirac trebuie utilizat cu precauție la pacienții cu boli hepatice cronice, cum ar fi hepatita. Datele după punerea pe piață indică faptul că prelungirea tratamentului dincolo de durata recomandată de 7 zile crește riscul apariției hepatitei (vezi și pct. 4.8).
Deoarece lactoza este prezentă printre excipienți, pacienții cu probleme ereditare rare de intoleranță la galactoză, deficit de lactază Lapp sau malabsorbție la glucoză-galactoză nu trebuie să ia medicamentul.
04.5 Interacțiuni cu alte medicamente și alte forme de interacțiune -
Contraindicații pentru utilizarea concomitentă a 5-fluorouracilului (inclusiv preparatele sale topice și pro-medicamente, de exemplu capecitabină, floxuridină, tegafur) sau alte 5-fluoropirimidine, cum ar fi flucitozina (vezi și pct. 4.3).
Această interacțiune, care are ca rezultat o toxicitate crescută a fluoropirimidinei, este potențial fatală.
Brivudina, prin principalul său metabolit bromoviniluracil (BVU), exercită o „inhibiție ireversibilă a dihidroxipirimidine dehidrogenazei (DPD), o enzimă care reglează metabolismul atât a nucleozidelor naturale (de exemplu: timidina), cât și a medicamentelor pe bază de pirimidină, cum ar fi 5-fluorouracil (5). -FU): Ca o consecință a inhibării enzimei, există o supraexpunere și o toxicitate crescută a 5-FU.
Studiile clinice au arătat că la adulții sănătoși care urmează un curs de terapie pe bază de Brivirac (125 mg o dată pe zi timp de 7 zile), recuperarea funcțională completă a activității enzimei DPD are loc la 18 zile de la ultima administrare.
Brivirac și 5-fluorouracil sau alte 5-fluoropirimidine cum ar fi capecitabina, floxuridina și tegafur (sau combinații care conțin aceste substanțe active) sau flucitozina nu trebuie administrate concomitent și trebuie respectat un interval minim de 4 săptămâni înainte de începerea tratamentului medicamentos. 5-fluoropirimidină. Ca măsură de precauție suplimentară, activitatea enzimei DPD trebuie monitorizată înainte de a începe orice tratament cu medicamente cu 5-fluoropirimidină la pacienții cărora li s-a administrat recent Brivirac.
În cazul administrării accidentale de 5-FU sau medicamente conexe la pacienții tratați cu Brivirac, ambele medicamente trebuie întrerupte și trebuie puse în aplicare măsuri drastice pentru reducerea toxicității 5-FU. Se recomandă spitalizarea imediată și trebuie luate toate măsurile pentru a preveni infecțiile sistemice și deshidratarea. Semnele toxicității 5-FU includ greață, vărsături, diaree și, în cazuri severe, stomatită, mucozită, necroliză epidermică toxică, neutropenie și depresie a măduvei osoase.
Medicamente dopaminergice și / sau boala Parkinson
Experiența după punerea pe piață indică o posibilă interacțiune a brivudinei cu medicamente dopaminergice împotriva bolii Parkinson, cum ar fi precipitarea coreei.
Alte informații
Nu a fost demonstrat niciun potențial de inducție sau inhibare a sistemului enzimatic hepatic P450.
Aportul alimentar nu modifică semnificativ absorbția brivudinei.
04.6 Sarcina și alăptarea -
Brivirac este contraindicat în timpul sarcinii sau la femeile care alăptează.
Studiile la animale nu au evidențiat efecte embriotoxice sau teratogene. Efectele toxice asupra fătului au fost observate numai la doze mari. Cu toate acestea, siguranța Brivirac la femeile gravide nu a fost stabilită.
Studiile la animale au arătat că brivudina și principalul său metabolit bromoviniluracil (BVU) sunt excretate în lapte.
04.7 Efecte asupra capacității de a conduce vehicule și de a folosi utilaje -
Nu există studii cu privire la efectul Brivirac asupra capacității de a conduce vehicule sau de a folosi utilaje. 4.8).
04.8 Efecte nedorite -
Rezumatul profilului de siguranță
Brivudina a fost administrată la mai mult de 3900 de pacienți în studiile clinice. Cea mai gravă, dar rară, reacție a fost hepatita, această reacție a fost observată și în timpul supravegherii după punerea pe piață.
Singura reacție adversă comună a fost greața (2,1%). Celelalte reacții adverse cele mai frecvente (mai puțin frecvente și rare) au fost cele legate de sistemul nervos și tulburările psihiatrice SOC. .
Tulburări ale pielii și ale țesutului subcutanat au fost observate în timpul utilizării clinice a produsului, evidențiată și de datele de supraveghere post-introducere pe piață.
Incidența și tipul reacțiilor nedorite au fost comparabile cu cele despre care se știe că apar cu alți agenți antivirali nucleozidici aparținând aceleiași clase.
Tabel rezumativ al reacțiilor adverse
Tabelul de mai jos prezintă reacțiile adverse la brivudină grupate în funcție de sistem în ordinea severității scăzute.
Descrierea reacțiilor adverse selectate
Brivudina poate interacționa cu agenți chimioterapeutici din clasa 5-fluoropirimidină. Această interacțiune, care induce o toxicitate crescută a fluoropirimidinei, este potențial fatală (vezi și 4.4 și 4.5).
Semnele de toxicitate 5-FU includ greață, vărsături, diaree și, în cazuri severe, stomatită, mucozită, necroliză epidermică toxică, neutropenie și depresie a măduvei osoase (vezi și pct. 4.5).
Efectele hepatotoxice au apărut atât în studiile clinice, cât și în timpul experienței după punerea pe piață. Aceste efecte constau în hepatită colestatică sau citolitică, icter colestatic sau enzime hepatice crescute. Majoritatea cazurilor de hepatită au început la vârsta de 3 până la 28 de zile după sfârșitul celor 7 zile Datele după punerea pe piață indică faptul că prelungirea tratamentului după perioada recomandată de 7 zile crește riscul de hepatită.
Populația pediatrică
Brivudina nu a fost studiată la populația pediatrică și utilizarea sa la copii nu este indicată. Prin urmare, profilul de siguranță la populația pediatrică este necunoscut.
Raportarea reacțiilor adverse suspectate
Raportarea reacțiilor adverse suspectate care apar după autorizarea medicamentului este importantă deoarece permite monitorizarea continuă a raportului beneficiu / risc al medicamentului. Profesioniștii din domeniul sănătății sunt rugați să raporteze orice reacții adverse suspectate prin intermediul sistemului național de raportare. "Adresa www. agenziafarmaco.gov.it/it/responsabili.
04.9 Supradozaj -
Până în prezent nu s-a raportat supradozajul acut cu Brivirac. După supradozajul intenționat sau accidental, trebuie instituită o terapie simptomatică și de susținere adecvată.
05.0 PROPRIETĂȚI FARMACOLOGICE -
05.1 "Proprietăți farmacodinamice -
Antivirale
Codul ATC J05AB15
Brivudina, substanța activă din Brivirac, este unul dintre cei mai puternici analogi nucleozidici care inhibă replicarea virusului Varicella Zoster (VZV). Deosebit de sensibile sunt tulpinile clinice ale VZV. În celulele infectate cu virus, brivudina suferă o serie de fosforilări succesive care produc brivudina trifosfat, care este responsabilă de inhibarea replicării virale. Conversia intracelulară a brivudinei în derivații săi fosforilați este catalizată de enzimele codificate de virus, în principal timidin kinaza. în celulele infectate, ceea ce explică selectivitatea ridicată a brivudinei pentru țintele virale. Brivudina trifosfat, odată format în celule infectate cu virus, rămâne în interiorul celulelor mai mult de 10 ore și interacționează cu ADN polimeraza virală. Această interacțiune are ca rezultat inhibarea puternică a replicării virale. Mecanismul de rezistență se bazează pe timidina kinază virală (TK) Cu toate acestea, în practica clinică, cerințele pentru rezistență sunt tratamentul cronic antiviral și imunodeficiența pacientului, ambele fiind puțin probabil să apară cu indicațiile și pozologia indicate.
Concentrația de brivudină capabilă să inhibe replicarea virală in vitro (IC50) corespunde la 0,001 mcg / ml (interval 0,0003 - 0,003 mcg / ml). Astfel, brivudina este de aproximativ 200 până la 1000 de ori mai puternică decât aciclovirul și penciclovirul în inhibarea replicării VZV in vitro. Concentrația plasmatică maximă (Cssmax) a brivudinei persoanelor care au primit doza propusă (125 mg o dată pe zi) este de 1,7 mcg / ml (adică de 1000 de ori IC50 "in vitro") și concentrația minimă (Cssmin) este de 0,06 mcg / ml (adică de cel puțin 60 de ori IC50). Brivudina a avut un debut de acțiune foarte rapid în condiții de creștere virală ridicată, ajungând la 50 % inhibare a replicării virale în decurs de 1 oră de la expunerea la medicament. Brivudina prezintă, de asemenea, activitate antivirală la animalele experimentale infectate cu virusul Simian (maimuțe) sau virusul herpes simplex tip I (șoareci și cobai). Brivudina este activă împotriva virusului herpes simplex tip I, în timp ce nu are activitate antivirală semnificativă împotriva herpes simplex tip II .
Inhibarea replicării virusului subliniază eficacitatea Brivirac în accelerarea rezolvării manifestărilor cutanate la pacienții cu stadiul inițial al herpesului zoster. Potența antivirală înaltă in vitro a brivudinei se reflectă în eficacitatea clinică superioară observată în studiile clinice comparative cu aciclovir, în ceea ce privește perioada de timp de la începutul tratamentului până la ultima erupție veziculară: timpul mediu a fost redus cu 25% cu brivudină (13,5 ore) comparativ cu aciclovir (18 ore).
În plus, riscul relativ de a dezvolta nevralgie postherpetică (PHN) la pacienții imunocompetenți cu vârsta peste 50 de ani care au fost tratați cu herpes zoster cu brivudină a fost cu 25% mai mic (33% dintre pacienții au raportat PHN) comparativ cu aciclovir (43% dintre pacienți au raportat PHN).
05.2 "Proprietăți farmacocinetice -
Absorbţie
Brivudina se absoarbe rapid după administrarea orală de Brivirac. Biodisponibilitatea brivudinei este de aproximativ 30% din doza orală de Brivirac, datorită unui metabolism crescut la prima trecere. Concentrația plasmatică maximă de brivudină la starea de echilibru medie după administrarea unei doze orale de 125 mg de Brivirac este de 1,7 μg / ml și este atinsă la 1 oră după administrarea dozei. Aportul alimentar întârzie ușor absorbția brivudinei, dar nu afectează cantitatea totală de medicament absorbit.
Distribuție
Brivudina se distribuie extensiv în țesuturi, după cum se indică prin volumul mare de distribuție (75 L). Brivudina este puternic legată de proteinele plasmatice (> 95%).
Biotransformare
Brivudina este metabolizată extensiv și rapid de enzima pirimidin fosforilază care clivează carbohidratul pentru a da bromovinil uracil (BVU), un metabolit fără activitate virustatică. BVU este singurul metabolit detectat în plasma umană și concentrația sa maximă. Plasma este un factor de doi mai mare decât cea a compusului părinte.
BVU este metabolizat în continuare în acid uracilacetic, principalul metabolit polar detectat în urina umană, dar nu detectabil în plasmă.
Eliminare
Brivudina este eliminată eficient cu un clearance corporal total de 240 ml / min. Timpul de înjumătățire plasmatică terminal al brivudinei este de aproximativ 16 ore. Brivudina este excretată în urină (65% din doza administrată) în principal sub formă de acid uracilacetic și compuși multipli asemănători cu ureea. Brivudina nemodificată reprezintă mai puțin de 1% din doză. de Brivirac excretat în urină. Parametrii cinetici ai BVU, în ceea ce privește timpul de înjumătățire terminală și clearance-ul sunt de același ordin de mărime ca și compusul părinte.
Liniaritate / neliniaritate
Cinetica liniară a fost observată în intervalul de doze între 31,25 și 125 mg.
Condițiile de echilibru pentru brivudină sunt atinse după 5 zile de administrare zilnică de Brivirac, fără indicii de acumulare ulterioară ulterioară.
Pacienți vârstnici și pacienți cu insuficiență renală sau hepatică
Parametrii cinetici principali (ASC, Cmax și timpul de înjumătățire plasmatică terminal) ai brivudinei măsurați la pacienții vârstnici și la pacienții cu insuficiență renală moderată până la severă (clearance-ul creatininei între 26 și 50 ml / min / 1,73m² de suprafață corporală și clearance-ul creatininei
05.3 Date preclinice de siguranță -
Datele non-clinice nu au evidențiat niciun risc special pentru oameni pentru utilizarea pe termen scurt pe baza studiilor convenționale de siguranță farmacologie, genotoxicitate, potențial cancerigen, toxicitate asupra funcției de reproducere.
Efectele preclinice ale toxicității acute și cronice au fost observate în studii pe termen scurt la expuneri considerate suficient de mari decât expunerea maximă la om. tratament pe termen scurt la om. Organul țintă al toxicității la toate speciile utilizate pentru studii preclinice a fost ficatul.
06.0 INFORMAȚII FARMACEUTICE -
06.1 Excipienți -
Celuloză microcristalină, lactoză monohidrat, povidonă K 24-27, stearat de magneziu.
06.2 Incompatibilitate "-
Nu este relevant.
06.3 Perioada de valabilitate "-
3 ani.
06.4 Precauții speciale pentru depozitare -
Păstrați blisterul în cutie pentru a-l proteja de lumină.
06.5 Natura ambalajului imediat și conținutul ambalajului -
a) Natura containerului
Blister din film opac din PVC rigid și folie de aluminiu.
b) Conținutul containerului
Ambalaj original cu 7 comprimate.
Pachet de spital cu 35 (5 x 7) tablete.
Pachet de probă cu 1 comprimat.
Este posibil ca nu toate mărimile de ambalaj să fie comercializate.
06.6 Instrucțiuni de utilizare și manipulare -
Medicamentele neutilizate și deșeurile derivate din acest medicament trebuie eliminate în conformitate cu reglementările locale.
07.0 DEȚINĂTORUL „AUTORIZAȚIEI DE PUNERE PE PIAȚĂ” -
Laboratori Guidotti S.p.A. - Via Livornese 897, Pisa - La Vettola
Dealer de vânzare: A. Menarini Industrie Farmaceutiche Riunite s.r.l. - Via Sette Santi 3, Florența
08.0 NUMĂRUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ -
AIC n. 035720010 - „Comprimate de 125 mg” 7 comprimate în blister din PVC / AL
AIC n. 035720022 - „125 mg comprimate” 35 (5x7) comprimate în blister din PVC / AL
09.0 DATA PRIMEI AUTORIZAȚII SAU REÎNNOIREA AUTORIZAȚIEI -
Data primei autorizații: 06/07/2000
Data celei mai recente reînnoiri: 06/07/2015
10.0 DATA REVIZUIRII TEXTULUI -
Februarie 2016