Ingrediente active: Iod (111 In) pentetreotid
Octreoscan - Trusă de preparare radiofarmaceutică 111-pentetreotidă, 111 MBq / mL
Indicații De ce se utilizează Octreoscan? Pentru ce este?
Acest medicament este un produs radiofarmaceutic destinat numai diagnosticului.
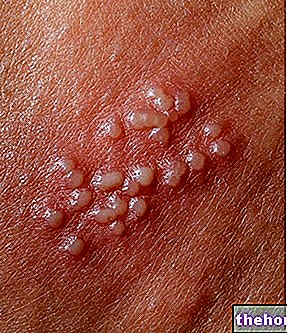
Octreoscan este utilizat prin scanare pentru a localiza celule specifice din stomac, intestine și pancreas, cum ar fi:
- țesuturi anormale sau
- tumori.
Acest medicament este o pulbere pentru soluție injectabilă și o substanță radioactivă. Aceste două componente nu trebuie utilizate separat. Odată amestecat de personal calificat și administrat organismului, medicamentul se acumulează în celule specifice.
Substanța radioactivă poate fi fotografiată din exteriorul corpului, folosind mașini speciale care pot înregistra o scanare. Această scanare arată distribuția radioactivității în corpul uman. De asemenea, furnizează medicului informații importante despre structura și funcția unei părți. specificație.
Utilizarea Octreoscan implică expunerea la cantități mici de radioactivitate. Medicul dumneavoastră sau specialistul în medicină nucleară a considerat că beneficiul clinic pe care îl veți obține din procedura radiofarmaceutică depășește riscul de radiații.
Contraindicații Când nu trebuie utilizat Octreoscan
Otreoscan nu trebuie utilizat dacă sunteți alergic (hipersensibil) la pentetreotidă sau la oricare dintre celelalte componente ale Octreoscan.
Precauții pentru utilizare Ce trebuie să știți înainte de a lua Octreoscan
Aveți grijă deosebită cu Octreoscan
- dacă aveți funcție renală redusă, medicul dumneavoastră vă va oferi Octreoscan numai dacă este absolut necesar
- dacă sunteți gravidă sau suspectați că sunteți gravidă - dacă alăptați.
Înainte de administrarea Octreoscan trebuie:
- beți cel puțin 2 litri de lichide, cum ar fi apa, și urinați cât mai mult posibil înainte și 2-3 zile după tratament. Acest lucru previne acumularea substanței active în rinichi și vezică.
- De asemenea, medicul dumneavoastră vă poate prescrie un laxativ.
Copii și adolescenți
Consultați specialistul în medicină nucleară dacă aveți sub 18 ani.
Interacțiuni Ce medicamente sau alimente pot schimba efectul Octreoscan
Vă rugăm să spuneți medicului dumneavoastră de medicină nucleară dacă luați sau ați luat recent orice alte medicamente, inclusiv cele obținute fără prescripție medicală, deoarece acestea pot interfera cu interpretarea imaginilor.
Următoarele medicamente pot afecta sau pot fi afectate de Octreoscan:
- Octreotida, un medicament pentru tratarea simptomelor unor tipuri de cancer. Este posibil ca medicul dumneavoastră să vă oprească temporar să luați octreotidă. Dacă se ia în considerare întreruperea tratamentului cu octreotidă, acest lucru trebuie făcut pe o perioadă de trei zile pentru a evita efectele nedorite.
- Insulină
Când Otreoscan este administrat pacienților care utilizează doze mari de insulină, aceștia pot prezenta scăderi severe ale glicemiei
Avertismente Este important să știm că:
Sarcina și alăptarea
Dacă sunteți gravidă, alăptați, credeți că ați putea fi gravidă sau intenționați să rămâneți gravidă, adresați-vă medicului dumneavoastră pentru medicină nucleară înainte de a vi se administra acest medicament.
Vă rugăm să informați medicul dumneavoastră de medicină nucleară înainte de a lua Octreoscan dacă este posibil să fiți gravidă, dacă ați pierdut o perioadă sau dacă alăptați. Dacă aveți dubii, este important să consultați specialistul în medicină nucleară care va supraveghea procedura.
Dacă sunteți gravidă
Medicul dumneavoastră de medicină nucleară vă va oferi Octreoscan numai dacă sunteți gravidă dacă beneficiul scontat depășește riscurile.
Dacă alăptați
Spuneți medicului dumneavoastră dacă alăptați, deoarece acesta poate decide să amâne tratamentul până când ați terminat alăptarea. De asemenea, medicul dumneavoastră vă poate cere să întrerupeți alăptarea și să aruncați laptele până când radioactivitatea va dispărea din corp. Adresați-vă medicului dumneavoastră de medicină nucleară când puteți relua alăptarea.
Consultați specialistul dumneavoastră în medicină nucleară înainte de a lua orice medicament.
Conducerea vehiculelor și utilizarea utilajelor
Este considerat puțin probabil ca Octreoscan să afecteze capacitatea de a conduce vehicule sau de a folosi utilaje.
Doze și metoda de utilizare Cum se utilizează Octreoscan: Doze
Există legi foarte stricte privind utilizarea, manipularea și eliminarea produselor radiofarmaceutice. Octreoscan va fi utilizat numai în zone speciale și controlate. Acest produs vă va fi manipulat și administrat numai de către persoane instruite și calificate să îl utilizeze în siguranță. va acorda o atenție deosebită utilizării în siguranță a acestui produs și vă va ține la curent cu acțiunile lor.
Specialistul în medicină nucleară care supraveghează procedura va decide cât de mult Octreoscan să utilizeze în cazul dumneavoastră. Aceasta va fi cantitatea minimă necesară pentru a obține informațiile dorite.
Cantitatea recomandată pentru un adult care trebuie administrat în majoritatea cazurilor variază de la
- 110-220 MBq (Mega Becquerel, unitatea utilizată pentru exprimarea radioactivității).
Utilizare la copii și adolescenți
Medicul va administra Octreoscan numai pacienților din această grupă de vârstă, dacă este absolut necesar.
Administrarea Octreoscan și gestionarea procedurii
Octreoscan este injectat într-o venă.
O injecție este suficientă pentru a efectua testul cerut de medic.
Durata procedurii
Specialistul în medicină nucleară vă va informa cu privire la durata obișnuită a procedurii.
Scanările se fac de obicei în decurs de o zi sau două de la injectare, în funcție de informațiile pe care doriți să le obțineți de la scanări.
Uneori scanările se repetă la câteva zile după examen pentru a înțelege clar rezultatele.
După administrarea Octreoscan, trebuie:
- evitați orice contact strâns cu copiii și femeile însărcinate în primele câteva ore după injecție;
- beți cel puțin 2 litri de lichide, cum ar fi apa, și urinați frecvent timp de 2-3 zile după tratament pentru a elimina produsul din corp.
- Medicul dumneavoastră vă va spune dacă trebuie să luați orice măsuri speciale de precauție după utilizarea acestui medicament. Dacă aveți întrebări, adresați-vă medicului dumneavoastră.
Supradozaj Ce trebuie făcut dacă ați luat prea mult Octreoscan
Supradozajul este puțin probabil, deoarece vi se va administra o „doză unică de Octreoscan controlată cu precizie de specialistul în medicină nucleară care supraveghează procedura. Cu toate acestea, în caz de supradozaj, veți fi tratat în mod corespunzător. „pentru a accelera eliminarea substanței radioactive. Dacă aveți întrebări cu privire la utilizarea Octreoscan, consultați specialistul în medicină nucleară care supraveghează procedura.
Efecte secundare Care sunt efectele secundare ale Octreoscan
Ca toate medicamentele, Octreoscan poate provoca reacții adverse, cu toate că nu apar la toate persoanele.
Produsul radiofarmaceutic administrat va transmite o cantitate redusă de radiații ionizante cu un risc foarte scăzut de cancer și anomalii ereditare.
Efectele secundare pot apărea cu următoarele frecvențe:
Mai puțin frecvente, apare la 1 până la 10 utilizatori din 1.000
pot apărea reacții alergice cu simptome precum:
- bufeuri
- roșeață a pielii
- mâncărime
- greață sau
- dificultăți respiratorii.
Personalul spitalului va trata aceste reacții dacă apar.
Frecvență necunoscută (frecvența nu poate fi estimată din datele disponibile)
- cancer, cu toate acestea riscul este foarte scăzut, deoarece dozele mici sunt utilizate pentru acest test.
Dacă observați orice reacție adversă, inclusiv orice reacție adversă posibilă nemenționată în acest prospect, vă rugăm să vă adresați medicului dumneavoastră de medicină nucleară.
Expirare și reținere
Nu trebuie să păstrați acest medicament. Acest medicament este păstrat sub responsabilitatea specialistului în locuri adecvate. Depozitarea radiofarmaceuticelor trebuie să respecte legislația națională pentru materialele radioactive. Aceste informații sunt destinate exclusiv specialistului.
Octreoscan nu trebuie utilizat după data de expirare înscrisă pe etichetă.
Octreoscan nu trebuie utilizat dacă se constată că integritatea cutiei de tablă a fost compromisă și / sau una dintre flacoane este deteriorată.
Alte informații
Ce conține Octreoscan
Octreoscan constă dintr-un pachet care conține două flacoane (A și B). Flaconul A conține 1,1 ml soluție, în timp ce Flaconul B conține o pulbere pentru soluție injectabilă.
Substanțele active sunt:
- Flacon A: Fiecare flacon conține 122 MBq de 111 In sub formă de clorură de indiu în 1,1 mL (111 MBq / mL) la momentul țintă de activitate.
- Flacon B: 10 micrograme de pentetreotidă.
Soluție mixtă (A plus B): 111In-Pentetreotidă 111 MBq / ml la timpul de referință al activității.
Ceilalți excipienți sunt:
- Flacon A: acid clorhidric, apă pentru preparate injectabile, clorură ferică hexahidrat.
- Flacon B: citrat de sodiu dihidrat, acid citric monohidrat, inozitol, acid gentisic.
Cum arată Octreoscan și conținutul ambalajului
Kitul Octreoscan pentru prepararea radiofarmaceutică a 111-Pentetreotidei, 122 MBq / 1,1 ml la momentul de referință al activității este furnizat într-o cutie de tablă închisă care conține două fiole și un ac Sterican Luer Lock.
Flaconul A este un flacon de sticlă protejat cu plumb, care conține o soluție limpede și incoloră.
Flaconul B este un flacon din sticlă cu dop din cauciuc butilic gri și capac din aluminiu ondulat cu închidere portocalie. Conține o pulbere albă liofilizată.
Flacoanele nu pot fi utilizate separat.
Prospect sursă: AIFA (Agenția italiană pentru medicamente). Conținut publicat în ianuarie 2016. Este posibil ca informațiile prezente să nu fie actualizate.
Pentru a avea acces la cea mai actualizată versiune, este recomandabil să accesați site-ul web AIFA (Agenția italiană pentru medicamente). Declinare de responsabilitate și informații utile.
01.0 DENUMIREA PRODUSULUI MEDICAMENTAL
OCTREOSCAN
02.0 COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ
Octreoscan este livrat în două flacoane care nu pot fi utilizate separat.
Flacon A cu 1,1 ml soluție care conține la momentul de referință al activității (ART): (111In) Indiu (III) clorură 122 MBq (111 MBq / mL)
Flaconul B conține: pentetreotidă 10 mcg
După reconstituire și etichetare, soluția conține 111In-pentetreotidă 111 MBq / mL.
Caracteristicile fizice ale 111In:
111In este un produs ciclotron și se descompune în cadmiu stabil cu un "timp de înjumătățire de 2,83 zile. Caracteristici de emisie:
Raze gamma 172 keV (90% abundență)
Raze gamma 247 keV (94% abundență) Raze X 23-26 keV
Puritate radionuclidică: 111 În ≥ 99%, alți nuclizi cu emisii de raze gamma ≤ 0,1%.
114mIn: max. 500 Bq pentru 1 MBq din 111In la data / ora de referință a activității. Timp de înjumătățire de 114mIn: 49,51 zile
Pentru lista completă a excipienților, vezi secțiunea 6.1.
03.0 FORMA FARMACEUTICĂ
Kit pentru prepararea radiofarmaceutică. Kitul este format din două flacoane:
Flacon A: Precursor radiofarmaceutic. Flacon B: Pulbere pentru soluție injectabilă.
Flaconul A este un flacon de sticlă protejat cu plumb, care conține o soluție limpede și incoloră.
Flaconul B este un flacon din sticlă cu dop de cauciuc gri și capac din aluminiu ondulat cu închidere portocalie. Conține o pulbere albă liofilizată.
04.0 INFORMAȚII CLINICE
04.1 Indicații terapeutice
Medicament destinat numai diagnosticului.
111 În pentetreotidă se leagă în mod specific de receptorii somatostatinei.
După radiomarcarea cu (111In) clorură de indiu (III), soluția obținută este indicată pentru a sprijini diagnosticul și gestionarea tumorilor gastroenteropancreatice neuroendocrine (GEP) și a tumorilor carcinoide care exprimă acești receptori, deoarece permite localizarea lor. Tumorile lipsite de receptori de somatostatină nu sunt vizualizate.
La un număr de pacienți cu GEP sau tumori carcinoide, densitatea receptorilor nu este suficientă pentru a permite vizualizarea cu Octreoscan. De obicei, la aproximativ 50% dintre pacienții cu insulinom nu este posibilă vizualizarea tumorii.
04.2 Doze și mod de administrare
Dozare
Adulți
Activitatea care trebuie administrată pentru tomografia cu emisie de fotoni unici (SPECT) depinde de echipamentul disponibil. În general, este suficientă o „activitate egală cu 110-220 MBq într-o singură” injecție intravenoasă. Trebuie administrat cu precauție pentru a evita depunerea paravazală a activității.
Populația vârstnică
Nu sunt necesare regimuri speciale de dozare pentru vârstnici.
Insuficiență renală
Pentru insuficiență renală vezi pct. 4.4.
Populația pediatrică
Decizia de a administra pentetreotidă (111In) unui copil ar trebui să fie luată de un specialist în medicină nucleară care are experiență în scintigrafia receptorilor de somatostatină, după ce a luat în considerare utilizarea unor produse radiofarmaceutice alternative cu expunere la radiații mai mică (în special PET) Pentetreotida (111In) trebuie administrată unui copil numai atunci când nu sunt disponibile medicamente radiofarmaceutice alternative sau când nu permit obținerea unui rezultat satisfăcător în evaluarea tabloului clinic al copilului.
Mod de administrare
Acest medicament trebuie reconstituit înainte de a fi administrat pacientului.
Pentru instrucțiuni privind reconstituirea medicamentului înainte de administrare, vezi pct. 12. Pentru pregătirea pacientului, vezi pct. 4.4.
Achizitie de imagini
Imaginile pot fi achiziționate la 4 și 24 de ore sau 24 și 48 de ore după injectare. Imaginile după 4 ore pot fi utile pentru compararea și evaluarea activității abdominale reprezentate în imagini după
24 de ore. Dacă activitatea din abdomen observată după 24 de ore nu poate fi interpretată cu certitudine ca absorbție în tumoră sau activitate în conținutul intestinal, scintigrafia trebuie repetată la 48 de ore. Este important să achiziționați două seturi de imagini cu cel puțin o achiziție "SPECT (sau SPECT / CT). Achiziția" imaginii "poate fi repetată la 48 de ore, 72 de ore și / sau 96 de ore după injectare, pentru a permite eliminarea radioactivității intestinale care interferează.
Absorbția fiziologică are loc în splină, ficat, rinichi și vezică.Tiroida, hipofiza și intestinele sunt vizibile la majoritatea pacienților.
04.3 Contraindicații
Hipersensibilitate la substanța activă sau la oricare dintre excipienții enumerați la pct. 6.1.
04.4 Avertismente speciale și precauții adecvate pentru utilizare
Sarcina, vezi pct. 4.6
Justificare individuală a beneficiului / riscului
Pentru fiecare pacient, expunerea la radiații ionizante trebuie să fie justificabilă pe baza posibilului beneficiu.În orice caz, activitatea administrată trebuie să fie cât mai redusă pentru a obține informațiile de diagnostic necesare.
Insuficiență renală
La pacienții cu insuficiență renală severă, administrarea de pentinreotidă 111In nu este recomandabilă, deoarece funcția absentă sau redusă a căii majore de excreție poate duce la expunerea crescută la doza de radiații. Administrarea trebuie luată în considerare numai dacă probabilitatea de a obține informații diagnostice depășește orice risc datorat la radiații. Scintigramele interpretabile pot fi obținute după hemodializă în timpul căreia activitatea de fond ridicată poate fi parțial eliminată.Înainte de dializă, imaginile nu dau indicații diagnostice din cauza activității circulante.
După dializă, s-a observat o absorbție mai mare decât de obicei la nivelul ficatului, splinei și tractului intestinal și o activitate mai mare decât de obicei în circulație.
Populația pediatrică
Datorită riscului potențial de radiații ionizante, 111-pentetreotidă nu trebuie utilizat la pacienții cu vârsta sub 18 ani, cu excepția cazului în care informațiile de diagnosticare așteptate depășesc orice risc de radiații.
Pregătirea pacientului
Pacientul trebuie să fie bine hidratat înainte de începerea examenului și îndemnat să golească cât mai des posibil în primele câteva ore după examen pentru a reduce radiațiile.
La pacienții care nu suferă de diaree este necesar să se administreze un laxativ pentru a diferenția acumulările de activitate statică, în leziunile tractului intestinal sau adiacente acestuia, de acumulările mobile ale conținutului intestinal.
111In-pentetreotid legat de non-receptor și 111In non-legat de peptid sunt eliminate rapid prin rinichi. Pentru a îmbunătăți procesul de excreție pentru a reduce zgomotul de fond și doza de radiații la rinichi și vezică, este necesar un aport mare de lichide (cel puțin 2 litri) timp de 2-3 zile după administrare.
Pentru pacienții tratați cu octreotidă, se recomandă ca această terapie să fie suspendată temporar pentru a evita o posibilă blocare a receptorilor de somatostatină. Această recomandare este dată pe bază empirică, dar necesitatea absolută a unei astfel de măsuri nu a fost demonstrată. La unii pacienți, întreruperea tratamentului nu poate fi tolerată și poate provoca efecte de revenire. Acest lucru este notoriu cazul la pacienții cu insulinom. trebuie luat în considerare riscul de hipoglicemie bruscă și al pacienților cu sindrom carcinoid.
Dacă medicul responsabil pentru managementul terapeutic al pacientului consideră că întreruperea tratamentului cu octreotide este tolerabilă, se recomandă o perioadă de întrerupere de trei zile.
Interpretarea imaginilor
Scintigrafia pozitivă 111In-pentetreotidă reflectă prezența "densității crescute a receptorilor tisulari pentru somatostatină, mai degrabă decât pentru malignitate. În plus, captarea pozitivă nu este specifică tumorilor GEP și carcinoide. O scanare pozitivă necesită evaluare. Posibilitatea ca o altă patologie să fie prezentă, caracterizată prin concentrații crescute de receptori locali pentru somatostatină. O creștere a densității receptorilor de somatostatină poate apărea și în următoarele condiții patologice: tumori cauzate de țesut derivat embriologic din creasta neuronală (paraganglioame, carcinoame tiroidiene medulare, neuroblastoame, feocromocitoame), tumori ale hipofizei, neoplasme endocrine ale plămânilor ( carcinomul cu celule mici), meningioamele, carcinoamele mamare, bolile limfoproliferative (boala Hodgkin, limfoamele non-Hodgkin) și posibilitatea absorbției în zone cu concentrație limfocitară (inflamație subacută).
După procedură
Limitați contactul strâns cu sugarii și femeile însărcinate în primele ore după administrarea radiofarmaceutice.
Avertismente specifice
La pacienții diabetici care primesc doze mari de insulină, administrarea de pentetreotide poate provoca hipoglicemie paradoxală prin „inhibarea temporară a secreției de glucagon”.
Acest medicament conține mai puțin de 1 mmol sodiu (23 mg) pe doză, adică este în esență „fără sodiu”.
Precauțiile împotriva riscului de mediu sunt raportate în secțiunea 6.6.
04.5 Interacțiuni cu alte medicamente și alte forme de interacțiune
Nu au fost descrise interacțiuni până acum.
04.6 Sarcina și alăptarea
Femeile aflate la vârsta fertilă
Atunci când este necesar să se administreze produse radiofarmaceutice unei femei în vârstă fertilă, este important să se determine dacă este gravidă. Toate femeile care au pierdut o perioadă ar trebui să fie considerate însărcinate până se dovedește contrariul. Dacă există îndoieli cu privire la o posibilă sarcină (dacă femeia a ratat un ciclu menstrual, dacă ciclul menstrual este foarte neregulat etc.), ar trebui oferite pacientului tehnici alternative care nu utilizează radiații ionizante (dacă sunt disponibile).
Sarcina
Nu există experiență cu privire la utilizarea Octreoscan la femeile gravide.
Procedurile de radionuclizi supuse femeilor însărcinate expun, de asemenea, fătul la o doză de radiații. Administrarea activității diagnostice maxime de 220 MBq pacientului are ca rezultat o doză absorbită din uter de 8,6 mGy. La acest interval de dozare, efectele letale și inducerea malformațiilor, întârzierilor de creștere și tulburărilor funcționale nu sunt previzibile; cu toate acestea, riscul de inducere a cancerului și a defectelor ereditare poate crește. Prin urmare, în timpul sarcinii, trebuie efectuate numai teste esențiale atunci când posibilul beneficiu depășește riscul pentru mamă și făt.
Timp de hrănire
Nu se știe dacă 111-pentetreotidă este excretată în laptele uman. Înainte de administrarea radiofarmaceuticelor la o mamă care alăptează, trebuie avută în vedere amânarea administrării de radionuclizi până la „încetarea alăptării” și determinarea carei radiofarmaceutice este cea mai potrivită, ținând seama de secreția de activitate din laptele matern. Dacă administrarea este considerată necesară, alăptarea trebuie întreruptă și laptele produs trebuie aruncat.
04.7 Efecte asupra capacității de a conduce vehicule și de a folosi utilaje
Octreoscan nu are efecte sau are efecte neglijabile asupra capacității de a conduce vehicule și de a folosi utilaje.
04.8 Efecte nedorite
Efectele nedorite atribuite administrării Octreoscan sunt mai puțin frecvente (≥1 / 1000 la simptomele raportate se referă la reacții vasovagale sau de tip anafilactoid la medicamente.
Întreruperea terapiei cu octreotide ca preparat pentru scintigrafie poate avea ca rezultat efecte adverse severe, în general de natura recidivei simptomelor observate înainte de inițierea acestei terapii.
Expunerea la radiații ionizante este legată de inducerea cancerului și potențialul de defecte ereditare. Deoarece doza eficientă este de 12 mSv, când se administrează activitatea maximă recomandată de 220 MBq, există o probabilitate redusă de apariție a acestor evenimente adverse.
04.9 Supradozaj
Forma farmaceutică (injecție cu doză unică) face puțin probabilă supradozajul accidental.
În cazul administrării unei supradoze de radiații cu 111-pentetreotidă, doza absorbită la pacient trebuie redusă, ori de câte ori este posibil, prin creșterea eliminării radionuclizilor din organism prin urinare frecventă sau diureză forțată și golirea frecventă a vezicii urinare.
05.0 PROPRIETĂȚI FARMACOLOGICE
05.1 Proprietăți farmacodinamice
Grupa farmacoterapeutică: radiofarmaceutice de diagnostic pentru depistarea tumorilor. Codul ATC: V09I B 01.
Mecanism de acțiune
Octreoscanul se leagă de receptorii somatostatinei (în principal subtipul 2 și subtipul 5) din țesuturile în care, ca urmare a bolii, suprafețele celulare conțin acești receptori într-o densitate mai fiziologică. La pacienții individuali, la care boala nu a condus la o creștere a densității receptorilor, scintigrafia nu va fi eficientă.
În carcinoizi și tumorile GEP, prevalența creșterii densității receptorilor în țesutul tumoral este în general destul de ridicată.
Efecte farmacodinamice
Au fost efectuate doar studii limitate privind efectele farmacodinamice. Activitatea biologică in vitro reprezintă aproximativ 30% din activitatea biologică a somatostatinei naturale. Activitatea biologică in vivo, măsurată la șobolani, este mai mică decât cea a unor cantități echivalente de ocreotidă. La unii pacienți, administrarea intravenoasă de 20 mcg de pentetreotidă a dus la o scădere măsurabilă, dar foarte limitată, a nivelului seric de gastrină și glucagon în sânge. cu o durată mai mică de 24 de ore.
05.2 Proprietăți farmacocinetice
Absorbția de către organe
111 In-pentetreotida este absorbită de următoarele organe: ficat (aproximativ 2% după 24 de ore) și splină (aproximativ 2,5% după 24 de ore). Absorbția în tiroidă și hipofiză este prezentă, dar nu reproductibilă. Absorbția în rinichi este parțial o reflectare a eliminării continue prin urină și parțial din cauza excreției întârziate de rinichi.
Eliminare
111In-pentetreotid legat de non-receptor și 111In non-legat de peptid sunt eliminate rapid prin rinichi. În termen de 24 de ore de la administrarea intravenoasă, aproximativ 80% din pentetreotida radiomarcată este excretată prin tractul urinar. După 48 de ore, 90% este excretată. Eliminarea prin vezica biliară și ulterior fecalele reprezintă aproximativ 2% din activitatea administrată la pacienții cu intestin normal funcţie.
111 In-pentetreotida este predominant intactă în urină timp de până la 6 ore de radioactivitate după administrare. Ulterior, sunt excretate cantități crescânde de activitate non-peptidică legată.
Jumătate de viață
111 În decaderi până la cadmiu stabil cu un "timp de înjumătățire de 2,83 zile.
05.3 Date preclinice de siguranță
Testele preclinice de siguranță nu au furnizat rezultate demne de remarcat. Nu s-au efectuat teste asupra potențialului cancerigen și nici asupra influenței pentetreotidei asupra fertilității sau embriotoxicității.
06.0 INFORMAȚII FARMACEUTICE
06.1 Excipienți
Flaconul A
Acid clorhidric
Apă pentru preparate injectabile
Hexhidrat de clorură ferică
Flaconul B
Citrat de sodiu dihidrat
Acid citric monohidrat
Inozitol
Acid gentisic.
Soluția gata de utilizare nu conține conservanți.
06.2 Incompatibilitate
Acest medicament nu trebuie amestecat cu alte medicamente, cu excepția celor menționate la punctul 12.
06.3 Perioada de valabilitate
Flaconul A și, în consecință, Flaconul B al lui Octreoscan expiră la 24 de ore după data / ora de referință a activității 111In.
După reconstituire: 6 ore. A se păstra la temperaturi sub 25 ° C
06.4 Precauții speciale pentru depozitare
A se păstra la temperaturi sub 25 ° C.
Pentru condițiile de păstrare a medicamentului reconstituit, vezi pct. 6.3.
Depozitarea radiofarmaceuticelor trebuie să respecte legislația națională pentru materialele radioactive.
06.5 Natura ambalajului imediat și conținutul ambalajului
Ambele flacoane de 10 ml îndeplinesc cerințele pentru sticla de tip I. Flaconul care conține pentetreotidă este închis cu un dop din cauciuc butilic. Flaconul care conține clorură de indiu 111In este închis cu un dop din cauciuc butilic acoperit cu teflon. Ambele flacoane sunt sigilate cu un capac din aluminiu.
Octreoscan este furnizat ca un singur pachet conținând două flacoane care nu pot fi utilizate separat, dintre care unul are un ecran de plumb. Ambele flacoane sunt ambalate într-o cutie de tablă închisă sigilată. Acesta conține, de asemenea, un ac Steruer Luer Lock de 0,90 x 70mm / 20G x 2 4/5 pentru a fi utilizat pentru procedura de marcare.
06.6 Instrucțiuni de utilizare și manipulare
Produsele radiofarmaceutice trebuie primite, utilizate și administrate numai de către persoane autorizate în medii clinice desemnate. Primirea, depozitarea, utilizarea, transferul și eliminarea acestora sunt supuse reglementărilor și / sau autorizațiilor corespunzătoare ale organizației oficiale locale competente.
Produsele radiofarmaceutice trebuie preparate într-un mod care să satisfacă atât cerințele de siguranță radiologică, cât și cerințele de calitate farmaceutică. Trebuie luate măsuri aseptice adecvate.
Conținutul ambelor flacoane este destinat utilizării numai la prepararea soluției injectabile 111In-Pentetreotide și nu trebuie administrat pacientului direct fără a fi supus mai întâi procedura de preparare.
Dacă, în orice moment al preparării acestui produs, integritatea flacoanelor este compromisă, acestea nu trebuie utilizate.
Procedurile de administrare trebuie efectuate într-un mod care să minimizeze riscul de contaminare a medicamentului și de iradiere a operatorilor. Este obligatoriu să folosiți un ecran adecvat.
Administrarea de produse radiofarmaceutice creează riscuri pentru alte persoane din cauza radiațiilor externe sau a contaminării cauzate de vărsarea de urină, vărsături etc. În consecință, trebuie luate măsuri de protecție împotriva radiațiilor în conformitate cu reglementările naționale.
Instrucțiuni pentru eliminarea deșeurilor:
Cantitățile neutilizate de 111In sau Octreoscan trebuie lăsate să se descompună până când activitatea scade la un nivel inferior care nu mai este considerat radioactiv în conformitate cu reglementările locale. Apoi va fi posibil să se elimine ca deșeuri inofensive. Flacoanele neutilizate care conțin pentetreotidă liofilizată pot fi eliminate eliminat ca deșeuri inofensive.
Produsul neutilizat sau deșeurile trebuie eliminate în conformitate cu cerințele locale.
07.0 DEȚINĂTORUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
Mallinckrodt Medical B.V., Westerduinweg 3
1755 LE Petten, Olanda
08.0 NUMĂRUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
AIC n. 029852011
09.0 DATA PRIMEI AUTORIZAȚII SAU REÎNNOIREA AUTORIZAȚIEI
27.02.1997 / 17.03.2010
10.0 DATA REVIZUIRII TEXTULUI
06/2013
11.0 PENTRU DROGURILE RADIO, DATE COMPLETE PRIVIND DOSIMETRIA INTERNĂ DE RADIARE
111In este un produs ciclotron și se descompune cu emisia de radiații gamma la o energie ca cea prezentată în tabelul următor și cu un timp de înjumătățire de 2,83 zile la cadmiu-111 (stabil).
Următoarea dozimetrie a radiației este calculată pe baza sistemului MIRD. Datele enumerate mai jos sunt prezente în publicația nr. 106 din ICRP din 2008 și au fost calculate pe baza următoarelor ipoteze.
Conform modelului biokinetic descris în publicația nr. 106 din ICRP, se presupune că 111-pentreotid injectat intravenos este imediat absorbit de ficat, splină, rinichi și tiroidă, în timp ce restul se presupune că este distribuit omogen în restul organismului. Datele de păstrare detectate la nivel experimental sunt mai bine descrise de funcțiile mono- sau bi-exponențiale. Datele biokinetice provin de la pacienții cu tumori carcinoide și tumori endocrine din tractul gastro-intestinal.
Prin urmare, absorbția în țesutul tumoral prezent în orice organ poate fi inclusă în valorile de absorbție a organelor publicate. Calea principală de excreție este renală și mai puțin de 2% este excretată în fecale. 85% excreție este observată în urină. Excreția minimă prin tractul gastro-intestinal nu este inclusă în model, deoarece contribuția sa la doza absorbită în circumstanțe normale este neglijabilă.
Doza eficientă rezultată din administrarea unei activități (maxim recomandată) de 220 MBq pentru un adult de 70 kg este de aproximativ 12 mSv.
111 În pentetreotid se leagă în mod specific de receptorii somatostatinei, deci nu este posibil să se definească un organ țintă. Pentru o activitate administrată de 220 MBq, doza de radiație pentru organele țintă (rinichi, ficat și splină) este de 90, 22 și respectiv 125 mGy.
12.0 PENTRU DROGURI RADIO, INSTRUCȚIUNI SUPLIMENTARE DETALIATE PRIVIND PREPARAREA EXEMPORARĂ ȘI CONTROLUL CALITĂȚII
Nu utilizați Octreoscan dacă există semne evidente de deteriorare.
Mod de preparare:
Instrucțiuni pentru marcare
1. Adăugați conținutul flaconului A (clorură 111In) în flaconul B (pentetreotidă liofilizată) pentru a obține produsul pentetreotid Indiu (111In); pentru a extrage clorura de indiu din flaconul său, utilizați doar acul Sterican (0,90 x 70) furnizat împreună cu doza trimisă pacientului.
2. Respectați o perioadă de incubație de 30 de minute după reconstituire.
3. Preparatul poate fi diluat cu 2-3 ml soluție de clorură de sodiu 0,9% dacă se dorește un volum mai mare pentru a facilita manipularea în seringă.
4. Soluția preparată trebuie să fie limpede și incoloră; această stare poate fi verificată în spatele unui perete de plumb cu fereastră de sticlă cu plumb. Dacă soluția nu este conformă, aruncați-o.
5. Folosiți un eșantion mic din acest volum (diluat sau nediluat) pentru controlul calității descris în secțiunea următoare.
6. Soluția este acum gata de utilizare. Soluția trebuie utilizată în decurs de 6 ore.
Notă: Pentru reconstituire, nu utilizați nicio altă soluție de clorură 111In decât cea furnizată în același recipient cu pentetreotidă liofilizată.
După reconstituire și etichetare, pH-ul soluției apoase este de 3,8-4,3.
Control de calitate:
Discriminarea dintre peptidele marcate cu 111In și compușii non-peptidici marcate cu 111In poate fi efectuată cu benzi de fibre de sticlă impregnate cu silicagel. Pregătiți o bandă bine uscată de aproximativ 10 cm lungime și 2,5 cm lățime, marcând o linie de plecare la 2 cm cu semne suplimentare la 6 și 9 cm. Se aplică 5-10 mcl soluție reconstituită și marcată pe linia inițială și se dezvoltă în 0,1 M soluție de citrat de sodiu proaspăt preparată, adusă la pH 5 cu HCI. În aproximativ 2-3 minute, partea din față va atinge marca de 9 cm. Tăiați banda la semnul de 6 cm și măsurați activitatea ambelor jumătăți. Non-peptida legată 111In se mișcă cu fața. Cerință: Capătul inferior al cromatogramei trebuie să conțină ≥ 98% din activitatea aplicată Cromatograma trebuie să conțină ≥ 98% din activitatea aplicată.