Ingrediente active: oxcarbazepină
TOLEP 300 mg comprimate
TOLEP 600 mg comprimate
Indicații De ce se folosește Tolep? Pentru ce este?
Grupa farmacoterapeutică
Antiepileptic, derivat al carboxamidei.
Indicații terapeutice
Tolep este indicat pentru tratamentul convulsiilor parțiale cu sau fără convulsii tonice clonice secundare generalizate.
Tolep este indicat pentru utilizare atât în monoterapie, cât și în terapia adjuvantă la adulți și copii cu vârsta de 6 ani și peste.
Contraindicații Când nu trebuie utilizat Tolep
Hipersensibilitate la substanța activă sau la oricare dintre excipienți.
Precauții pentru utilizare Ce trebuie să știți înainte de a lua Tolep
Tolep trebuie administrat numai sub supraveghere medicală.
Hipersensibilitate
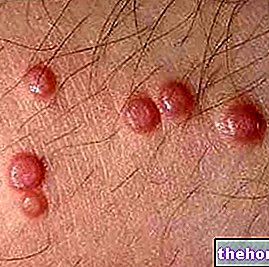
În perioada de după punerea pe piață, au fost raportate reacții de hipersensibilitate (imediată) de clasa I, inclusiv erupții cutanate, prurit, urticarie, angioedem și cazuri de anafilaxie. Au fost raportate cazuri de anafilaxie și angioedem care afectează laringele, glota, buzele și pleoapele după administrarea primei doze sau a dozelor ulterioare de Tolep. Dacă aceste reacții apar la un pacient după tratamentul cu Tolep, acestea trebuie să întrerupă administrarea Tolep și terapia alternativă ar trebui să fie iniţiat.
Pacienții care au prezentat reacții de hipersensibilitate la carbamazepină trebuie informați că aproximativ 25-30% din aceiași pacienți pot reapărea reacții similare (de exemplu reacții cutanate severe) după administrarea Tolep (vezi „Efecte nedorite”).
Reacțiile de hipersensibilitate, inclusiv reacțiile de hipersensibilitate cu mai multe organe, pot apărea și la pacienții care nu au avut episoade anterioare de hipersensibilitate la carbamazepină. Aceste reacții pot afecta pielea, ficatul, sângele și sistemul limfatic sau alte organe, fie individual, fie simultan în cazul unei reacții sistemice (vezi „Efecte nedorite”). În general, dacă apar semne și simptome care sugerează reacții de hipersensibilitate, administrarea Tolep trebuie oprită imediat.
Efecte dermatologice
În cazuri foarte rare, au fost raportate reacții dermatologice severe, inclusiv sindromul Stevens-Johnson, necroliza epidermică toxică (sindromul Lyell) și eritemul multiform, în asociere cu utilizarea Tolep. Pacienții cu reacții dermatologice severe pot avea nevoie de spitalizare, deoarece aceste afecțiuni pot pune viața în pericol și foarte rar letale. Timpul mediu de debut a fost de 19 zile. Au fost raportate mai multe cazuri izolate de reapariție a reacțiilor cutanate severe la reluarea tratamentului cu Tolep. Pacienții tratați cu Tolep care dezvoltă o reacție cutanată trebuie evaluați imediat și tratamentul cu Tolep trebuie oprit imediat, cu excepția cazului în care erupția cutanată nu este în mod clar legată de medicament. Dacă tratamentul este întrerupt, trebuie luată în considerare înlocuirea Tolep cu un alt medicament antiepileptic pentru a evita atacurile de sevraj. Tolep nu trebuie re-administrat la pacienții care au întrerupt tratamentul din cauza reacțiilor de hipersensibilitate (vezi „Contraindicații”).
Riscul de reacții cutanate severe la pacienții han-chinezi sau thailandezi asociați cu carbamazepină sau substanțe înrudite chimic poate fi prezis prin testarea unei probe de sânge de la acești pacienți. Medicul dumneavoastră ar trebui să fie în măsură să vă sfătuiască dacă sunt necesare teste de sânge înainte de a lua oxcarbazepină.
Riscul de agravare a convulsiilor
Riscul agravării convulsiilor a fost raportat în timpul tratamentului cu oxcarbazepină. Riscul agravării convulsiilor a fost observat în principal la copii, dar poate apărea și la adulți. În cazul agravării convulsiilor, tratamentul cu Tolep trebuie întrerupt.
Hiponatremie
La pacienții cu disfuncție renală preexistentă asociată cu niveluri scăzute de sodiu (de exemplu, sindromul secreției inadecvate de ADH) sau la pacienții tratați concomitent cu medicamente care scad nivelurile de sodiu (de exemplu, diuretice, desmopresină, molecule asociate cu secreție inadecvată de ADH) ca și cu cele nesteroidiene medicamente antiinflamatoare (de exemplu, indometacin), nivelurile de sodiu din sânge trebuie măsurate înainte de începerea terapiei, după aproximativ două săptămâni și după aceea la intervale lunare în primele trei luni de tratament sau după cum a apreciat medicul. Acești factori de risc pot afecta în principal pacienții vârstnici. Pacienții deja tratați cu Tolep care încep tratamentul cu medicamente care scad nivelul de sodiu ar trebui să fie supuși acelorași verificări ale nivelului de sodiu din sânge. În general, dacă simptome care sugerează hiponatremie (niveluri prea scăzute de sodiu în sânge; vezi „Efecte secundare”) apar în timpul tratamentului cu Tolep, medicul dumneavoastră poate decide să efectueze măsurători de sodiu în sânge. Pentru alți pacienți, aceste teste pot face parte din controalele normale de laborator.
Toți pacienții cu insuficiență cardiacă și insuficiență cardiacă secundară ar trebui să fie verificați greutatea în mod regulat pentru a se asigura că retenția de lichide nu are loc. În caz de retenție de lichide sau agravarea afecțiunilor cardiace, trebuie verificate nivelurile de sodiu din sânge. Dacă se observă hiponatremie, poate fi util să reduceți fluidele luate. Pacienții cu tulburări de conducere preexistente (de exemplu blocul atrioventricular, aritmia) trebuie monitorizați îndeaproape.
Hipotiroidism
Hipotiroidismul este o reacție adversă foarte rară la oxcarbazepină. Având în vedere importanța hormonilor tiroidieni în dezvoltarea copiilor după naștere, se recomandă verificarea funcției tiroidiene înainte de inițierea tratamentului cu Tolep la copii și adolescenți. La copii și adolescenți, se recomandă monitorizarea funcției tiroidiene în timpul tratamentului cu Tolep.
Funcția hepatică
Au fost raportate episoade foarte rare de hepatită, care s-au rezolvat favorabil în majoritatea cazurilor. Când se suspectează un efect hepatic, funcția hepatică trebuie monitorizată și trebuie luată în considerare întreruperea tratamentului cu Tolep. Se recomandă prudență la administrarea Tolep la pacienții cu insuficiență hepatică severă (vezi „Doza, metoda și momentul administrării”).
Functie renala
La pacienții cu insuficiență renală (clearance-ul creatininei mai mic de 30 ml / min) trebuie administrată precauție în timpul tratamentului cu Tolep, în special în ceea ce privește doza inițială și titrarea dozei (vezi „Doza, metoda și timpul de administrare”).
Efecte hematologice
După punerea pe piață au fost raportate cazuri foarte rare de agranulocitoză, anemie aplastică și pancitopenie la pacienții tratați cu Tolep (vezi „Efecte nedorite”). Întreruperea tratamentului trebuie luată în considerare dacă apar semne de depresie semnificativă a măduvei osoase.
Contraceptive hormonale
Pacienții cu vârsta fertilă trebuie informați că utilizarea concomitentă a Tolep și contraceptivele hormonale poate anula efectul acestora (vezi „Interacțiuni”). Se recomandă utilizarea în timpul terapiei cu Tolep a unor metode contraceptive non-hormonale alternative.
Alcool
Este necesară o prudență extremă în cazul în care se consumă băuturi alcoolice în timpul tratamentului cu Tolep datorită posibilului efect sedativ aditiv.
Ideea și comportamentul sinucigaș
Un număr mic de pacienți tratați cu medicamente antiepileptice, cum ar fi Tolep, au dezvoltat gânduri de auto-vătămare sau sinucidere. Oricând apar astfel de gânduri, contactați imediat medicul dumneavoastră.
Întreruperea tratamentului
Ca și în cazul altor medicamente antiepileptice, tratamentul cu Tolep trebuie întrerupt treptat pentru a minimiza riscul creșterii frecvenței convulsiilor.
Interacțiuni Ce medicamente sau alimente pot modifica efectul Tolep
Spuneți medicului dumneavoastră sau farmacistului dacă luați sau ați luat recent orice alte medicamente, chiar și cele fără prescripție medicală.
Interacțiuni potențiale au fost observate între Tolep și alte medicamente antiepileptice, cum ar fi carbamazepina, fenobarbitalul, fenitoina, acidul valproic și lamotrigina. Atunci când unul sau mai multe medicamente antiepileptice sunt administrate concomitent cu oxcarbazepină, poate fi necesară ajustarea prudentă a dozei și / sau monitorizarea concentrațiilor plasmatice, în special la copii și adolescenți tratați concomitent cu lamotrigină. Terapia concomitentă cu Tolep și lamotrigină a fost asociată cu un risc crescut de evenimente adverse (greață, somnolență, amețeli și cefalee).
S-a demonstrat că Tolep afectează cele două componente ale unui contraceptiv oral, etinilestradiolul și levonorgestrelul. Prin urmare, utilizarea concomitentă a Tolep și contraceptivele hormonale poate face ca acesta din urmă să fie ineficient (a se vedea „Precauții de utilizare”). Alte metode de contracepție, altele decât cele hormonale , trebuie luat în considerare.
Sunt posibile interacțiuni între Tolep și imunosupresoare (de exemplu, ciclosporină, tacrolimus).
O interacțiune între oxcarbazepină și inhibitori MAO este teoretic posibilă, bazată pe o relație structurală între oxcarbazepină și antidepresive triciclice. Pacienții cu antidepresive triciclice au fost incluși în studiile clinice și nu au fost observate interacțiuni semnificative clinic. Administrarea oxcarbazepinei și litiu poate provoca neurotoxicitate crescută.
La întreruperea tratamentului cu Tolep, poate fi necesară reducerea dozei de medicamente concomitente după o evaluare clinică adecvată și / sau o monitorizare a nivelului plasmatic.
S-a demonstrat că Tolep nu interferează cu warfarina, viloxazina, cimetidina, eritromicina și dextropropoxifenul.
Avertismente Este important să știm că:
Sarcina
Adresați-vă medicului dumneavoastră sau farmacistului pentru recomandări înainte de a lua orice medicament. Riscuri asociate cu epilepsia și medicamentele antiepileptice în general Pacientelor care pot rămâne însărcinate sau care au vârsta fertilă trebuie să li se ofere sfaturi de specialitate.
Necesitatea tratamentului antiepileptic trebuie reevaluată atunci când pacientul intenționează să rămână gravidă.
S-a demonstrat că incidența malformațiilor este de două până la trei ori mai mare la cei născuți de femei cu epilepsie decât la o frecvență de aproximativ 3% în populația generală.
Se știe că cei născuți de femei epileptice sunt mai predispuși la tulburări de dezvoltare, inclusiv malformații. Datele dintr-un număr limitat de sarcini indică faptul că oxcarbazepina poate provoca malformații congenitale grave atunci când este administrată în timpul sarcinii.
O creștere a malformațiilor cu politerapie a fost observată la populația tratată, totuși nu s-a clarificat în ce măsură tratamentul este responsabil pentru boală. Mai mult, terapia antiepileptică eficientă nu trebuie întreruptă, deoarece agravarea bolii este dăunătoare atât mamei, cât și fătului.
Luând în considerare toate acestea:
- Dacă pacientele care iau Tolep rămân însărcinate sau intenționează să rămână însărcinate sau dacă trebuie să înceapă tratamentul cu Tolep în timpul sarcinii, beneficiile potențiale ale medicamentului trebuie evaluate cu atenție cu riscul potențial de malformații fetale. Acest lucru este deosebit de important în primele trei luni de sarcină.
- Trebuie administrate cele mai mici doze eficiente.
- La femeile cu vârsta fertilă, Tolep trebuie administrat în monoterapie ori de câte ori este posibil.
- Pacienții trebuie informați că riscul apariției malformațiilor poate crește și trebuie să poată fi supus unui screening prenatal.
- În timpul sarcinii, terapia antiepileptică eficientă cu oxcarbazepină nu trebuie întreruptă, deoarece agravarea bolii este dăunătoare atât mamei, cât și fătului.
Monitorizare și prevenire
Medicamentele antiepileptice pot contribui la deficitul de acid folic, unul dintre posibilii factori responsabili pentru anomaliile fetale. Se recomandă administrarea suplimentară de acid folic înainte și în timpul sarcinii. Deoarece eficacitatea acestei administrări suplimentare nu este dovedită, oportunitatea unui diagnostic prenatal specific poate fi luată în considerare și la femeile în tratament suplimentar cu acid folic.
Datorită modificărilor fiziologice care apar, nivelurile plasmatice ale metabolitului activ al oxcarbazepinei (derivatul monohidroxilat, MHD) pot scădea treptat în timpul sarcinii. Prin urmare, la femeile care urmează tratament cu Tolep în timpul sarcinii, se recomandă monitorizarea atentă a răspunsului clinic și monitorizarea concentrațiilor plasmatice ale MHD pentru a asigura un control adecvat al convulsiilor în timpul sarcinii. Monitorizarea concentrațiilor plasmatice de MHD poate fi luată în considerare și după naștere, mai ales dacă dozele de medicament au fost crescute în timpul sarcinii.
La nou-născut
La nou-născuți au fost raportate tulburări de sângerare cauzate de medicamente antiepileptice. Ca măsură de precauție, vitamina K1 trebuie administrată în scop preventiv în ultimele săptămâni de sarcină și ulterior nou-născuților.
Timp de hrănire
Oxcarbazepina și metabolitul său activ (MHD) sunt excretați în laptele matern. Efectele asupra sugarilor expuși la Tolep în acest mod sunt necunoscute. Prin urmare, Tolep nu trebuie administrat în timpul alăptării.
Femeile aflate la vârsta fertilă și măsurile contraceptive
Femeile aflate la vârsta fertilă trebuie informate cu privire la necesitatea utilizării unor metode contraceptive extrem de eficiente (de preferință non-hormonale, cum ar fi implanturile intrauterine) în timpul tratamentului cu Tolep. Utilizarea Tolep poate anula efectul terapeutic al contraceptivelor orale pe bază de etinilestradiol și levonorgestrel (vezi „Interacțiuni” și „Precauții de utilizare”).
Fertilitate
Nu există date despre om referitoare la fertilitate.
Efecte asupra capacității de a conduce vehicule și de a folosi utilaje
Au fost raportate reacții adverse, cum ar fi amețeli, somnolență, ataxie, diplopie, vedere încețoșată, tulburări vizuale, hiponatremie, tulburări de conștiință cu utilizarea oxcarbazepinei (pentru lista completă a reacțiilor adverse, vezi „Efecte nedorite”), în special la început de tratament sau când se fac ajustări ale dozei (mai frecvent în timpul fazei de titrare) .Pacienții trebuie, prin urmare, să fie atenți cuvenit atunci când conduc vehicule și folosesc utilaje.
Doze și metoda de utilizare Cum se utilizează Tolep: Doze
Ca monoterapie și ca terapie adjuvantă, tratamentul cu Tolep trebuie inițiat prin administrarea unei doze eficiente clinic, împărțită în două administrări. Doza poate fi crescută în funcție de răspunsul clinic al pacientului. Când Tolep este utilizat pentru a înlocui alte medicamente antiepileptice, doza de medicamente antiepileptice combinate trebuie redusă treptat la inițierea tratamentului cu Tolep. În terapia suplimentară, deoarece sarcina totală a medicamentelor antiepileptice asupra pacientului este crescută, poate fi necesară reducerea dozei celorlalte combinații antiepileptice și / sau creșterea dozei de Tolep mai lent (vezi secțiunea „Precauții pentru utilizare").
Adulți
Monoterapie
Doza inițială recomandată
Tratamentul cu Tolep trebuie să înceapă cu o doză de 600 mg / zi (8-10 mg / kg / zi) împărțită în două doze.
Doza de întreținere
Dacă este indicată clinic, doza poate fi crescută în trepte maxime de 600 mg / zi la intervale aproximativ săptămânale de la doza inițială până la obținerea răspunsului clinic dorit. Efectele terapeutice sunt observate la doze cuprinse între 600 mg / zi și 2400 mg / zi.
Doza maximă recomandată
Într-un spital controlat, creșterea dozei de până la 2400 mg / zi s-a făcut pe parcursul a 48 de ore.
Terapia adjuvantă
Doza inițială recomandată
Tratamentul cu Tolep trebuie să înceapă cu o doză de 600 mg / zi (8-10 mg / kg / zi) împărțită în două doze.
Doza de întreținere
Dacă este indicată clinic, doza poate fi crescută în trepte maxime de 600 mg / zi la intervale aproximativ săptămânale începând cu doza inițială până când se obține răspunsul clinic dorit. Efectele terapeutice sunt observate la doze cuprinse între 600 mg / zi și 2400 mg / zi.
Doza maximă recomandată
Dozele zilnice cuprinse între 600 și 2400 mg / zi au fost eficiente, deși majoritatea pacienților nu au putut tolera doza de 2400 mg / zi fără a reduce concomitent alte medicamente antiepileptice, în principal datorită apariției evenimentelor adverse asociate cu medicamentul. Sistem nervos. Dozele zilnice peste 2400 mg / zi nu au fost evaluate sistematic în studiile clinice.
Pacienți vârstnici (65 de ani sau peste)
Nu sunt necesare recomandări speciale de dozare la pacienții vârstnici, deoarece dozele terapeutice sunt ajustate individual. Se recomandă ajustări ale dozelor la pacienții vârstnici cu insuficiență renală (clearance-ul creatininei mai mic de 30 ml / min) (vezi secțiunea „Pacienți cu insuficiență renală”). Se recomandă o monitorizare atentă a concentrațiilor de sodiu la pacienții cu risc de hiponatremie (vezi „Precauții de utilizare”).
Pacienți cu insuficiență hepatică
Nu este necesară ajustarea dozelor la pacienții cu insuficiență hepatică ușoară până la moderată. Tolep nu a fost studiat la pacienții cu insuficiență hepatică severă, prin urmare se recomandă prudență la administrarea Tolep acestor pacienți.
Pacienți cu insuficiență renală
La pacienții cu insuficiență renală (clearance-ul creatininei mai mic de 30 ml / min), tratamentul cu Tolep trebuie început cu jumătate din doza inițială obișnuită (300 mg / zi) și crescut la intervale cel puțin săptămânale până la obținerea răspunsului clinic dorit (vezi „Precauții pentru Creșterea dozei la pacienții cu insuficiență renală poate necesita o observare mai atentă.
Copii
Doza inițială recomandată
Ca monoterapie și ca terapie adjuvantă, tratamentul cu Tolep trebuie să înceapă cu o doză de 8-10 mg / kg / zi, împărțită în două administrări.
Doza de întreținere
O doză de întreținere de 30-46 mg / kg / zi, atinsă în decurs de două săptămâni, s-a dovedit a fi eficientă și bine tolerată la copii. Efectele terapeutice au fost observate la o doză medie de întreținere de aproximativ 30 mg / kg / zi.
Doza maximă recomandată
Dacă este indicată clinic, doza poate fi crescută în trepte maxime de 10 mg / kg / zi la intervale aproximativ săptămânale începând de la doza inițială până la doza maximă de 46 mg / kg / zi pentru a obține răspunsul clinic dorit.
Tolep este indicat pentru utilizare la copii cu vârsta de 6 ani și peste. Tolep nu este recomandat la copii cu vârsta sub 6 ani, deoarece siguranța și eficacitatea nu au fost demonstrate în mod adecvat.
Toate recomandările descrise mai sus (adulți, vârstnici și copii) se referă la dozele studiate în studiile clinice la toate grupele de vârstă. Cu toate acestea, se poate decide, dacă este cazul, inițierea tratamentului cu doze mai mici.
Mod de administrare
Comprimatele au o linie de scor și pot fi tăiate în jumătate pentru a fi mai ușor de înghițit. Cu toate acestea, comprimatul nu poate fi împărțit în doze egale.
Tolep poate fi luat cu sau fără mese.
Monitorizarea terapeutică
Efectul terapeutic al oxcarbazepinei se exercită în principal prin metabolitul său activ 10-monohidroxi-derivat (MHD). Monitorizarea de rutină a nivelurilor plasmatice de oxcarbazepină sau MHD nu este justificată. Totuși, monitorizarea nivelurilor plasmatice MHD poate fi luată în considerare. pentru a exclude neaderarea la tratament sau în situații în care este de așteptat modificarea clearance-ului MHD, inclusiv următoarele:
- modificări ale funcției renale (vezi „Pacienți cu insuficiență renală”)
- sarcină (vezi „Atenționări speciale - Sarcină”)
- utilizarea concomitentă a medicamentelor care au un efect inductiv asupra enzimelor hepatice (vezi „Interacțiuni”).
- vârsta pediatrică și geriatrică
Dacă apare oricare dintre aceste situații, doza de Tolep poate fi ajustată (pe baza nivelurilor plasmatice măsurate la 2-4 ore după administrare) pentru a menține valorile plasmatice maxime ale MHD <35 mg / l.
Supradozaj Ce trebuie făcut dacă ați luat prea mult Tolep
Au fost raportate cazuri izolate de supradozaj. Doza maximă luată a fost de aproximativ 24.000 mg.
semne si simptome
Echilibrul hidro-electrolitic: hiponatremie
Tulburări oculare: diplopie, mioză, vedere încețoșată
Tulburări gastro-intestinale: greață, vărsături, hiperkinezie
Tulburări generale și condiții la locul de administrare: astenie
Investigații: depresie a frecvenței respiratorii, prelungirea intervalului QTc
Tulburări ale sistemului nervos: somnolență și somnolență, amețeli, ataxie, nistagmus, tremor, tulburări de coordonare (coordonare anormală), convulsii, cefalee, comă, inconștiență, diskinezie
Tulburări psihiatrice: agresivitate, agitație, stare confuzională
Tulburări vasculare: hipotensiune arterială
Tulburări respiratorii, toracice și mediastinale: dispnee.
Tratament
Nu există un antidot specific. Pacienții cu simptome de otrăvire din cauza unei supradoze de Tolep trebuie tratați cu terapie simptomatică și de susținere adecvată, iar medicamentul trebuie opțional îndepărtat prin spălare gastrică sau inactivat prin administrarea de cărbune activat.
În caz de ingestie / administrare accidentală a unei doze excesive de Tolep, anunțați imediat medicul sau mergeți la cel mai apropiat spital.
Efecte secundare Care sunt efectele secundare ale Tolep
Ca toate medicamentele, Tolep poate provoca reacții adverse, deși nu apar la toate persoanele.
Cele mai frecvent raportate reacții adverse sunt somnolență, cefalee, amețeli, diplopie, greață, vărsături și oboseală, care au apărut la mai mult de 10% dintre pacienți.
Efectele nedorite sunt enumerate mai jos, împărțite pe tip și frecvență. În cadrul fiecărei clase de frecvență, reacțiile adverse sunt raportate în ordinea descrescătoare a severității.
Tulburări ale sistemului sanguin și limfatic
- Mai puțin frecvente: leucopenie.
- Foarte rare: trombocitopenie
- Cu frecvență necunoscută: depresie a măduvei osoase, anemie aplastică, agranulocitoză, pancitopenie, neutropenie.
Tulburări ale sistemului imunitar
- Foarte rare: hipersensibilitate (inclusiv hipersensibilitate cu mai multe organe) caracterizată prin erupție cutanată, febră. Alte organe sau sisteme pot fi afectate, cum ar fi sângele și sistemul limfatic (de exemplu, eozinofilie, trombocitopenie, leucopenie, limfadenopatie, splenomegalie), ficatul (de exemplu, rezultate anormale ale testelor funcției hepatice, hepatită), mușchii și articulațiile (de exemplu, umflarea articulațiilor, mialgia , artralgie), sistemul nervos (ex. encefalopatie hepatică), rinichii (ex. proteinurie, nefrită interstițială, insuficiență renală), plămânii (ex. dispnee, edem pulmonar, astm, bronhospasm, boală pulmonară interstițială), angioedem.
- Cu frecvență necunoscută: reacții anafilactice.
Patologii endocrine
- Nu se cunoaște: hipotiroidism.
Tulburări de metabolism și nutriție
- Frecvente: hiponatremie.
- Foarte rare: hiponatremie * asociată cu semne și simptome precum convulsii, confuzie, alterare a conștiinței, encefalopatie, tulburări vizuale (de exemplu, vedere încețoșată), vărsături, greață, deficit de acid folic
Tulburari psihiatrice
- Frecvente: stare confuzională, depresie, apatie, agitație (de ex. Nervozitate), fragilitate emoțională.
Tulburări ale sistemului nervos
- Foarte frecvente: somnolență, cefalee, amețeli.
- Frecvente: ataxie, tremor, nistagmus, tulburări de concentrație, amnezie.
Tulburări oculare
- Foarte frecvente: diplopie.
- Frecvente: vedere încețoșată, tulburări vizuale.
Tulburări ale urechii și labirintului
- Frecvente: amețeli
Patologii cardiace
- Foarte rare: aritmii, bloc atrioventricular.
Patologii vasculare
- Cu frecvență necunoscută: hipertensiune arterială.
Tulburări gastrointestinale
- Foarte frecvente: greață, vărsături.
- Frecvente: diaree, constipație, dureri abdominale.
- Foarte rare: pancreatită și / sau creștere a lipazei și / sau amilazei
Tulburări hepatobiliare
- Foarte rare: hepatită.
Afecțiuni ale pielii și ale țesutului subcutanat
- Frecvente: erupții cutanate, alopecie, acnee.
- Mai puțin frecvente: urticarie.
- Foarte rare: angioedem, sindrom Stevens-Johnson, necroliză epidermică toxică (sindrom Lyell), eritem multiform (vezi „Precauții pentru utilizare”).
Tulburări musculo-scheletice și ale țesutului conjunctiv
- Foarte rare: lupus eritematos sistemic
Tulburări generale și condiții la locul administrării
- Foarte frecvente: oboseală. - Frecvente: astenie.
Testele de diagnostic
- Mai puțin frecvente: valori crescute ale enzimelor hepatice, valori crescute ale fosfatazei alcaline din sânge.
- Foarte rare: creșterea valorilor amilazei, creșterea valorilor lipazei.
- Nu se cunoaște: scăderea nivelului T4
* Hiponatremie semnificativă clinic (sodiu sodic sodic
Reacții adverse din rapoarte spontane și literatură (frecvență necunoscută)
Următoarele reacții adverse provin din experiența de după punerea pe piață cu Tolep și se referă la rapoarte spontane și cazuri descrise în literatură. Deoarece aceste reacții apar spontan dintr-o populație de dimensiuni incerte, nu este posibil să se estimeze cu certitudine frecvența care este, prin urmare, indicată . ca „necunoscut”. Reacțiile adverse sunt enumerate în funcție de clasa de sisteme și organe MedDRA. În cadrul fiecărei clase, reacțiile adverse sunt enumerate în ordinea descrescătoare a severității.
Tulburări ale sistemului imunitar
Erupții medicamentoase cu eozinofilie și simptome sistemice (DRESS).
Tulburări de metabolism și nutriție
Sindrom de secreție inadecvată de ADH cu semne și simptome precum letargie, greață, amețeli, scăderea osmolalității serice (sânge), vărsături, cefalee, confuzie sau alte semne și simptome neurologice.
Afecțiuni ale pielii și ale țesutului subcutanat
Pustuloza exantematoasă acută generalizată (AGEP).
Leziuni, otrăviri și complicații procedurale
Cade.
Tulburări ale sistemului nervos
Tulburări de vorbire (inclusiv disartrie), mai frecvente în timpul fazei de titrare. Tulburări musculo-scheletice și ale țesutului conjunctiv Au fost raportate cazuri de boli osoase, inclusiv osteopenie și osteoporoză (subțierea oaselor) și fracturi. Adresați-vă medicului dumneavoastră sau farmacistului dacă ați luat medicamente antiepileptice de mult timp sau dacă aveți antecedente de osteoporoză sau dacă luați steroizi.
Respectarea instrucțiunilor conținute în prospect reduce riscul de efecte nedorite.
Raportarea efectelor secundare
Dacă manifestați orice reacții adverse, adresați-vă medicului dumneavoastră sau farmacistului, inclusiv orice reacții adverse posibile care nu sunt enumerate în acest prospect. De asemenea, puteți raporta reacțiile adverse direct prin intermediul site-ului http://www.agenziafarmaco.gov.it/it/responsabili. Raportând reacțiile adverse, puteți contribui la furnizarea mai multor informații despre siguranța acestui medicament.
Expirare și reținere
Expirare: vezi data de expirare tipărită pe ambalaj
Data de expirare se referă la produsul ambalat intact și depozitat corect.
Atenție: nu utilizați medicamentul după data de expirare indicată pe ambalaj
Acest medicament nu necesită condiții speciale de păstrare.
Medicamentele nu trebuie aruncate pe calea apei uzate sau a deșeurilor menajere. Întrebați farmacistul cum să aruncați medicamentele pe care nu le mai utilizați. Acest lucru va ajuta la protejarea mediului.
Nu lăsați acest medicament la vederea și îndemâna copiilor
Compoziție și formă farmaceutică
Compoziţie
Fiecare comprimat divizibil de 300 mg conține: 300 mg oxcarbazepină.
Fiecare comprimat divizibil de 600 mg conține: 600 mg oxcarbazepină.
Excipienți: silice coloidală anhidră; celuloză microcristalină; hipromeloză; oxid de fier roșu; oxid galben de fier; stearat de magneziu; carmeloză sodică.
Forma și conținutul farmaceutic
Tablete
Cutie cu 50 de comprimate divizibile de 300 mg.
Cutie cu 50 de comprimate divizibile de 600 mg.
Prospect sursă: AIFA (Agenția italiană pentru medicamente). Conținut publicat în ianuarie 2016. Este posibil ca informațiile prezente să nu fie actualizate.
Pentru a avea acces la cea mai actualizată versiune, este recomandabil să accesați site-ul web AIFA (Agenția italiană pentru medicamente). Declinare de responsabilitate și informații utile.
01.0 DENUMIREA PRODUSULUI MEDICAMENTAL
COMPRIMATE TOLEP
02.0 COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ
Fiecare comprimat divizibil de 300 mg conține:
Oxcarbazepină 300 mg
Fiecare comprimat divizibil de 600 mg conține:
Oxcarbazepină 600 mg
Pentru lista completă a excipienților, vezi secțiunea 6.1.
03.0 FORMA FARMACEUTICĂ
Tablete.
04.0 INFORMAȚII CLINICE
04.1 Indicații terapeutice
Epilepsie
- convulsii parțiale cu sau fără generalizare secundară
- crize tonico-clonice generalizate.
04.2 Doze și mod de administrare
Dozare
Tratamentul cu Tolep, indiferent dacă este administrat ca mono sau polifarmacie, trebuie început treptat, iar doza trebuie adaptată la nevoile fiecărui pacient.
Adulți
Monoterapie: doza inițială recomandată este de 300 mg pe zi, doza poate fi crescută treptat până se obține cel mai bun răspuns, de obicei în jur de 600-1200 mg / zi.
Politerapie (la pacienții cu epilepsie necontrolată sau în cazuri refractare la terapie): doza inițială recomandată este de 300 mg pe zi, doza poate fi crescută treptat până se obține cel mai bun răspuns.Doza de întreținere variază între 900 și 3000 mg / zi.
Copii
Experiența cu Tolep la copii este limitată și nu există experiență la copiii cu vârsta sub 3 ani.
În plus, deoarece este dificil să personalizați doza cu comprimatele disponibile și să împărțiți doza zilnică în 2-3 ori, nu este recomandată utilizarea Tolep la vârsta pediatrică. Cu toate acestea, utilizarea produsului la copii cu vârsta sub 3 ani ar trebui evitată.
Pacienți cu insuficiență hepatică
Nu este necesară ajustarea dozelor la pacienții cu insuficiență hepatică ușoară până la moderată. Tolep nu a fost studiat la pacienții cu insuficiență hepatică severă, prin urmare se recomandă prudență la administrarea Tolep acestor pacienți.
Pacienți cu insuficiență renală
La pacienții cu insuficiență renală (clearance-ul creatininei mai mic de 30 ml / min), doza de Tolep trebuie stabilită cu atenție, iar doza crește cel puțin săptămânal până la obținerea răspunsului clinic dorit.
Administrare
În general, Tolep trebuie administrat de 3 ori pe zi, dar, atunci când este posibil, trebuie administrat de două ori pe zi. Comprimatele pot fi administrate în timpul sau după masă, cu puțin lichid.
04.3 Contraindicații
Hipersensibilitate la substanța activă sau la oricare dintre excipienți.
04.4 Avertismente speciale și precauții adecvate pentru utilizare
Hipersensibilitate
În perioada de după punerea pe piață, au fost raportate reacții de hipersensibilitate (imediată) de clasa I, inclusiv erupții cutanate, prurit, urticarie, angioedem și cazuri de anafilaxie. Au fost raportate cazuri de anafilaxie și angioedem care afectează laringele, glota, buzele și pleoapele după administrarea primei doze sau a dozelor ulterioare de Tolep. Dacă aceste reacții apar la un pacient după tratamentul cu Tolep, acestea trebuie să întrerupă administrarea Tolep și terapia alternativă ar trebui să fie iniţiat.
Pacienții care au prezentat reacții de hipersensibilitate la carbamazepină trebuie informați că aproximativ 25-30% din aceiași pacienți pot prezenta reacții similare (de exemplu, reacții cutanate severe) după administrarea Tolep (vezi pct. 4.8).
Reacțiile de hipersensibilitate, inclusiv reacțiile de hipersensibilitate cu mai multe organe, pot apărea și la pacienții care nu au avut episoade anterioare de hipersensibilitate la carbamazepină. Aceste reacții pot afecta pielea, ficatul, sângele și sistemul limfatic sau alte organe, fie individual, fie simultan în cazul unei reacții sistemice (vezi pct. 4.8). În general, dacă apar semne și simptome care sugerează reacții de hipersensibilitate, administrarea Tolep trebuie oprită imediat.
Efecte dermatologice
În cazuri foarte rare, au fost raportate reacții dermatologice severe, inclusiv sindromul Stevens-Johnson, necroliza epidermică toxică (sindromul Lyell) și eritemul multiform, în asociere cu utilizarea Tolep. Pacienții cu reacții dermatologice severe pot avea nevoie de spitalizare, deoarece aceste afecțiuni pot pune viața în pericol și foarte rar letale. Timpul mediu de debut a fost de 19 zile. Au fost raportate mai multe cazuri izolate de reapariție a reacțiilor cutanate severe la reluarea tratamentului cu Tolep. Pacienții tratați cu Tolep care dezvoltă o reacție cutanată trebuie evaluați imediat și tratamentul cu Tolep trebuie oprit imediat, cu excepția cazului în care erupția cutanată nu este în mod clar legată de medicament. Dacă tratamentul este întrerupt, trebuie luată în considerare înlocuirea Tolep cu un alt medicament antiepileptic pentru a evita atacurile de sevraj. Tolep nu trebuie re-administrat la pacienții care au întrerupt tratamentul din cauza reacțiilor de hipersensibilitate (vezi pct. 4.3).
Allele HLA-B * 1502 - în populația chineză de etnie Han, thailandeză și alte populații asiatice
La persoanele de origine chineză de etnie Han și de origine thailandeză, pozitivitatea față de alela HLA-B * 1502 s-a dovedit a fi puternic asociată cu riscul de a dezvolta reacții cutanate severe precum sindromul Steven-Johnson (SJS) în timpul tratamentului cu carbamazepină. Structura chimică a oxcarbazepinei este similară cu cea a carbamazepinei și este posibil ca pacienții care sunt pozitivi pentru HLA-B * 1502 să fie, de asemenea, expuși riscului de a dezvolta SJS după tratamentul cu oxcarbazepină. Unele date sugerează că există o astfel de asociere. oxcarbazepina Prevalența purtătorilor de alelă HLA-B * 1502 este de aproximativ 10% la populațiile chinezești Han și Thai. Frecvența alelelor de până la aproximativ 2% și 6% au fost raportate în Coreea și, respectiv, în India.
Ori de câte ori este posibil, acești indivizi trebuie examinați pentru această alelă înainte de a începe tratamentul cu carbamazepină sau substanțe chimice. Dacă pacienții cu aceste origini dau rezultate pozitive pentru alela HLA-B * 1502, utilizarea Tolep poate fi luată în considerare numai dacă beneficiile scontate depășesc riscurile.
Datorită prevalenței acestei alele la alte populații asiatice (de exemplu, peste 15% în Filipine și Malaezia), poate fi luată în considerare testarea prezenței alelei HLA-B * 1502 la populațiile cu risc genetic.
Prevalența alelei HLA-B * 1502 este neglijabilă, de exemplu la populațiile de origine europeană, africane, într-un eșantion de populație hispanică și în japoneză (
Prezența alelei HLA-B * 1502 poate fi un factor de risc pentru dezvoltarea SJS / TEN la pacienții chinezi care iau alte medicamente antiepileptice care pot provoca SJS / TEN. Prin urmare, la pacienții pozitivi pentru alela HLA-B. * 1502 , trebuie să aveți grijă să evitați utilizarea altor medicamente care pot provoca SJS / TEN.
Allele HLA-A * 3101 - la populația de origine europeană și la populația japoneză
Unele date sugerează că alela HLA-A * 3101 este asociată cu un risc crescut de reacții adverse cutanate induse de carbamazepină, inclusiv SJS și TEN, erupție cutanată cu eozinofilie (DRESS) sau pustuloză exantematoasă acută generalizată mai puțin severă (AGEP) și erupție maculopapulară în oameni de origine europeană și japoneză.
Frecvența alelei HLA-A * 3101 variază foarte mult în rândul populațiilor etnice. Alela HLA-A * 3101 are o prevalență de 2 până la 5% în populațiile europene și aproximativ 10% în populația japoneză.
Prezența alelei HLA-A * 3101 poate crește riscul reacțiilor cutanate induse de carbamazepină (majoritatea mai puțin severe) de la 5,0% la populația generală la 26,0% la subiecții de origine europeană, în timp ce absența acesteia poate reduce riscul de la 5,0 % la 3,8%.
Nu există date suficiente pentru a susține recomandarea de screening pentru HLA-A * 3101 înainte de a începe tratamentul cu carbamazepină sau substanțe chimice.
Dacă se constată că pacienții cu origine europeană sau japoneză sunt pozitivi pentru alela HLA-A * 3101, utilizarea carbamazepinei sau a substanțelor chimice ar trebui luată în considerare numai dacă beneficiile scontate depășesc riscurile.
Limitările screeningului genetic
Screeningul genetic nu ar trebui să înlocuiască niciodată „observația clinică adecvată și gestionarea pacientului. Mulți pacienți asiatici HLA-B * 1502 tratați cu Tolep nu vor dezvolta SJS / TEN și la pacienții de orice etnie negativi pentru HLA-B * 1502.„ HLA-B * Alela 1502, cu toate acestea, pot apărea episoade de SJS / TEN. În mod similar, mulți pacienți care sunt pozitivi pentru alela HLA-A * 3101 și tratați cu Tolep nu vor dezvolta SJS, TEN, DRESS, AGEP sau erupție maculopapulară și la pacienții cu orice etnie negativă pentru alela HLA-A * 3101, cu toate acestea, pot apărea aceste reacții adverse cutanate severe.
Hiponatremie
S-au observat concentrații de sodiu sub 125 mmol / l, în general asimptomatice și care nu necesită ajustarea terapiei, la până la 2,7% dintre pacienții tratați cu Tolep. Rezultatele studiilor clinice arată că nivelurile serice de sodiu revin la normal după reducerea dozei de Tolep, când dozarea este întreruptă sau când pacientul este tratat în mod conservator (de exemplu, prin limitarea aportului de lichide). sau la pacienții tratați concomitent cu medicamente care scad sodiul (de exemplu, diuretice, desmopresină), precum și antiinflamatoare nesteroidiene (de exemplu, indometacin), nivelurile serice de sodiu trebuie măsurate înainte de inițierea terapiei. aproximativ două săptămâni și, ulterior, la intervale lunare în primele trei luni de terapie, sau după cum este necesar clinic. Acești factori de risc pot afecta în principal pacienții vârstnici.
Pacienții deja tratați cu Tolep care încep tratamentul cu medicamente care scad concentrațiile de sodiu ar trebui să fie supuși acelorași verificări ale concentrațiilor serice de sodiu. În general, dacă simptomele sugestive de hiponatremie apar în timpul tratamentului cu Tolep (vezi pct. 4.8), pot fi stabilite măsurători ale nivelului seric de sodiu. Pentru alți pacienți, aceste teste pot face parte din controalele normale de laborator.
Toți pacienții cu insuficiență cardiacă și insuficiență cardiacă secundară ar trebui să fie verificați greutatea în mod regulat pentru a se asigura că retenția de lichide nu are loc. În cazul retenției de lichide sau agravării afecțiunilor cardiace, nivelurile serice de sodiu trebuie monitorizate. Dacă se observă hiponatremie, reducerea aportului de lichide poate reprezenta o „contramăsură importantă. Deoarece tratamentul cu oxcarbazepină poate duce, în cazuri foarte rare, la agravarea conducerii cardiace, pacienții cu tulburări de conducere preexistente (de exemplu, ventricular, aritmie) trebuie să fie monitorizat indeaproape.
Funcția hepatică
Au fost raportate episoade foarte rare de hepatită, care s-au rezolvat favorabil în majoritatea cazurilor. Atunci când se suspectează un efect hepatic, funcția hepatică trebuie monitorizată și trebuie luată în considerare întreruperea tratamentului cu Tolep.
Efecte hematologice
Au fost raportate cazuri foarte rare de agranulocitoză, anemie aplastică și pancitopenie la pacienții tratați cu Tolep după punerea pe piață (vezi pct. 4.8).
Întreruperea tratamentului trebuie luată în considerare dacă apar semne de depresie semnificativă a măduvei osoase.
Contraceptive hormonale
Pacienții cu vârsta fertilă trebuie informați că utilizarea concomitentă a Tolep și contraceptivele hormonale poate anula efectul acestora (vezi pct. 4.5). Se recomandă utilizarea în timpul terapiei cu Tolep a unor metode contraceptive non-hormonale alternative.
Alcool
Este necesară o prudență extremă în cazul în care se consumă băuturi alcoolice în timpul tratamentului cu Tolep datorită posibilului efect sedativ aditiv.
Ideea și comportamentul sinucigaș
Au fost raportate cazuri de idei și comportamente suicidare la pacienții cărora li s-au administrat medicamente antiepileptice în diferite indicații ale acestora. O meta-analiză a studiilor clinice randomizate versus placebo a evidențiat, de asemenea, prezența unei creșteri modeste a riscului de ideație și comportament suicidar.
Mecanismul acestui risc nu a fost stabilit și datele disponibile nu exclud posibilitatea unui risc crescut cu Tolep.
Prin urmare, pacienții trebuie monitorizați pentru a detecta semne de idei și comportament suicidar și, dacă este cazul, trebuie luat în considerare tratamentul adecvat. Pacienții (și îngrijitorii) ar trebui să fie instruiți să anunțe medicul curant dacă apar semne de idei sau comportamente suicidare.
Întreruperea tratamentului
Ca și în cazul altor medicamente antiepileptice, tratamentul cu Tolep trebuie întrerupt treptat pentru a minimiza riscul creșterii frecvenței convulsiilor.
04.5 Interacțiuni cu alte medicamente și alte forme de interacțiune
Inducerea enzimei
Oxcarbazepina și metabolitul său farmacologic activ (un derivat monohidroxi MHD) sunt inductori slabi in vitro Și in vivo ale enzimelor citocromului P450 CYP3A4 și CYP3A5, responsabile de metabolismul multor medicamente, precum imunosupresoare (de exemplu ciclosporină, tacrolimus), contraceptive orale (vezi mai jos) și alte medicamente antiepileptice (de exemplu carbamazepină), rezultând astfel o scădere a plasmei nivelurile acestor medicamente (vezi tabelul de mai jos care rezumă interacțiunile cu alte medicamente antiepileptice).
In vitro oxcarbazepina și MHD sunt inductori slabi ai enzimei UDP-glucuronil transferază (nu se cunosc efectele asupra enzimelor specifice aparținând acestei familii). in vivo Oxcarbazepina și MHD pot avea un efect inductor mic asupra metabolismului medicamentelor care sunt eliminate în principal după conjugare prin enzima UDP-glucuronil transferază. La începerea tratamentului sau modificarea dozei de Tolep, noul nivel de inducție poate dura 2 până la 3 săptămâni .
La întreruperea tratamentului cu Tolep, poate fi necesară reducerea dozei de medicamente concomitente după o evaluare clinică adecvată și / sau o monitorizare a nivelului plasmatic. Este probabil ca inducția să scadă treptat peste 2 până la 3 săptămâni după întreruperea tratamentului.
Contraceptive hormonale: s-a demonstrat că Tolep afectează cele două componente ale unui contraceptiv oral, etinilestradiolul (EE) și levonorgestrelul (GNL). Valorile medii ale ASC ale EE și GNL scad, respectiv, cu 48-52% și cu 32-52% . Prin urmare, utilizarea concomitentă a Tolep și contraceptivele hormonale poate face ca acestea din urmă să fie ineficiente (vezi pct. 4.4). Ar trebui luate în considerare alte metode contraceptive, altele decât cele hormonale.
Inhibare enzimatică
Oxcarbazepina și MHD inhibă CYP2C19. Prin urmare, pot apărea interacțiuni atunci când se administrează concomitent doze mari de Tolep și medicamente metabolizate de CYP2C19 (de exemplu, fenitoină). Nivelurile plasmatice de fenitoină cresc cu până la 40% după administrarea de Tolep la doze mai mari de 1200 mg / zi (vezi tabelul de mai jos care rezumă interacțiunile cu alte medicamente antiepileptice). În acest caz, poate fi necesară o reducere a dozei de fenitoină (vezi pct. 4.2).
Medicamente antiepileptice
Interacțiuni potențiale între Tolep și alte medicamente antiepileptice au fost observate în timpul studiilor clinice. Efectul acestor interacțiuni asupra valorilor medii ale ASC și Cmin sunt rezumate în tabelul următor.
Rezumatul interacțiunilor dintre Tolep și alte medicamente antiepileptice
* Rezultatele preliminare indică faptul că oxcarbazepina poate duce la scăderea concentrațiilor de lamotrigină, posibil importante la copii. Cu toate acestea, această interacțiune potențială a oxcarbazepinei pare a fi mai mică decât cea observată la administrarea concomitentă a medicamentelor care induc enzime, cum ar fi carbamazepina, fenobarbitalul și fenitoina.
Inductorii puternici ai enzimelor citocromului P450 (adică carbamazepină, fenitoină și fenobarbital) sunt capabili să reducă nivelurile plasmatice de MHD la adulți (29-40%); la copiii cu vârsta cuprinsă între 4 și 12 ani, clearance-ul MHD crește cu aproximativ 35% atunci când este administrat unul dintre cele trei medicamente antiepileptice care induc enzimele, comparativ cu monoterapia. Terapia concomitentă cu Tolep și lamotrigină a fost asociată cu un risc crescut de evenimente adverse (greață, somnolență, amețeli și cefalee). Atunci când unul sau mai multe medicamente antiepileptice sunt administrate concomitent cu Tolep, poate fi necesară ajustarea prudentă a dozei și / sau monitorizarea concentrațiilor plasmatice, în special la copii și adolescenți tratați concomitent cu lamotrigină.
Nu s-au observat fenomene de autoinducție cu Tolep.
Interacțiuni cu alte medicamente
Cimetidina, eritromicina, viloxazina, warfarina și dextropropoxifenul nu au niciun efect asupra farmacocineticii MHD.
O interacțiune între oxcarbazepină și inhibitori MAO este teoretic posibilă, pe baza unei relații structurale între oxcarbazepină și antidepresive triciclice.
Pacienții tratați cu antidepresivi triciclici au fost incluși în studiile clinice și nu au fost observate interacțiuni semnificative clinic.
Administrarea de oxcarbazepină și litiu poate determina neurotoxicitate crescută.
04.6 Sarcina și alăptarea
Sarcina
Riscurile asociate cu epilepsia și medicamentele antiepileptice în general:
Pacientelor care pot rămâne însărcinate sau au vârsta fertilă trebuie să li se ofere sfaturi de specialitate.
Necesitatea tratamentului antiepileptic trebuie reevaluată atunci când pacientul intenționează să rămână gravidă.
S-a demonstrat că la persoanele născute de femei cu epilepsie, incidența malformațiilor este de două până la trei ori mai mare decât la o frecvență de aproximativ 3% din populația generală. O creștere a malformațiilor cu politerapie nu a fost observată la populația tratată. măsura în care tratamentul este responsabil pentru boală a fost clarificată.
Mai mult, terapia antiepileptică eficientă nu trebuie întreruptă, deoarece agravarea bolii este dăunătoare atât mamei, cât și fătului.
Riscuri asociate cu oxcarbazepina:
Datele clinice privind expunerea în timpul sarcinii sunt încă insuficiente pentru a evalua potențialul teratogen al oxcarbazepinei. În studiile la animale, s-a observat o incidență crescută a mortalității embrionilor, întârzierea creșterii și prezența malformațiilor la doze toxice materne (vezi pct. 5.3).
Luând în considerare toate acestea:
- Dacă pacienții care iau Tolep rămân gravide sau intenționează să rămână gravide, utilizarea acestui produs trebuie reevaluată cu atenție. Trebuie administrate cele mai mici doze eficiente, iar monoterapia este preferabilă, acolo unde este posibil, cel puțin în primele trei luni de sarcină. ..
- Pacienții trebuie informați că riscul apariției malformațiilor poate crește și trebuie să poată fi supus unui screening prenatal.
- În timpul sarcinii, terapia antiepileptică eficientă cu oxcarbazepină nu trebuie întreruptă, deoarece agravarea bolii este dăunătoare atât mamei, cât și fătului.
Monitorizare și prevenire
Medicamentele antiepileptice pot contribui la deficitul de acid folic, unul dintre posibilii factori responsabili pentru anomaliile fetale. Se recomandă administrarea suplimentară de acid folic înainte și în timpul sarcinii. Deoarece eficacitatea acestei administrări suplimentare nu este dovedită, oportunitatea unui diagnostic prenatal specific poate fi luată în considerare și la femeile în tratament suplimentar cu acid folic.
Datele de la un număr limitat de femei indică faptul că în timpul sarcinii, din cauza modificărilor fiziologice care apar, nivelurile plasmatice ale metabolitului activ al oxcarbazepinei (derivatul monohidroxilat, MHD) pot scădea treptat. Prin urmare, la femeile care urmează tratament cu Tolep în timpul sarcinii, se recomandă monitorizarea atentă a răspunsului clinic și monitorizarea concentrațiilor plasmatice ale MHD pentru a asigura un control adecvat al convulsiilor în timpul sarcinii. Monitorizarea concentrațiilor plasmatice de MHD poate fi luată în considerare și după naștere, mai ales dacă dozele de medicament au fost crescute în timpul sarcinii.
La nou-născut
La nou-născuți au fost raportate tulburări de sângerare cauzate de medicamente antiepileptice. Ca măsură de precauție, vitamina K1 trebuie administrată în scop preventiv în ultimele săptămâni de sarcină și ulterior nou-născuților.
Timp de hrănire
Oxcarbazepina și metabolitul său activ (MHD) sunt excretați în laptele matern. Pentru ambii compuși raportul concentrației lapte / plasmă a fost de 0,5. Efectele asupra nou-născuților expuși la Tolep în acest mod sunt necunoscute. Prin urmare, Tolep nu trebuie administrat în timpul alăptării.
04.7 Efecte asupra capacității de a conduce vehicule și de a folosi utilaje
Utilizarea Tolep a fost asociată cu apariția efectelor nedorite, cum ar fi amețeli și somnolență (vezi pct. 4.8). Prin urmare, pacienții trebuie avertizați că abilitățile lor fizice și / sau mentale necesare pentru a conduce vehicule sau a folosi utilaje ar putea fi afectate.
04.8 Efecte nedorite
Cele mai frecvent raportate reacții adverse sunt somnolență, cefalee, amețeli, diplopie, greață, vărsături și oboseală, care au apărut la mai mult de 10% dintre pacienți.
Efectele nedorite descrise mai jos, pe sistem, se referă la evenimentele adverse raportate în studiile clinice evaluate legate de tratamentul cu Tolep. În plus, au fost analizate rapoartele de evenimente adverse semnificative din punct de vedere clinic din farmacovigilența după punerea pe piață și din programele de utilizare compasională.
Estimarea frecvenței *: Foarte comun: ≥ 1/10; Uzual: ≥ 1/100 - ≥ 1/1.000 - ≥ 1/10.000 -
În cadrul fiecărei clase de frecvență, reacțiile adverse sunt raportate în ordinea descrescătoare a severității.
* pe baza clasificării frecvenței CIOMS III
† Hiponatremie semnificativă clinic (sodiu
Reacții adverse din rapoarte spontane și literatură (frecvență necunoscută)
Următoarele reacții adverse provin din experiența de după punerea pe piață cu Tolep și se referă la rapoarte spontane și cazuri descrise în literatură. Deoarece aceste reacții apar spontan dintr-o populație de dimensiuni incerte, nu este posibil să se estimeze cu certitudine frecvența care este, prin urmare, indicată . ca „necunoscut”. Reacțiile adverse sunt enumerate în funcție de clasa de sisteme și organe MedDRA. În cadrul fiecărei clase, reacțiile adverse sunt enumerate în ordinea descrescătoare a severității.
Tulburări ale sistemului imunitar
Erupții medicamentoase cu eozinofilie și simptome sistemice (DRESS).
Afecțiuni ale pielii și ale țesutului subcutanat
Pustuloza exantematoasă acută generalizată (AGEP).
Tulburări musculo-scheletice și ale țesutului conjunctiv
Au fost raportate scăderea densității minerale osoase, osteopenie, osteoporoză și fracturi la pacienții tratați pe termen lung cu Tolep. Nu a fost identificat mecanismul prin care Tolep afectează metabolismul osos.
04.9 Supradozaj
Au fost raportate cazuri izolate de supradozaj. Doza maximă luată a fost de aproximativ 24.000 mg. Toți pacienții s-au recuperat numai cu tratament simptomatic. Simptomele supradozajului includ somnolență, amețeli, greață, vărsături, hiperkinezie, hiponatremie, ataxie și nistagmus. Nu există un antidot specific.Pacienții cu simptome de otrăvire din cauza unei supradoze de Tolep trebuie tratați cu o terapie simptomatică și de susținere adecvată, iar medicamentul trebuie opțional îndepărtat prin spălare gastrică și / sau inactivat prin administrarea de cărbune activat.
05.0 PROPRIETĂȚI FARMACOLOGICE
05.1 Proprietăți farmacodinamice
Grupa farmacoterapeutică: Antiepileptic, derivat al carboxamidei, codul ATC: N03AF02
Ingredientul activ al lui Tolep oxcarbazepina și metabolitul său 10-monohidroxilat exercită un efect antiepileptic.
Ambele substanțe active s-au dovedit a fi anticonvulsivante puternice și eficiente într-o serie de studii farmacologice la animale.
Mai mult, în modelul „pisicii furioase”, rezultatele obținute sunt indicative ale unui potențial efect psihotrop la oameni.
Studiile la animale, care privesc spectrul de activitate al oxcarbazepinei, indică o eficacitate deosebită în convulsiile tonico-clonice parțiale și generalizate.
Mecanismul anticonvulsivant de acțiune al oxcarbazepinei și al principalului său metabolit a fost doar parțial elucidat; totuși, se crede că, similar carbamazepinei, aceste substanțe stabilizează membranele neuronale supraexcitate, inhibă descărcările neuronale repetitive și transmiterea impulsurilor sinaptice.
Substanța activă a Tolep nu prezintă autoinducție: farmacocinetica oxcarbazepinei și metabolitul său farmacologic activ nu se modifică după administrarea repetată. .
Nicio influență Tolep asupra urmelor EEG nu este evidentă.
Tolep este adecvat atât ca monoterapie, cât și în asociere cu alte antiepileptice (de exemplu, valproat, fenitoină).
05.2 Proprietăți farmacocinetice
Absorbţie
Absorbție rapidă și practic completă, cel mult 95%.
Concentrația plasmatică: datorită metabolismului rapid, concentrația plasmatică a oxcarbazepinei este neglijabilă și metabolitul activ farmacologic (10-hidroxi-10,11-dihidro-5-carbamoil-5H-dibenzazepină = 10-monohidroxi derivat) predomină.
După doze orale unice de 150-600 mg oxcarbazepină, ASC plasmatică a metabolitului 10-monohidroxi arată o corelație liniară cu doza administrată.
La pacienții cu epilepsie, dozele zilnice de oxcarbazepină variind de la 600 la 5400 mg produc concentrații plasmatice la starea de echilibru ale metabolitului activ variind de la 2,1 la 36,7 μg / ml. Vârfurile plasmatice ale metabolitului activ sunt atinse, după administrare unică, în decurs de 4 ore. Farmacocinetica oxcarbazepinei și a metabolitului său activ rămân neschimbate chiar și după administrarea orală repetată.
La copii, concentrațiile la starea de echilibru sunt comparabile cu cele la adulți.
Distribuție
Volumul de distribuție: 0,8 l / kg (metabolit activ).
Legarea proteinelor: 38% (metabolit activ).
Metabolism
Oxcarbazepina se reduce rapid în mare măsură la metabolitul său farmacologic activ, derivatul 10-monohidroxi (prezent atât liber, cât și conjugat, reprezentând aproximativ 60% din compușii excretați de rinichi).
Metaboliți minori: glucuronid direct și sulfat de oxcarbazepină și metabolit 10,11-dihidroxi (aproximativ 5-15% fiecare) .Oxcarbazepină nemodificată: mai puțin de 0,3%.
Eliminare
Eliminare completă în termen de 10 zile. Mai mult de 95% din doza administrată este excretată în urină, mai ales sub formă de metaboliți; aproximativ 3% cu fecale.
Timp de înjumătățire plasmatică eliminat 8-13 ore (metabolit activ).
05.3 Date preclinice de siguranță
Datele preclinice obținute din studii de toxicitate după doze repetate, siguranță farmacologică și studii de genotoxicitate efectuate cu oxcarbazepină și metabolitul său farmacologic activ (derivat monohidroxilat, MHD), nu au evidențiat niciun risc special pentru om.
Semne de nefrotoxicitate au fost observate în studii cu doze repetate efectuate la șobolani, dar nu la șoareci și câini. Deoarece nu au fost raportate efecte similare la om, semnificația clinică a acestor constatări la șobolan rămâne necunoscută.
Testele de imunostimulare efectuate la șoareci au arătat că MHD (și într-o măsură mai mică oxcarbazepina) poate induce hipersensibilitate întârziată.
Studiile la animale au relevat, la doze toxice materne, o creștere a incidenței mortalității embrionare și, uneori, întârzierea creșterii ante și / sau postnatală. la malformațiile fetale la șobolan au apărut la doze care au fost, de asemenea, toxice pentru mamă (vezi pct. 4.6).
În studiile de carcinogenitate, tumorile ficatului (șobolan și șoarece), testiculele și celulele granulare ale tractului genital feminin (șobolan) au fost induse la animalele tratate. Apariția tumorilor hepatice a fost cel mai probabil o consecință a inducerii enzimelor hepatice microsomale, efect inductiv care, deși nu poate fi exclus, este slab sau absent la pacienții tratați cu Tolep. Tumorile testiculare ar fi putut fi induse de concentrații mari de luteinizare Deoarece această creștere nu se găsește la om, se crede că aceste tumori nu au nicio relevanță clinică. În studiul de carcinogenitate efectuat cu MHD la șobolani, a fost observată o creștere legată de doză a incidenței tumorilor cu celule granulare ale tractului genital feminin (colul uterin și vagin). Aceste efecte s-au produs la niveluri de expunere comparabile cu cele așteptate în practică. de dezvoltare a acestor tumori nu a fost elucidată, prin urmare nu se cunoaște semnificația clinică a acestor tumori.
06.0 INFORMAȚII FARMACEUTICE
06.1 Excipienți
Silice coloidală anhidră, celuloză microcristalină, hipromeloză, oxid de fier roșu, oxid de fier galben, stearat de magneziu, carmeloză sodică.
06.2 Incompatibilitate
Nu stie nimeni.
06.3 Perioada de valabilitate
3 ani.
06.4 Precauții speciale pentru depozitare
Acest medicament nu necesită condiții speciale de păstrare.
06.5 Natura ambalajului imediat și conținutul ambalajului
Blistere netoxice din PVC sau PVC / PCTFE
Cutie cu 50 de comprimate divizibile de 300 mg.
Cutie cu 50 de comprimate divizibile de 600 mg.
06.6 Instrucțiuni de utilizare și manipulare
Fără instrucțiuni speciale.
07.0 DEȚINĂTORUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
Novartis Farma S.p.A.
Largo Umberto Boccioni, 1 - 21040 Origgio (VA)
08.0 NUMĂRUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
TOLEP 300 mg comprimate - 50 comprimate divizibile A.I.C. n.: 028304018
TOLEP 600 mg comprimate - 50 comprimate divizibile A.I.C. n.: 028304020
09.0 DATA PRIMEI AUTORIZAȚII SAU REÎNNOIREA AUTORIZAȚIEI
Prima autorizație: 31.10.1994
Reînnoire: 15.11.2009
10.0 DATA REVIZUIRII TEXTULUI
Determinarea AIFA din 04.04.2014