Ingrediente active: Ticagrerol
Brilique 90 mg comprimate filmate
De ce se utilizează Brilique? Pentru ce este?
Ce este Brilique
Brilique conține substanța activă numită ticagrelor, care aparține unui grup de medicamente numite agenți antiplachetari.
Cum funcționează Brilique
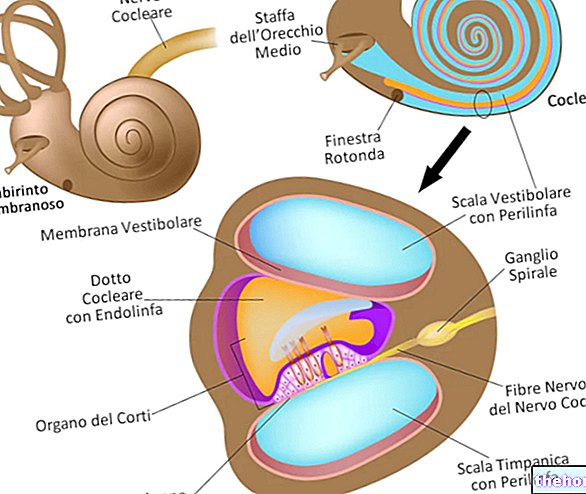
Brilique funcționează pe celule numite „trombocite” (numite și trombocite). Aceste celule foarte mici din sânge ajută la oprirea sângerării prin aglomerarea dintre ele pentru a închide găurile mici din vasele de sânge tăiate sau deteriorate.
Cu toate acestea, trombocitele pot forma și cheaguri în vasele de sânge bolnave ale inimii și creierului. Acest lucru poate fi foarte periculos deoarece:
- cheagul poate întrerupe complet aportul de sânge - acest lucru poate provoca un atac de cord (infarct miocardic) sau accident vascular cerebral, sau
- cheagul poate bloca parțial vasele de sânge care alimentează inima - acest lucru reduce fluxul de sânge către inimă și poate provoca dureri toracice care vin și pleacă (numită „angina instabilă”). Brilique ajută la blocarea aglomerării trombocitelor, ceea ce reduce posibilitatea formării unui cheag de sânge care poate reduce fluxul de sânge.
Pentru ce este Brilique
Brilique în combinație cu acid acetilsalicilic (un alt agent antiplachetar) trebuie utilizat numai la pacienții adulți.
I s-a prescris Brilique pentru că avea:
- un atac de cord, sau
- angină instabilă (angină sau durere toracică care nu este bine controlată).
Brilique reduce șansele de a avea un alt atac de cord sau accident vascular cerebral sau de a muri din cauza bolii legate de inimă sau vasele de sânge.
Contraindicații Când nu trebuie utilizat Brilique
Nu luați Brilique dacă:
- Sunteți alergic la ticagrelor sau la oricare dintre celelalte componente ale Brilique
- Are sângerări continue
- A avut un accident vascular cerebral cauzat de sângerări la nivelul creierului.
- Aveți probleme hepatice moderate până la severe.
- Luați unul dintre următoarele medicamente: ketoconazol (utilizat pentru tratarea infecțiilor fungice), claritromicină (utilizată pentru tratarea infecțiilor bacteriene), nefazodonă (un antidepresiv), ritonavir și atazanavir (utilizat pentru tratarea infecției cu HIV și SIDA).
Nu luați Brilique dacă oricare dintre cele de mai sus vi se aplică. Dacă nu sunteți sigur, discutați cu medicul sau farmacistul înainte de a lua Brilique
Precauții pentru utilizare Ce trebuie să știți înainte de a lua Brilique
Înainte de a lua Brilique, adresați-vă medicului dumneavoastră, farmacistului sau dentistului dacă:
- Aveți un risc crescut de sângerare din cauza:
- o vătămare gravă recentă
- o intervenție chirurgicală recentă (inclusiv chirurgie dentară)
- o boală care afectează coagularea sângelui - sângerări recente din stomac sau intestine (de exemplu, din cauza ulcerului gastric sau a „polipilor” colonului)
- Aveți de gând să aveți o intervenție chirurgicală (inclusiv munca dentară) în orice moment în timp ce luați Brilique, deoarece există un risc crescut de sângerare. Medicul dumneavoastră vă poate spune să încetați să luați Brilique cu 7 zile înainte de operație.
- Ritmul cardiac este neobișnuit de scăzut (de obicei mai puțin de 60 de bătăi pe minut) și nu ați implantat deja un instrument care reglează ritmul inimii (stimulator cardiac).
- Aveți astm sau o altă problemă pulmonară sau dificultăți de respirație.
- A făcut deja analize de sânge care au arătat mai mult acid uric decât în mod normal. Dacă oricare dintre cele de mai sus vi se aplică (sau dacă nu sunteți sigur), discutați cu medicul dumneavoastră, farmacistul sau dentistul înainte de a lua Brilique.
Copii și adolescenți
Brilique nu este recomandat copiilor și adolescenților cu vârsta sub 18 ani.
Interacțiuni Ce medicamente sau alimente pot schimba efectul Brilique
Spuneți medicului dumneavoastră sau farmacistului dacă luați, ați luat recent sau s-ar putea să luați orice alte medicamente. Acest lucru se datorează faptului că Brilique poate afecta modul în care funcționează unele medicamente, iar unele medicamente pot avea un efect asupra Brilique.
Spuneți medicului dumneavoastră sau farmacistului dacă luați oricare dintre următoarele medicamente:
- mai mult de 40 mg pe zi de simvastatină sau lovastatină (medicamente utilizate pentru tratamentul colesterolului ridicat)
- rifampicină (un antibiotic), fenitoină, carbamazepină și fenobarbital (utilizate pentru controlul convulsiilor), digoxină (utilizată pentru tratamentul insuficienței cardiace), ciclosporină (utilizată pentru scăderea apărării corpului), chinidină și diltiazem (utilizate pentru tratarea insuficienței cardiace) ritm cardiac anormal ), beta-blocante și verapamil (utilizate pentru tratamentul hipertensiunii arteriale).
Spuneți în special medicului dumneavoastră sau farmacistului dacă luați oricare dintre următoarele medicamente care cresc riscul de sângerare:
- „anticoagulante orale” denumite adesea „diluanți ai sângelui”, care includ warfarina.
- medicamente antiinflamatoare nesteroidiene (prescurtate ca AINS), utilizate adesea ca analgezice, cum ar fi ibuprofenul și naproxenul.
- inhibitori selectivi ai recaptării serotoninei (prescurtat ca SSRI) luați ca antidepresive, cum ar fi paroxetina, sertralina și citalopramul.
- alte medicamente precum ketoconazol (utilizat pentru tratarea infecțiilor fungice), claritromicină (utilizată pentru tratarea infecțiilor bacteriene), nefazodonă (un antidepresiv), ritonavir și atazanavir (utilizate pentru tratarea infecției cu HIV și SIDA), cisapridă (utilizată pentru tratarea arsurilor la stomac) sau ergot alcaloizi (utilizați pentru tratarea migrenelor și durerilor de cap).
De asemenea, spuneți medicului dumneavoastră că, deoarece luați Brilique, este posibil să aveți un risc crescut de sângerare dacă medicul dumneavoastră vă prescrie fibrinolitice, adesea numite „trombolitice”, cum ar fi streptokinaza sau alteplaza.
Avertismente Este important să știm că:
Sarcina și alăptarea
Utilizarea Brilique nu este recomandată dacă sunteți gravidă sau suspectați o sarcină. Femeile ar trebui să utilizeze metode contraceptive adecvate pentru a evita să rămână gravide în timp ce luați acest medicament. Discutați cu medicul dumneavoastră înainte de a lua Brilique dacă alăptați. Medicul dumneavoastră va discuta cu dvs. beneficiile și riscurile tratamentului Brilique în acest timp.
Dacă sunteți gravidă sau alăptați, credeți că ați putea fi gravidă sau intenționați să aveți un copil, adresați-vă medicului dumneavoastră sau farmacistului pentru recomandări înainte de a lua acest medicament.
Conducerea vehiculelor și utilizarea utilajelor
Este puțin probabil ca Brilique să vă afecteze capacitatea de a conduce vehicule sau de a folosi utilaje. Dacă vă simțiți amețit în timp ce luați Brilique, aveți grijă în timp ce conduceți vehicule sau folosiți utilaje
Doză, metodă și timp de administrare Cum se utilizează Brilique: Doze
Luați întotdeauna acest medicament exact așa cum v-a spus medicul sau farmacistul. Dacă aveți dubii, consultați medicul sau farmacistul.
Cât Brilique să iei
- Doza inițială este de două comprimate odată (doza de încărcare de 180 mg). Această doză vă va fi administrată în mod normal în spital.
- După această doză inițială, doza uzuală este de un comprimat de 90 mg de două ori pe zi timp de până la 12 luni, cu excepția cazului în care medicul dumneavoastră vă spune altfel. Luați Brilique aproximativ la aceeași oră în fiecare zi (de exemplu, un comprimat dimineața și unul seara).
De obicei, medicul dumneavoastră vă va spune să luați și acid acetilsalicilic. Aceasta este o substanță care se găsește în multe medicamente utilizate pentru a preveni coagularea sângelui. Medicul dumneavoastră vă va spune cât trebuie să luați (de obicei între 75 și 150 mg pe zi).
Cum să luați Brilique
- Puteți lua comprimatul cu sau fără mese.
- puteți verifica când ați luat ultimul comprimat Brilique uitându-vă la blister. Există un soare (pentru dimineață) și o lună (pentru seară). Acest lucru vă va spune dacă ați luat doza.
Dacă aveți dificultăți la înghițirea comprimatului (tabletelor)
Dacă aveți dificultăți la înghițirea comprimatului (tabletelor), îl puteți zdrobi și amesteca cu apă după cum urmează:
- Zdrobiți tableta (tabletele) într-o pulbere fină
- Se toarnă pudra într-o jumătate de pahar de apă
- Se amestecă și se bea imediat
- Pentru a vă asigura că nu ați lăsat niciun medicament, clătiți paharul gol cu o jumătate de pahar de apă și beți.
Supradozaj Ce trebuie făcut dacă ați luat prea mult Brilique
Dacă luați mai mult Brilique decât ar trebui
Dacă ați luat mai mult Brilique decât trebuie, contactați-vă medicul sau mergeți imediat la spital.Luați pachetul cu medicamente cu dvs. Este posibil să aveți un risc crescut de sângerare.
Dacă uitați să luați Brilique
- Dacă uitați să luați o doză, luați doza următoare, ca de obicei.
- Nu luați o doză dublă (două doze în același timp) pentru a compensa doza uitată.
Dacă încetați să luați Brilique
Nu încetați să luați Brilique fără să discutați mai întâi cu medicul dumneavoastră. Luați Brilique în mod regulat și atâta timp cât vi-l prescrie medicul.
Dacă încetați să luați Brilique, acest lucru poate crește șansele de a avea un alt atac de cord sau accident vascular cerebral sau de a muri de o boală legată de probleme ale inimii sau vaselor de sânge.
Dacă aveți orice întrebări suplimentare cu privire la acest medicament, adresați-vă medicului dumneavoastră sau farmacistului
Efecte secundare Care sunt efectele secundare ale Brilique
Ca toate medicamentele, acest medicament poate provoca reacții adverse, deși nu apar la toate persoanele.
Următoarele reacții adverse pot apărea cu acest medicament:
Consultați imediat un medic dacă observați oricare dintre următoarele simptome - este posibil să aveți nevoie de asistență medicală urgentă:
- Sângerarea în creier sau în interiorul craniului este un efect secundar neobișnuit și poate provoca semne de accident vascular cerebral, cum ar fi:
- amorțeală bruscă sau slăbiciune în brațe, picioare sau față, mai ales dacă este doar pe o parte a corpului
- confuzie bruscă, dificultăți de vorbire sau înțelegere a celorlalți
- dificultăți bruște la mers sau pierderea echilibrului sau coordonării - amețeli bruște sau cefalee intensă bruscă, fără o cauză cunoscută
- Sângerări - unele sângerări sunt frecvente. Cu toate acestea, sângerarea severă nu este un lucru obișnuit, dar poate pune viața în pericol. Pot fi crescute diferite tipuri de sângerări, cum ar fi:
- sângerări severe sau care nu pot fi controlate
- sângerări neașteptate sau sângerări care durează mult
- prezența sângelui în urină
- producerea de scaune negre sau sânge roșu în scaun
- tulburări vizuale cauzate de prezența sângelui în ochi
- eliberarea cheagurilor de sânge prin tuse sau vărsături
- sângerări în interiorul articulațiilor, rezultând umflături și durere
Adresați-vă medicului dumneavoastră dacă observați oricare dintre următoarele simptome:
- Senzație de respirație scurtă - această apariție este frecventă. Poate fi din cauza bolilor de inimă sau a unei alte cauze sau poate fi un efect secundar al Brilique. Dacă șuieratul se înrăutățește sau durează în timp, spuneți medicului dumneavoastră. Medicul dumneavoastră va decide dacă aveți nevoie de tratament sau veți continua cu investigații suplimentare .
Alte posibile efecte secundare
Frecvente (pot afecta până la 1 din 10 persoane)
- Vânătaie
- Sângerarea nasului
- Sângerări mai abundente din cauza intervențiilor chirurgicale, tăieturi sau răni
Mai puțin frecvente (pot afecta până la 1 din 100 de persoane)
- Reacție alergică - erupții cutanate, mâncărime sau umflarea feței sau a buzelor / limbii pot fi semne ale unei reacții alergice
- Durere de cap
- Senzație de amețeală sau de parcă camera se învârte
- Durere abdominală
- Diaree sau indigestie
- Senzație sau stare de rău
- Eczemă
- Mâncărime
- Inflamația stomacului (gastrită)
- Sângerări vaginale care sunt mai intense sau care apar în alte momente decât sângerarea menstruală normală
- Sângerări de pe pereții stomacului (ulcer)
- Sângerarea gingiilor
Rare (pot afecta până la 1 din 1000 de persoane)
- Constipație
- Senzație de furnicături
- confuzie
- Sânge în urechi
- Hemoragie internă
Raportarea efectelor secundare
Dacă manifestați orice reacții adverse, adresați-vă medicului dumneavoastră sau farmacistului, inclusiv orice reacții adverse posibile care nu sunt enumerate în acest prospect. De asemenea, puteți raporta reacțiile adverse direct prin intermediul sistemului național de raportare enumerat în Anexa V.
Raportând reacțiile adverse, puteți contribui la furnizarea mai multor informații despre siguranța acestui medicament.
Expirare și reținere
Nu utilizați acest medicament după data de expirare înscrisă pe blister și cutie după abrevierea EXP / EXP. Data de expirare se referă la ultima zi a lunii respective. Nu aruncați niciun medicament pe calea apei uzate sau a deșeurilor menajere. Întrebați farmacistul cum să aruncați medicamentele pe care nu le mai utilizați. Acest lucru va ajuta la protejarea mediului.
Conținutul pachetului și alte informații
Ce conține Brilique
- Ingredientul activ este ticagrelor. Fiecare comprimat filmat conține 90 mg ticagrelor.
- Celelalte ingrediente sunt:
Miezul tabletei: manitol (E421), hidrogen fosfat de calciu dihidrat, amidon glicolat de sodiu, hidroxipropilceluloză (E463), stearat de magneziu (E470b)
Acoperire tablete: hipromeloză (E464), dioxid de titan (E171), talc, polietilen glicol 400 și oxid galben de fier (E172).
Descrierea aspectului Brilique și conținutul ambalajului
Comprimat filmat (comprimat): Comprimatele sunt rotunde, biconvexe, galbene, filmate, marcate cu „90” peste un „T” pe o față.
Brilique este disponibil în:
- blister standard (cu simboluri soare / lună) în cutii de 60 și 180 de tablete
- blister calendaristic (cu simboluri soare / lună) în cutii de 14, 56 și 168 tablete
- blistere perforate monodozate într-o cutie de 100x1 comprimate.
Este posibil ca nu toate mărimile de ambalaj să fie comercializate.
Prospect sursă: AIFA (Agenția italiană pentru medicamente). Conținut publicat în ianuarie 2016. Este posibil ca informațiile prezente să nu fie actualizate.
Pentru a avea acces la cea mai actualizată versiune, este recomandabil să accesați site-ul web AIFA (Agenția italiană pentru medicamente). Declinare de responsabilitate și informații utile.
01.0 DENUMIREA PRODUSULUI MEDICAMENTAL
COMPRIMATE BRILIQUE 90 MG ÎMPĂRTATE CU FILM
02.0 COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ
Fiecare comprimat filmat conține 90 mg ticagrelor.
Pentru lista completă a excipienților, vezi secțiunea 6.1.
03.0 FORMA FARMACEUTICĂ
Comprimat filmat (comprimat).
Comprimate rotunde, biconvexe, galbene, marcate cu „90” peste un „T” pe o parte și simple pe cealaltă parte.
04.0 INFORMAȚII CLINICE
04.1 Indicații terapeutice
Brilique, administrat concomitent cu acid acetilsalicilic (ASA), este indicat pentru prevenirea evenimentelor aterotrombotice la pacienții adulți cu sindrom coronarian acut (angină instabilă, infarct miocardic cu creștere a segmentului non-ST [NSTEMI] sau infarct miocardic cu creștere a segmentului ST [STEMI] ), incluzând pacienții tratați farmacologic și cei supuși intervenției coronariene percutanate (PCI) sau grefei de bypass a arterei coronare (CABG).
Pentru informații suplimentare, vă rugăm să consultați punctul 5.1.
04.2 Doze și mod de administrare
Dozare
Tratamentul cu Brilique trebuie început cu o singură doză de încărcare de 180 mg (două comprimate de 90 mg) și apoi continuat cu 90 mg de două ori pe zi.
Pacienții tratați cu Brilique trebuie, de asemenea, să ia ASA zilnic, cu excepția cazului în care este contraindicat în mod specific. După o doză inițială de ASA, Brilique trebuie administrat cu o doză de întreținere de ASA între 75 și 150 mg (vezi pct. 5.1).
Tratamentul este recomandat până la 12 luni, cu excepția cazului în care întreruperea tratamentului cu Brilique este indicată clinic (vezi pct. 5.1). Experiența de peste 12 luni este limitată.
La pacienții cu sindrom coronarian acut (SCA), întreruperea prematură a oricărei terapii antiplachetare, inclusiv cea cu Brilique, ar putea duce la un risc crescut de deces cardiovascular sau infarct miocardic din cauza bolii de bază a pacientului. Prin urmare, trebuie evitată întreruperea prematură a tratamentului.
De asemenea, trebuie evitate întreruperile în continuitatea tratamentului. Pacientul care ratează o doză de Brilique trebuie să ia doar un comprimat de 90 mg (următoarea doză) la ora programată.
Dacă este necesar, pacienții tratați cu clopidogrel pot fi trecuți direct la Brilique (vezi pct. 5.1). Trecerea de la prasugrel la Brilique nu a fost studiată.
Populații speciale
Persoane în vârstă
Nu este necesară ajustarea dozei la pacienții vârstnici (vezi pct. 5.2).
Pacienți cu insuficiență renală
Nu este necesară ajustarea dozei la pacienții cu insuficiență renală (vezi pct. 5.2). Nu sunt disponibile informații cu privire la tratamentul pacienților dializați și, prin urmare, Briliquen nu este recomandat la acești pacienți.
Pacienți cu funcție hepatică afectată
Brilique nu a fost studiat la pacienții cu insuficiență hepatică moderată sau severă. Prin urmare, la pacienții cu insuficiență hepatică moderată până la severă, utilizarea acestuia este contraindicată (vezi pct. 4.3, 4.4 și 5.2). Nu este necesară ajustarea dozei la pacienții cu insuficiență hepatică ușoară.
Populația pediatrică
Siguranța și eficacitatea Brilique la copii cu vârsta sub 18 ani pentru indicațiile aprobate la adulți nu au fost stabilite. Nu există date disponibile.
Mod de administrare
Pentru uz oral.
Brilique poate fi administrat în timpul meselor sau între mese.
Pentru pacienții care nu pot înghiți comprimatul (tabletele) întregi, comprimatele Brilique pot fi zdrobite într-o pulbere fină, amestecate în jumătate de pahar de apă și băute imediat. Paharul trebuie clătit cu o jumătate de pahar suplimentar. D "apă și conținutul beat. Amestecul poate fi administrat și printr-un tub nazogastric (CH8 sau mai mare). După administrarea amestecului, este important să se irige tubul nazogastric cu apă.
04.3 Contraindicații
• Hipersensibilitate la substanța activă sau la oricare dintre excipienții enumerați la pct. 6.1 (vezi pct. 4.8).
• Sângerări patologice în curs.
• Antecedente de hemoragie intracraniană (vezi pct. 4.8).
• Insuficiență hepatică moderată până la severă (vezi pct. 4.2, 4.4 și 5.2).
• Administrarea concomitentă de ticagrelor cu inhibitori puternici ai CYP3A4 (de exemplu, ketoconazol, claritromicină, nefazodonă, ritonavir și atazanavir) este contraindicată, deoarece administrarea concomitentă poate duce la o creștere substanțială a expunerii la ticagrelor (vezi pct. 4.5).
04.4 Avertismente speciale și precauții adecvate pentru utilizare
Risc de sângerare
În studiul clinic de fază pivot 3 (PLATO [Inhibiția PLATelet și rezultatele pacientului], 18.624 pacienți), principalele criterii de excludere includeau un risc crescut de sângerare, trombocitopenie sau anemie relevantă clinic, sângerări intracraniene anterioare, sângerări gastro-intestinale în ultimele 6 luni sau chirurgie majoră în ultimele 30 de zile. Pacienții cu sindrom coronarian acut tratați cu Brilique și ASA au prezentat un risc crescut de sângerare majoră care nu este legată de CABG și mai general de sângerare care a necesitat supraveghere medicală, adică sângerări majore + minore conform criteriilor PLATO, dar nu sângerări fatale sau cele care au fost de viață - amenințare (vezi pct. 4.8).
Prin urmare, utilizarea Brilique la pacienții cu risc crescut cunoscut de sângerare ar trebui să fie echilibrată cu beneficiul în ceea ce privește prevenirea evenimentelor aterotrombotice. Dacă este indicat clinic, Brilique trebuie utilizat cu precauție în următoarele grupuri de pacienți:
• Pacienți cu predispoziție la sângerare (de exemplu datorită traumei recente, intervenții chirurgicale recente, tulburări de sângerare, sângerări gastrointestinale active sau recente). Utilizarea Brilique este contraindicată la pacienții cu sângerări patologice active, la cei cu antecedente de hemoragie intracraniană și la pacienții cu insuficiență hepatică moderată până la severă (vezi pct. 4.3).
• Pacienți cu administrare concomitentă de medicamente care pot crește riscul de sângerare (de exemplu, antiinflamatoare nesteroidiene (AINS), anticoagulante orale și / sau fibrinolitice) în 24 de ore de la administrarea dozei de Brilique.
Nu există date cu ticagrelor cu privire la un beneficiu hemostatic al transfuziilor de trombocite; cantitatea circulantă de ticagrelor poate inhiba trombocitele transfuzate. Deoarece administrarea concomitentă de ticagrelor și desmopresină nu a scăzut timpul de sângerare standard, este puțin probabil ca desmopresina să fie eficientă în tratamentul clinic al evenimentelor de sângerare (vezi pct. 4.5).
Terapia antifibrinolitică (acid aminocaproic sau acid tranexamic) și / sau factorul recombinant VIIa pot crește hemostaza.Ticagrelor poate fi reluat odată ce cauza sângerării a fost identificată și controlată.
Intervenții chirurgicale
Pacienții trebuie sfătuiți să informeze medicii și stomatologii că iau Brilique înainte de a programa orice intervenție chirurgicală și înainte de a lua orice medicament nou.
Dintre pacienții cu PLATO supuși unei intervenții chirurgicale de altoire a bypass-ului arterial coronarian (CABG), brațul Brilique a avut mai multe sângerări decât clopidogrelul când tratamentul a fost oprit în decurs de o zi înainte de operație, dar o rată similară de sângerare majoră comparativ cu clopidogrelul când terapia a fost oprită 2 sau mai multe zile înainte de operație (vezi pct. 4.8). Dacă un pacient urmează să fie supus unei intervenții chirurgicale elective și nu este dorit un efect antiplachetar, Brilique trebuie întrerupt cu 7 zile înainte de intervenția chirurgicală (vezi pct. 5.1).
Pacienți cu risc de evenimente de bradicardie
În urma observațiilor unor pauze ventriculare majoritar asimptomatice într-un studiu clinic anterior, pacienții cu risc crescut de evenimente de bradicardie (de exemplu, pacienți fără stimulator cardiac cu sindrom sinusal bolnav, bloc AV de gradul 2 sau 3 sau sincopă legată de bradicardie) au fost excluși din PLATO pivot studiu evaluând siguranța și eficacitatea ticagrelor. Prin urmare, având în vedere experiența clinică limitată, ticagrelor trebuie utilizat cu precauție la acești pacienți (vezi pct. 5.1).
În plus, trebuie administrată precauție atunci când se administrează ticagrelor concomitent cu medicamente cunoscute ca inducând bradicardie. Cu toate acestea, în studiul PLATO nu s-au observat dovezi relevante din punct de vedere clinic ale reacțiilor adverse după administrarea concomitentă cu unul sau mai multe medicamente cunoscute ca inducând bradicardie (de ex. 96% beta-blocante, 33% blocante ale canalelor de calciu diltiazem și verapamil și 4% digoxină) ( vezi pct. 4.5).
În timpul studiului PLATO Holter de monitorizare, mai mulți pacienți au prezentat pauze ventriculare ≥ 3 secunde cu ticagrelor decât cu clopidogrel în timpul fazei acute a SCA. Creșterea pauzelor ventriculare observate la Holter cu ticagrelor a fost mai mare la pacienții cu insuficiență cardiacă cronică (CHF) decât la populația totală din studiu în faza acută a SCA, dar nu după o lună la ticagrelor sau în comparație cu clopidogrel. Nu au existat consecințe clinice adverse asociate cu acest dezechilibru (inclusiv sincopă sau aplicarea stimulatorului cardiac) la această populație de pacienți (vezi pct. 5.1).
Dispnee
Episoade de dispnee au fost raportate de 13,8% dintre pacienții tratați cu Brilique și de 7,8% dintre pacienții tratați cu clopidogrel. La 2,2% dintre pacienți, investigatorii au considerat dispneea ca fiind cauzal legată de tratamentul cu Brilique. Dispneea este de obicei de intensitate ușoară până la moderată și deseori se rezolvă fără a necesita întreruperea tratamentului. Pacienții cu astm / BPOC pot avea un risc crescut absolut de a dezvolta dispnee cu Brilique (vezi pct. 4.8). Ticagrelor trebuie utilizat cu precauție la pacienții cu antecedente. de astm bronșic și / sau BPOC. Mecanismul nu a fost elucidat. Dacă un pacient dezvoltă dispnee nouă, prelungită sau agravată, acest lucru trebuie investigat cu atenție și, dacă nu este tolerat, tratamentul cu Brilique trebuie întrerupt.
Creșterea creatininei
Nivelurile de creatinină pot crește în timpul tratamentului cu ticagrelor (vezi pct. 4.8). Mecanismul nu a fost clarificat. Funcția renală trebuie monitorizată după o lună și ulterior, în conformitate cu practica clinică standard, cu o atenție deosebită la pacienții cu vârsta ≥ 75 de ani, la pacienții cu insuficiență renală moderată / severă și la cei care primesc tratament concomitent cu antagoniști ai angiotensinei II.
Creșterea acidului uric
În studiul PLATO, pacienții care au luat ticagrelor au avut un risc mai mare de hiperuricemie decât cei care au primit clopidogrel (vezi pct. 4.8). Se recomandă precauție atunci când ticagrelor se administrează pacienților cu antecedente de hiperuricemie sau artrită gută.Ca măsură de precauție, nu se recomandă utilizarea ticagrelor la pacienții cu nefropatie cu acid uric.
Alte
Pe baza relației observate în studiul PLATO între doza de întreținere a ASA și eficacitatea relativă a ticagrelor în comparație cu clopidogrel, nu se recomandă administrarea concomitentă de ticagrelor și doze mari de întreținere de ASA (> 300 mg) (vezi pct. 5.1).
04.5 Interacțiuni cu alte medicamente și alte forme de interacțiune
Ticagrelor este în primul rând un substrat al CYP3A4 și un inhibitor ușor al CYP3A4. Ticagrelor este, de asemenea, un substrat al glicoproteinei P (P-gp) și un inhibitor slab al P-gp și poate crește expunerea la substraturile P-gp.
Efectele altor medicamente asupra Brilique
Produse medicamentoase metabolizate de CYP3A4
Inhibitori ai CYP3A4
• Inhibitori puternici ai CYP3A4 - Administrarea concomitentă de ketoconazol și ticagrelor a crescut Cmax și ASC ticagrelor cu 2,4 și respectiv 7,3 ori. Cmax și ASC ale metabolitului activ au fost reduse cu 89% și respectiv 56%. Alți inhibitori puternici ai CYP3A4 (claritromicină, nefazodonă, ritonavir și atazanavir) pot produce efecte similare și, prin urmare, este contraindicată utilizarea concomitentă a inhibitorilor puternici ai CYP3A4 cu Brilique (vezi secțiunile 4.3).
• Inhibitori moderati ai CYP3A4 - Administrarea concomitenta de diltiazem si ticagrelor a crescut Cmaxul ticagrelor cu 69% si ASC de 2,7 ori si a scazut Cmax al metabolitului activ cu 38%, in timp ce ASC a fost neschimbata. Nu există niciun efect al ticagrelor asupra nivelurilor plasmatice ale diltiazemului. Alți inhibitori moderate ai CYP3A4 (de exemplu amprenavir, aprepitant, eritromicină și fluconazol) pot produce un efect similar și pot fi administrați împreună cu Brilique.
Inductori CYP3A
Administrarea concomitentă de rifampicină și ticagrelor a scăzut Cmax și ASC ale ticagrelor cu 73%, respectiv 86%. Cmaxul metabolitului activ a fost neschimbat, iar ASC a fost redusă cu 46%, respectiv. Alți inductori ai CYP3A (de exemplu fenitoină, carbamazepină și fenobarbital) pot reduce expunerea la ticagrelor. Administrarea concomitentă de ticagrelor cu inductori puternici ai CYP3A poate reduce expunerea și eficacitatea la ticagrelor, prin urmare utilizarea lor concomitentă cu Brilique nu este recomandată.
Ciclosporină (inhibitor al P-gp și CYP3A)
Administrarea concomitentă de ciclosporină (600 mg) și ticagrelor a crescut Cmax și ASC ale ticagrelor de 2,3 ori respectiv 2,8 ori. ASC a metabolitului activ a crescut cu 32% și Cmax a scăzut. 15% în prezența ciclosporină.
Nu există date privind utilizarea concomitentă a ticagrelor cu alte substanțe active care sunt, de asemenea, inhibitori puternici ai glicoproteinei P (P-gp) și inhibitori moderati ai CYP3A4 (de exemplu, verapamil, chinidină) care pot determina, de asemenea, o expunere crescută la ticagrelor. Dacă această asociere nu poate fi evitată, utilizarea lor concomitentă trebuie făcută cu prudență.
Alții
Studiile clinice de interacțiune medicamentoasă au arătat că administrarea concomitentă de ticagrelor cu heparină, enoxaparină și ASA sau desmopresină nu a avut niciun efect asupra profilului farmacocinetic al ticagrelor sau al metabolitului activ sau asupra agregării plachetare induse de ADP comparativ cu ticagrelor în monoterapie. că hemostaza alterată trebuie utilizată cu precauție în asociere cu ticagrelor.
S-a observat o creștere de două ori a expunerii la ticagrelor după consumul zilnic de cantități mari de suc de grapefruit (3 x 200 ml) pe zi. Această amploare a creșterii expunerii nu este considerată a fi relevantă clinic la majoritatea pacienților. .
Efectele Brilique asupra altor medicamente
Produse medicamentoase metabolizate de CYP3A4
• Simvastatină - Administrarea concomitentă de ticagrelor și simvastatină a crescut C simvastatină cu 81% și ASC cu 56% și a dus la o creștere a C simvastatină-acid cu 64% și ASC cu 52%, cu unele creșteri individuale mai mari de 2 până la 3 ori. Administrarea concomitentă de doze de ticagrelor și simvastatină mai mari de 40 mg pe zi poate provoca efecte adverse datorate simvastatinei și trebuie cântărită în raport cu beneficiile potențiale. Nu a existat niciun efect al simvastatinei asupra nivelurilor plasmatice ale ticagrelor. Nu se recomandă utilizarea concomitentă de ticagrelor cu doze de simvastatină sau lovastatină mai mari de 40 mg.
• Atorvastatină - Administrarea concomitentă de atorvastatină și ticagrelor a crescut Cmaxul acidului atorvastatin cu 23% și ASC cu 36%. Creșteri similare ale ASC și Cmax au fost observate pentru toți metaboliții acidului atorvastatină. Aceste creșteri nu sunt considerate semnificative clinic.
• Nu poate fi exclus un efect similar asupra altor statine metabolizate de CYP3A4. Pacienții PLATO care au primit ticagrelor au luat o varietate de statine, fără o problemă de asociere cu siguranța statinelor la 93% din cohorta PLATO de pacienți care au luat aceste medicamente.
Ticagrelor este un inhibitor ușor al CYP3A4. Nu se recomandă administrarea concomitentă de substraturi de ticagrelor și CYP3A4 cu indici terapeutici scăzuti (de exemplu, cisapridă sau alcaloizi de ergot), deoarece ticagrelor poate crește expunerea la aceste medicamente.
Substraturi de glicoproteină P (P-gp) (inclusiv digoxină, ciclosporină)
Administrarea concomitentă de Brilique a crescut digoxina Cmax cu 75% și „ASC cu 28%. Nivelurile medii de digoxină„ în aval ”au crescut cu aproximativ 30% odată cu administrarea concomitentă de ticagrelor, cu creșteri individuale maxime de 2 ori în prezența digoxinei , Cmax și ASC ale ticagrelor și ale metabolitului său activ nu au fost afectate.
Prin urmare, se recomandă monitorizarea clinică și / sau de laborator adecvată atunci când se administrează medicamente cu un indice terapeutic scăzut dependent de P-gp, cum ar fi digoxina, concomitent cu ticagrelor.
Nu a existat niciun efect al ticagrelor asupra nivelului sanguin al ciclosporinei. Efectul ticagrelor asupra altor substraturi P-gp nu a fost studiat.
Medicamente metabolizate de CYP2C9
Administrarea concomitentă de ticagrelor cu tolbutamidă nu a determinat nicio modificare a concentrațiilor plasmatice ale ambelor medicamente, indicând faptul că ticagrelor nu este un inhibitor al CYP2C9 și este puțin probabil să afecteze metabolismul mediat de CYP2C9 al medicamentelor, cum ar fi warfarina și tolbutamida.
Contraceptive orale
Administrarea concomitentă de ticagrelor și levonorgestrel și etinilestradiol a crescut expunerea la etinilestradiol cu aproximativ 20%, dar nu a modificat profilul farmacocinetic al levonorgestrelului. Nu este de așteptat un efect relevant clinic asupra eficacității contraceptivelor orale după utilizarea concomitentă de levonorgestrel și etinilestradiol și ticagrelor.
Medicamente despre care se știe că induc bradicardie
După observarea majorității pauzelor ventriculare asimptomatice și a bradicardiei, trebuie administrată prudență atunci când se administrează Brilique concomitent cu alte medicamente care induc bradicardia (vezi pct. 4.4). Cu toate acestea, în studiul PLATO nu au fost observate dovezi ale reacțiilor adverse clinic semnificative după administrarea concomitentă. cu unul sau mai multe medicamente despre care se știe că induc bradicardie (de ex. 96% beta-blocante, 33% blocante ale canalelor de calciu diltiazem și verapamil și 4% digoxină).
Alte terapii concomitente
În studiul PLATO, Brilique a fost administrat în mod obișnuit cu ASA, inhibitori ai pompei de protoni, statine, blocante beta, inhibitori ai enzimei de conversie a angiotensinei și antagoniști ai receptorilor de angiotensină, așa cum este necesar în condiții clinice concomitente, pe termen lung și, de asemenea, cu heparină, moleculară scăzută greutate heparină și inhibitori intravenoși pe termen scurt de GpIIb / IIIa (vezi pct. 5.1) Nu au fost observate dovezi ale interacțiunilor adverse relevante clinic cu aceste medicamente.
Administrarea concomitentă de ticagrelor și heparină, enoxaparină sau desmopresină nu are niciun efect asupra timpului de tromboplastină parțială activată (aPTT), a timpului de coagulare activat (ACT) sau a dozelor de factor Xa. Cu toate acestea, datorită potențialelor interacțiuni farmacodinamice, trebuie administrată prudență atunci când se administrează concomitent Brilique cu medicamente despre care se știe că afectează hemostaza.
După raportarea unor anomalii ale sângerării cutanate cu ISRS (de exemplu, paroxetină, sertralină și citalopram), trebuie administrată precauție atunci când se administrează ISRS cu ticagrelor, deoarece acest lucru poate duce la un risc crescut de sângerare.
04.6 Sarcina și alăptarea
Femeile aflate la vârsta fertilă
Femeile aflate la vârsta fertilă trebuie să ia măsuri contraceptive adecvate pentru a evita o posibilă sarcină în timpul tratamentului cu Brilique.
Sarcina
Nu există date limitate sau sunt limitate cu privire la utilizarea ticagrelor la femeile gravide.
Studiile la animale au arătat toxicitate asupra funcției de reproducere (vezi pct. 5.3). Brilique nu este recomandat în timpul sarcinii.
Timp de hrănire
Datele farmacodinamice / toxicologice la animale au arătat excreția ticagrelor și a metaboliților săi activi în lapte (vezi pct. 5.3). Nu poate fi exclus un risc pentru nou-născuți / sugari. Trebuie luată o decizie dacă se întrerupe alăptarea sau alăptarea. Se întrerupe / se abține de la Terapia Brilique luând în considerare beneficiul alăptării pentru bebeluș și beneficiul terapiei pentru mamă.
Fertilitate
Ticagrelor nu are niciun efect asupra fertilității masculine sau feminine la animale (vezi pct. 5.3).
04.7 Efecte asupra capacității de a conduce vehicule și de a folosi utilaje
Brilique nu are nicio influență sau are o influență neglijabilă asupra capacității de a conduce vehicule sau de a folosi utilaje. Amețeli au fost raportate în timpul tratamentului sindromului coronarian acut. Din acest motiv, pacienții care prezintă amețeli trebuie să fie prudenți în timp ce conduc vehicule sau folosesc utilaje.
04.8 Efecte nedorite
Rezumatul profilului de siguranță
Cele mai frecvent raportate reacții adverse la pacienții tratați cu ticagrelor au fost dispneea, contuzia și epistaxisul, care au apărut la o incidență mai mare decât în grupul cu clopidogrel.
Tabelul reacțiilor adverse
Siguranța Brilique la pacienții cu sindrom coronarian acut (angină instabilă, NSTEMI și STEMI) a fost evaluată în studiul PLATO de mare fază pivot 3 ([PLATĂelet Inhibiție și pacient SAUrezultate], 18.624 de pacienți), care au comparat pacienții tratați cu Brilique (doza de încărcare de 180 mg de Brilique și doza de întreținere de 90 mg de două ori pe zi) și pacienții tratați cu clopidogrel (doza de încărcare de 300-600 mg urmată de 75 mg o dată pe zi ca o întreținere ambele administrate în asociere cu acid acetilsalicilic (ASA) și alte terapii standard.
Următoarele reacții adverse au fost identificate în urma studiilor efectuate cu Brilique sau au fost raportate în experiența după punerea pe piață (Tabelul 1).
Reacțiile adverse sunt clasificate în funcție de frecvență și clasa sistemelor de organe. Clasele de frecvență sunt definite în conformitate cu următoarele convenții: Foarte frecvente (≥1 / 10), Frecvente (≥1 / 100,
Terminologiile multiple ale reacțiilor adverse corelate au fost grupate împreună în Tabelul e
includeți termeni medicali descriși mai jos:
la hiperuricemie, creșterea acidului uric seric
b hemoragie cerebrală, hemoragie intracraniană, accident vascular cerebral hemoragic
c dispnee, dispnee din efort, dispnee în repaus, dispnee nocturnă
d hemoragie gastro-intestinală, hemoragie rectală, hemoragie intestinală, melaena, sânge ocult
și hemoragie de ulcer gastro-intestinal, hemoragie de ulcer gastric, hemoragie de ulcer duodenal, hemoragie de ulcer peptic
f hematom subcutanat, hemoragie cutanată, hemoragie subcutanată, petechii
g contuzie, hematom, vânătăi, tendință crescută la vânătăi, hematom traumatic
h hematurie, sânge în urină, hemoragie a tractului urinar
hemoragie la locul puncției, hematom la locul puncției vasculare, hemoragie la locul injecției, hemoragie la locul puncției, hemoragie la locul cateterului
# Nu au fost raportate reacții adverse de hemartroză în brațul ticagrelor (n = 9.235) în studiul PLATO; frecvența a fost calculată utilizând limita superioară a intervalului de încredere de 95% pentru estimarea punctuală (bazată pe 3 / X, unde X reprezintă eșantionul total, adică 9.235 de pacienți). Aceasta este calculată ca 3 / 9.235, ceea ce este egal cu „rare "clasa de frecvență
## Au fost raportate hemoragii intracraniene fatale în experiența ulterioară punerii pe piață
Descrierea reacțiilor adverse selectate
Sângerare
Rezultatele generale ale ratelor de sângerare din studiul PLATO sunt prezentate în Tabelul 2.
Tabelul 2 - Evaluarea Kaplan-Meier a ratelor de sângerare în funcție de tratament
Definiții ale categoriilor de sângerare:
Sângerări majore fatale / care pun viața în pericol: aparent clinic cu scăderea hemoglobinei> 50 g / l sau transfuzie ≥ 4 unități de celule roșii din sânge; sau fatală; sau intracranian; o intrapericardic cu tamponare cardiacă; sau cu șoc hipovolemic sau hipotensiune severă care necesită tratament hipertensiv sau intervenție chirurgicală.
Alte sângerări majore: aparent clinic cu scăderea hemoglobinei de 30-50 g / l sau transfuzie de 2-3 unități de celule roșii din sânge; saudezactivând semnificativ.
Sângerări minore: necesită intervenție medicală pentru a opri sau trata sângerarea.
Sângerări majore TIMI: aparent clinic cu scăderea hemoglobinei> 50 g / l sau hemoragie intracraniană.
Sângerări minore TIMI: aparent clinic cu scăderea hemoglobinei cu 30-50 g / l.
Brilique și clopidogrel nu diferă în ceea ce privește ratele de sângerare majoră fatală / care pune viața în pericol conform criteriilor PLATO, Sângerări totale majore conform criteriilor PLATO, Sângerări majore în conformitate cu scara TIMI sau Minore în conformitate cu scara TIMI (Tabelul 2) . Cu toate acestea, s-au produs mai multe sângerări combinate PLATO majore + minore cu ticagrelor decât cu clopidogrel. Puțini pacienți din studiul PLATO au prezentat sângerări fatale: 20 (0,2%) pentru ticagrelor și 23 (0,3%) pentru clopidogrel (vezi pct. 4.4).
Factori precum vârsta, sexul, greutatea, rasa, regiunea geografică, starea fizică concomitentă, terapia concomitentă și istoricul medical, inclusiv accidentul vascular cerebral anterior sau atacul ischemic tranzitor, nu au fost predictive pentru sângerări majore totale sau care nu au legătură cu procedurile, definite conform Criteriile PLATO. În consecință, niciun grup special nu a fost identificat cu risc pentru o anumită categorie de sângerare.
Sângerări legate de CABG: În studiul PLATO, 42% din 1.584 pacienți (12% din cohortă) supuși unei intervenții chirurgicale de altoire a bypass-ului coronarian (CABG) au avut sângerări majore fatale / care pun viața în pericol conform criteriilor PLATO, fără nicio diferență între grupurile de tratament. Sângerările fatale legate de CABG au apărut la 6 pacienți din fiecare grup de tratament (vezi pct. 4.4).
Sângerarea nu este legată de CABG și sângerarea nu este legată de nicio procedură: Brilique și clopidogrel nu diferă în sângerările majore fatale / care pun viața în pericol, care nu sunt legate de CABG, definite conform criteriilor PLATO, în timp ce sângerările majore totale în conformitate cu criteriile PLATO, majore în funcție de scala TIMI și Major + Minor în conformitate cu scala TIMI, au fost mai frecvente cu ticagrelor. În mod similar, la eliminarea sângerărilor legate de procedură, s-au observat mai multe sângerări la ticagrelor decât la clopidogrel (Tabelul 2). Întreruperea tratamentului din cauza sângerărilor non-procedurale a fost mai frecventă pentru ticagrelor (2,9%) decât pentru clopidogrel (1,2%; p
Hemoragia intracraniană: Au apărut mai multe sângerări intracraniene non-procedurale cu ticagrelor (n = 27 sângerări la 26 pacienți, 0,3%) decât cu clopidogrel (n = 14 sângerări, 0,2%), inclusiv 11 sângerări cu ticagrelor și 1 cu clopidogrel au avut un rezultat fatal. Nu au existat diferențe în sângerările fatale generale.
Dispnee
Dispneea, o senzație de scurtare a respirației, a fost raportată la pacienții tratați cu Brilique. Evenimente adverse dispnoice (EA) (dispnee, dispnee în repaus, dispnee la efort, dispnee nocturnă paroxistică și dispnee nocturnă), atunci când sunt asociate, au fost raportate de 13,8% dintre pacienții tratați cu ticagrelor și de 7,8% dintre pacienții tratați cu clopidogrel. La 2,2% dintre pacienții care au luat ticagrelor și la 0,6% dintre pacienții tratați cu clopidogrel, investigatorii au considerat dispneea ca fiind cauzal legată de tratament în studiul PLATO și câteva cazuri au fost severe (0,14% pentru ticagrelor; 0,02% pentru clopidogrel) (vezi pct. 4.4). Cele mai frecvent raportate simptome de dispnee au fost de intensitate ușoară până la moderată, iar cele mai multe au fost raportate ca un singur episod la scurt timp după inițierea tratamentului.
În comparație cu clopidogrel, pacienții cu astm / BPOC tratați cu ticagrelor pot avea un risc crescut de dispnee non-severă (3,29% pentru ticagrelor versus 0,53% pentru clopidogrel) și dispnee severă (0,38%). Pentru ticagrelor versus 0,00% pentru clopidogrel). În termeni absoluți, acest risc a fost mai mare decât populația generală a studiului PLATO. Ticagrelor trebuie administrat cu precauție pacienților cu antecedente de astm și / sau BPOC (vezi pct. 4.4).
Aproximativ 30% din toate episoadele de dispnee s-au rezolvat în decurs de 7 zile. Studiul PLATO a inclus pacienți care au avut insuficiență cardiacă congestivă, boli pulmonare obstructive cronice sau astm bronșic la momentul inițial; acești pacienți și vârstnicii au fost mai predispuși să raporteze episoade de dispnee. În grupul Brilique, 0,9% dintre pacienți au întrerupt substanța activă studiată din cauza dispneei, comparativ cu 0,1% dintre pacienții cărora li s-a administrat clopidogrel. Incidența mai mare a dispneei observată la Brilique nu este asociată cu debutul sau agravarea bolilor cardiace sau pulmonare (vezi pct. 4.4). Brilique nu afectează testele funcției pulmonare.
Testele de diagnostic
Creșteri ale creatininei: În studiul PLATO, concentrația serică a creatininei a crescut semnificativ cu mai mult de 30% la 25,5% dintre pacienții care au luat ticagrelor, comparativ cu 21,3% dintre pacienții care au luat clopidogrel și mai mult de 50% la pacienții care au luat ticagrelor. 8,3% dintre pacienții tratați cu ticagrelor comparativ cu 6,7% dintre pacienții tratați cu clopidogrel. Creșterea creatininei> 50% a fost mai pronunțată la pacienții cu vârsta peste 75 de ani (ticagrelor 13,6% față de clopidogrel 8,8%), la pacienții cu insuficiență renală severă la momentul inițial (ticagrelor 17,8% versus clopidogrel 12,5%) și la pacienții tratați concomitent cu antagoniști ai receptorilor angiontensinei II (ticagrelor 11,2% față de clopidogrel 7, 1%). În cadrul acestor subgrupuri, evenimentele adverse renale severe și evenimentele adverse care au condus la întreruperea studiului medicamentului au fost similare în cele două grupuri de tratament. Totalitatea evenimentelor adverse renale raportate a fost de 4,9% pentru ticagrelor versus 3,8% pentru clopidogrel, totuși un procent similar de pacienți a raportat evenimente considerate de anchetatori ca fiind direct cauzale tratamentului: 54 (0,6%) pentru ticagrelor și 43 (0,5%) pentru clopidogrel.
Creșteri ale acidului uric: în studiul PLATO, concentrațiile serice de acid uric au crescut peste limita superioară a normalului la 22% dintre pacienții tratați cu ticagrelor, comparativ cu 13% dintre pacienții care au luat clopidogrel. Concentrația medie a acidului uric a fost crescută cu aproximativ 15% ticagrelor comparativ cu 7,5% cu clopidogrel și a scăzut la aproximativ 7% cu ticagrelor după întreruperea tratamentului, în timp ce nu s-a observat nicio reducere cu clopidogrel. Evenimentul advers al hiperuricemiei a fost raportat la 0,5% pentru ticagrelor versus 0,2% pentru clopidogrel. Dintre aceste evenimente adverse, 0,05% pentru ticagrelor versus 0,02% pentru clopidogrel au fost considerate a fi legate de cauzalitatea îndreptată de investigator. Pentru artrita gutoasă, evenimentele adverse raportate au fost 0,2% pentru ticagrelor versus 0,1% pentru clopidogrel; niciunul dintre aceste evenimente adverse nu a fost considerat cauzal legat de tratament de către anchetatori.
Raportarea reacțiilor adverse suspectate
Raportarea reacțiilor adverse suspectate care apar după autorizarea medicamentului este importantă, deoarece permite monitorizarea continuă a raportului beneficiu / risc al medicamentului. Profesioniștii din domeniul sănătății sunt rugați să raporteze orice reacții adverse suspectate prin intermediul sistemului național de raportare. .agenziafarmaco.gov.it / it / responsabili ".
04.9 Supradozaj
Ticagrelor este bine tolerat în doze unice de până la 900 mg. Toxicitatea gastro-intestinală a fost limitată la doză într-un studiu de creștere a dozei unice. Alte reacții adverse relevante clinic care pot apărea după supradozaj includ dispneea și pauzele ventriculare (vezi pct. 4.8).
În caz de supradozaj, pot apărea reacțiile adverse potențiale de mai sus și trebuie luată în considerare monitorizarea ECG.
Până în prezent, nu există un antidot cunoscut care să contracareze efectele ticagrelor și se presupune că ticagrelor nu este dializabil (vezi pct. 4.4). Tratamentul supradozajului trebuie să respecte standardele practicii medicale locale. Efectul scontat al unei cantități prea mari de Brilique este prelungirea riscului de sângerare asociat cu inhibarea trombocitelor. Dacă apare sângerare, trebuie instituite măsuri medicale adecvate de susținere.
05.0 PROPRIETĂȚI FARMACOLOGICE
05.1 Proprietăți farmacodinamice
Grupa farmacoterapeutică: agenți antiplachetari, cu excepția heparinei.
Codul ATC: B01AC24.
Mecanism de acțiune
Brilique conține ticagrelor, care aparține clasei chimice a ciclopentiltriazolopirimidinelor
(CPTP), care este un antagonist al receptorului P2Y12 oral, direct, selectiv și reversibil și previne activarea și agregarea trombocitelor dependente de P2Y12 mediate de adenozin difosfat (ADP).
Ticagrelor nu împiedică legarea ADP, dar atunci când se leagă de receptorul P2Y12 previne transducția semnalului indusă de ADP. Deoarece trombocitele joacă un rol în apariția și / sau evoluția complicațiilor trombotice ale bolii aterosclerotice, s-a demonstrat că inhibarea funcției trombocitelor reduce riscul evenimentelor cardiovasculare, cum ar fi moartea, infarctul miocardic sau accidentul vascular cerebral.
Ticagrelor crește, de asemenea, nivelurile endogene locale de adenozină prin inhibarea transportorului echilibrant de nucleozide -1 (ENT-1).
S-a demonstrat că Ticagrelor crește următoarele efecte induse de adenozină la subiecții sănătoși și la pacienții cu SCA: vasodilatație (măsurată ca flux crescut de sânge coronarian la voluntari sănătoși și la pacienții cu SCA; cefalee), inhibarea funcției trombocitelor (în sângele uman întreg in vitro) și dispnee. Cu toate acestea, legătura dintre creșterea observată a adenozinei și rezultatele clinice (de exemplu, morbiditate-mortalitate) nu a fost elucidată.
Efecte farmacodinamice
Debutul acțiunii (Onset)
La pacienții cu boală coronariană stabilă tratați cu ASA, ticagrelor induce o apariție rapidă a efectului farmacologic, după cum se demonstrează printr-o „inhibiție a agregării plachetare (HAP) pentru ticagrelor, la 0,5 ore după o doză de încărcare de 180 mg. Aproximativ 41% cu o valoare maximă efect asupra HAP de 89% în 2-4 ore după administrarea dozei și menținut între 2 și 8 ore.90% dintre pacienți au avut HAP final> 70% în decurs de 2 ore după administrare.
Reversibilitatea acțiunii (Offset)
Dacă a fost planificată o procedură CABG, riscul de sângerare cu ticagrelor este crescut în comparație cu clopidogrel atunci când este oprit cu mai puțin de 96 de ore înainte de operație.
Date referitoare la schimbarea terapiei
Trecerea de la clopidogrel la ticagrelor are ca rezultat o creștere absolută a HAP de 26,4%, în timp ce trecerea de la ticagrelor la clopidogrel are ca rezultat o scădere absolută a HAP de 24,5%. Pacienții pot fi trecuți de la terapia cu clopidogrel la terapia cu ticagrelor fără a întrerupe efectul antiplachetar (vezi pct. 4.2).
Eficacitate și siguranță clinică
Studiul PLATO a inclus 18.624 de pacienți care au prezentat în termen de 24 de ore de la apariția simptomelor de angină pectorală instabilă (UA), infarct miocardic cu creștere a segmentului ST (NSTEMI) sau infarct miocardic cu creștere a segmentului ST (STEMI) și care au fost tratați inițial farmacologic, fie cu intervenție coronariană percutană (PCI), fie cu altoire de by-pass coronarian (CABG) (vezi secțiunea 4.1).
La aceeași doză zilnică de ASA, ticagrelor 90 mg de două ori pe zi au fost superioare clopidogrelului 75 mg / zi în prevenirea obiectivului compozit de deces cardiovascular [CV], infarct miocardic [IM] sau accident vascular cerebral, cu diferența ghidată de reducerea de decese CV și IM Pacienții au primit fie o doză de încărcare de 300 mg de clopidogrel (doză de 600 mg posibilă pentru PCI), fie ticagrelor de 180 mg.
Rezultatul a fost obținut devreme (reducerea riscului absolut [ARR] 0,6% și reducerea riscului relativ [RRR] cu 12% la 30 de zile), cu un efect de tratament care a rămas constant timp de 12 luni, obținându-se un "ARR" de 1,9% pe an și un RRR de 16%. Aceste date sugerează că este adecvat să se trateze pacienții cu ticagrelor timp de până la 12 luni (vezi pct. 4.2). ; tratamentul a 91 de pacienți ar evita moartea cu 1 CV (Tabelul 3).
Efectul tratamentului cu ticagrelor în comparație cu clopidogrelul este consistent în toate subgrupurile de pacienți în funcție de greutate, sex, antecedente de diabet zaharat, atac ischemic tranzitor sau accident vascular cerebral nehemoragic, revascularizare, terapii concomitente, inclusiv heparine, inhibitori de GpIIb / IIIa și pompă de protoni. inhibitori (vezi pct. 4.5), diagnosticul final al evenimentului (STEMI, NSTEMI sau UA) și calea tratamentului atribuită randomizării (invazivă sau medicală).
S-a observat o interacțiune slab semnificativă între tratament și regiunea geografică, prin care Hazard Ratio (HR) pentru obiectivul primar favorizează ticagrelor în restul lumii, în timp ce favorizează clopidogrelul în America de Nord, care reprezintă aproximativ 10%. populația studiată (valoarea p a interacțiunii = 0,045).
Analizele exploratorii sugerează o posibilă asociere cu doza de ASA, deoarece eficacitatea redusă a fost observată cu ticagrelor asociată cu creșterea dozelor de ASA. Doza cronică zilnică de ASA, administrată împreună cu Brilique, ar trebui să fie între 75 și 150 mg (vezi pct. 4.2 și 4.4) .
Figura 1 prezintă riscul estimat de prima apariție a oricărui eveniment evaluat în obiectivul final al eficacității compuse.
Brilique a redus apariția obiectivului primar compozit comparativ cu clopidogrel atât în populațiile UA / NSTEMI, cât și în STEMI (Tabelul 3).
Tabelul 3 - Rezultate clinice în studiul PLATO
a ARR = reducerea riscului absolut; RRR = reducerea riscului relativ = (1-Raport pericol) x 100%. Un RRR negativ indică un risc relativ crescut.
b excluzând infarctul miocardic tăcut.
c SRI = ischemie recidivantă severă; RI = ischemie recurentă; TIA = atac ischemic tranzitor; ATE = eveniment aterotrombotic. MI total include MI silențios, cu data evenimentului setată ca dată a diagnosticului.
d valoarea semnificației nominale; toate celelalte valori sunt semnificative din punct de vedere statistic, pe baza unui test ierarhic predefinit.
Substudiu Holter
Pentru a studia apariția pauzelor ventriculare și a altor episoade aritmice în timpul studiului PLATO, anchetatorii au efectuat monitorizarea Holter într-un subgrup de aproape 3.000 de pacienți, dintre care aproximativ 2.000 au înregistrat atât faza acută a sindromului coronarian. după o lună. Variabila primară de interes a fost debutul pauzelor ventriculare ≥3 secunde. Mai mulți pacienți au prezentat pauze ventriculare cu ticagrelor (6,0%) decât cu clopidogrel (3,5%) în faza acută; și, respectiv, 2,2% și 1,6% după o lună (vezi pct. 4.4). Creșterea pauzelor ventriculare în faza acută a SCA a fost mai pronunțată la pacienții tratați cu ticagrelor cu antecedente de CHF (9,2% față de 5,4% la pacienții fără antecedente de ICC; pentru pacienții tratați cu clopidogrel, 4, 0% la pacienți cu antecedente de CHF comparativ cu 3,6% la cei fără antecedente de CHF). Această diferență nu a fost observată după o lună: 2,0% față de 2,1% pentru pacienții tratați cu ticagrelor cu respectiv fără antecedente de CHF și 3,8% față de 1,4% Nu s-au găsit consecințe clinice adverse asociate cu această diferență (inclusiv aplicații de stimulator cardiac) la această populație de pacienți.
Substudiu genetic din studiul PLATO
Genotiparea CYP2C19 și ABCB1 a 10.285 de pacienți din studiul PLATO a permis asocierea rezultatelor clinice ale studiului cu distribuția genotipică. Superioritatea ticagrelor față de clopidogrel în reducerea evenimentelor cardiovasculare majore nu a fost afectată de genotipul pacientului CYP2C19 sau ABCB1. Similar cu datele generale din studiul PLATO, incidența sângerărilor majore totale după criteriile PLATO nu a diferit între ticagrelor și clopidogrel, indiferent de a genotipului CYP2C19 sau ABCB1. Incidența sângerărilor majore care nu au legătură cu PLATO au fost crescute cu ticagrelor comparativ cu clopidogrel la pacienții cu una sau mai multe alele cu funcție redusă CYP2C19, dar similar cu clopidogrelul la pacienții fără alele cu funcție redusă.
Asociere compozită de eficacitate și siguranță
Combinația compusă de eficacitate și siguranță (moarte CV, IM, accident vascular cerebral sau sângerare majoră totală PLATO) indică faptul că beneficiul eficacității Brilique față de clopidogrel nu este negat de evenimentele sângerării majore (ARR 1, 4%; RRR 8%; HR 0,92 ; p = 0,0257) în cele 12 luni următoare SCA.
Populația pediatrică
Agenția Europeană a Medicamentului a renunțat la obligația de a prezenta rezultatele studiilor efectuate cu Brilique la toate subseturile populației pediatrice în indicația autorizată (vezi secțiunile 4.2 și 5.2).
05.2 Proprietăți farmacocinetice
Ticagrelor prezintă farmacocinetică liniară și expunerea la ticagrelor și metabolitul activ (AR-C124910XX) sunt aproximativ proporționale cu doza până la 1.260 mg.
Absorbţie
Absorbția ticagrelor este rapidă, cu o medie t de aproximativ 1,5 ore. Formarea metabolitului principal circulant, AR-C124910XX (de asemenea activ), derivat din ticagrelor, este rapidă, cu o t
medie de aproximativ 2,5 ore. După administrarea orală de 90 mg ticagrelor în condiții de repaus alimentar, Cmax este de 529 ng / ml și ASC este de 3.451 ng xh / ml. Raportul precursor al metabolitului este de 0,28 pentru Cmax și 0,42 pentru ASC.
Biodisponibilitatea absolută medie a ticagrelor a fost estimată la 36%. Ingerarea unei mese bogate în grăsimi a determinat o creștere cu 21% a ASC a ticagrelor și o scădere cu 22% a Cmax a metabolitului activ, dar nu a avut niciun efect asupra Cmax a ticagrelor sau ASC a ticagrelor. Metabolit activ. modificările sunt considerate a fi de relevanță clinică minimă, prin urmare ticagrelor pot fi administrate atât cu cât și departe de mese. Ticagrelor și metabolitul său activ sunt substraturi pentru P-gp.
Ticagrelor sub formă de comprimate zdrobite amestecate în apă, administrate oral sau printr-un tub nazogastric în stomac, are o biodisponibilitate comparabilă cu comprimatele întregi pentru ASC și Cmax atât pentru ticagrelor, cât și pentru metabolitul activ. Expunere inițială (0, 5 și 1 oră după doză) la comprimatele de ticagrelor zdrobite amestecate în apă a fost mai mare decât la comprimatele întregi, cu un profil de concentrație de atunci în general identic (2 până la 48 de ore).
Distribuție
Volumul de distribuție la starea de echilibru a ticagrelor este de 87,5 L. Ticagrelor și metabolitul său activ se leagă extensiv de proteinele plasmatice (> 99,0%).
Biotransformare
CYP3A4 este enzima principală responsabilă de metabolismul ticagrelor și de formarea metabolitului activ, iar interacțiunile acestora cu alte substraturi CYP3A variază de la activare la inhibare.
Metabolitul principal al ticagrelor este AR-C124910XX, care are și activitate farmacologică, după cum s-a demonstrat in vitro prin legarea la receptorul trombocit P2Y12 al ADP. Expunerea sistemică la metabolitul activ este de aproximativ 30-40% din cea observată la ticagrelor.
Eliminare
Calea principală de eliminare a ticagrelor este prin metabolismul hepatic. Când se administrează ticagrelor marcate radioactiv, recuperarea medie a radioactivității este de aproximativ 84% (57,8% în materiile fecale, 26,5% în urină). doza.
Calea principală de eliminare a metabolitului activ este probabil secreția biliară. Media t1 / 2 a fost de aproximativ 7 ore pentru ticagrelor și 8,5 ore pentru metabolitul activ.
Populații speciale
Persoane în vârstă
Au fost observate expuneri mai mari la ticagrelor (aproximativ 25% atât pentru Cmax, cât și pentru ASC) și metabolitul activ la pacienții vârstnici (≥75 ani) cu SCA comparativ cu pacienții mai tineri, printr-o „analiză farmacocinetică populațională. Sunt considerate semnificative clinic (vezi pct. 4.2 ).
Populația pediatrică
Ticagrelor nu a fost evaluat la copii și adolescenți (vezi pct. 4.2 și 5.1).
Sex
Au fost observate expuneri mai mari ale ticagrelor și ale metabolitului activ la femei decât la bărbați. Aceste diferențe nu sunt considerate semnificative clinic.
Afectarea funcției renale
Expunerea la ticagrelor a fost cu aproximativ 20% mai mică, iar expunerea la metabolit activ a fost cu aproximativ 17% mai mare la pacienții cu insuficiență renală severă (clearance-ul creatininei
Afectarea funcției hepatice
Cmax și ASC ale ticagrelor au fost cu 12% și 23% mai mari la pacienții cu insuficiență hepatică ușoară comparativ cu un eșantion comparabil de subiecți sănătoși (vezi pct. 4.2). Ticagrelor nu a fost studiat la pacienții cu insuficiență hepatică moderată sau severă, iar utilizarea acestuia la acești pacienți este contraindicată (vezi pct. 4.3 și 4.4).
Etnie
Pacienții de origine asiatică prezintă o biodisponibilitate medie care este cu 39% mai mare decât pacienții caucazieni. Pacienții auto-identificați ca negri au avut o biodisponibilitate a ticagrelor cu 18% mai mică decât pacienții caucazieni. În studiile clinice de farmacologie, expunerea (Cmax și ASC) la ticagrelor la pacienții japonezi a fost cu aproximativ 40% (20% după ajustarea greutății corporale) mai mare decât la pacienții caucazieni.
05.3 Date preclinice de siguranță
Datele preclinice ale ticagrelor și ale metabolitului său major nu au demonstrat un risc inacceptabil de efecte adverse pentru om pe baza studiilor convenționale de siguranță farmacologică, toxicitate la doză unică sau repetată și potențial genotoxic.
S-a observat iritație gastro-intestinală la mai multe specii de animale pentru niveluri de expunere relevante clinic (vezi pct. 4.8).
La femelele de șobolan, ticagrelor la doze mari au arătat o incidență crescută a tumorilor uterine (adenocarcinoame) și o incidență crescută a adenoamelor hepatice. Mecanismul de apariție a tumorilor uterine este probabil legat de un dezechilibru hormonal care poate duce la formarea tumorii la șobolani. Mecanismul care stă la baza formării adenoamelor hepatice se datorează probabil unei induceri a enzimelor hepatice specifice rozătoarelor. Prin urmare, observațiile referitoare la potențialul cancerigen sunt considerate a fi puțin relevante pentru oameni.
Au fost observate anomalii minore de dezvoltare la șobolani la o doză toxică maternă (marja de siguranță 5.1). La iepuri, o ușoară întârziere a maturității hepatice și a dezvoltării scheletului a fost observată la fetuși de la mame expuse la doze mari, fără semne de toxicitate maternă (marjă de siguranță 4.5).
Studiile efectuate la șobolani și iepuri au arătat toxicitate asupra funcției de reproducere, cu o ușoară scădere a creșterii în greutate a mamei, reducerea viabilității neonatale și scăderea greutății la naștere, cu întârziere a creșterii. privind fertilitatea generală la șobolani masculi și femele Studiile farmacocinetice efectuate cu ticagrelor radiomarcate au arătat că compusul părinte și metaboliții săi sunt excretați în laptele șobolanilor (vezi pct. 4.6).
06.0 INFORMAȚII FARMACEUTICE
06.1 Excipienți
Miezul tabletei
Manitol (E421)
Hidrogen fosfat de calciu dihidrat
Stearat de magneziu (E470b)
Glicolat de amidon de sodiu
Hidroxipropilceluloză (E463)
Acoperirea tabletei
Talc
Dioxid de titan (E171)
Oxid de fier galben (E172)
Polietilen glicol 400
Hipromeloză (E464)
06.2 Incompatibilitate
Nu este relevant.
06.3 Perioada de valabilitate
3 ani.
06.4 Precauții speciale pentru depozitare
Acest medicament nu necesită condiții speciale de păstrare.
06.5 Natura ambalajului imediat și conținutul ambalajului
• Blister transparent (cu simboluri soare / lună) în PVC-PVDC / Al a 10 comprimate; cutii de 60 de comprimate (6 blistere) și 180 de comprimate (18 blistere).
• Blister transparent din calendar (cu simboluri soare / lună) în PVC-PVDC / Al din 14 comprimate; cutii cu 14 comprimate (1 blister), 56 comprimate (4 blistere) și 168 comprimate (12 blistere).
• Blister transparent perforat monodoză perforat în PVC-PVDC / Al a 10 comprimate; cutii de 100x1 comprimate (10 blistere).
Este posibil ca nu toate mărimile de ambalaj să fie comercializate.
06.6 Instrucțiuni de utilizare și manipulare
Fără instrucțiuni speciale.
07.0 DEȚINĂTORUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
AstraZeneca AB
SE-151 85
Södertälje
Suedia
08.0 NUMĂRUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
EU / 1/10/655 / 001-006
040546018
040546020
040546032
040546044
040546057
040546069
09.0 DATA PRIMEI AUTORIZAȚII SAU REÎNNOIREA AUTORIZAȚIEI
Data primei autorizații: 03 decembrie 2010
Data celei mai recente reînnoiri: 17 iulie 2015
10.0 DATA REVIZUIRII TEXTULUI
Iulie 2015