Pentru a putea vorbi într-un mod ușor de înțeles de „hemoglobina (Hb), este util să ai grijă de primul mioglobina (Mb) care este foarte asemănător cu hemoglobina, dar este mult mai simplă. Între hemoglobină și mioglobină există relații de rudenie strânse: ambele sunt proteine conjugate, iar grupul lor protetic (partea neproteică) este grupul heme.
Mioglobina este o proteină globulară formată dintr-un singur lanț de aproximativ o sută cincizeci de aminoacizi (depinde de organism) și greutatea sa moleculară este de aproximativ 18 Kd.
După cum sa menționat, este echipat cu o grupă hem care este inserată într-o porțiune hidrofobă (sau lipofilă) a proteinei, constând din pliuri atribuibile structurilor α-helix ale proteinelor fibroase.
Mioglobina este compusă în principal din segmente de helice α, prezente în număr de opt și constă, aproape exclusiv, din reziduuri nepolare (leucină, valină, metionină și fenilalanină) în timp ce reziduurile polare sunt practic absente (acid aspartic, acid glutamic, lizină și arginină); singurele reziduuri polare sunt două histidine, care joacă un rol fundamental în atașarea oxigenului la grupul hem.
Grupul hem este un grup cromofor (se absoarbe în vizibil) și este grupul funcțional al mioglobinei.
Vezi și: hemoglobină glicată - hemoglobină în urină
Un pic de chimie

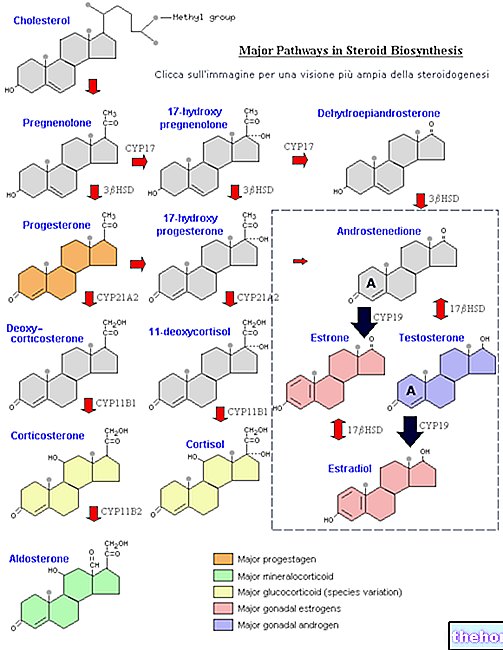
Legătura dintre protoporfirină și fier este o legătură tipică a compușilor de coordonare care sunt compuși chimici în care un atom central (sau ion) formează legături cu alte specii chimice într-un număr mai mare decât numărul său de oxidare (sarcină electrică). În cazul hemului, aceste legături sunt reversibile și slabe.
Numărul de coordonare (numărul de legături de coordonare) al fierului este de șase: pot exista șase molecule în jurul fierului care împart electronii care leagă.
Pentru a forma un compus de coordonare, este nevoie de doi orbitali cu orientare corectă: unul capabil să „dobândească” electroni și celălalt capabil să-i doneze.
În hem, fierul formează patru legături plane cu cei patru atomi de azot din centrul inelului proto-porfirinic și o a cincea legătură cu un azot histidinic proximal; fierul are a șasea legătură de coordonare liberă și se poate lega de oxigen.
Când fierul se prezintă sub forma unui ion liber, tipul său este orbital d toți au aceeași energie; în mioglobină, ionul de fier este legat de protoporfirină și histidină: aceste specii perturbă magnetic orbitalele d ceva fier; extinderea perturbației va fi diferită pentru diferiții orbitali d în funcție de orientarea lor spațială și de cea a speciilor perturbatoare. Deoarece energia totală a orbitalilor trebuie să fie constantă, perturbația provoacă o separare energetică între diferiții orbitali: energia dobândită de unii orbitali este echivalentă cu energia pierdută de ceilalți.
Dacă separarea care se produce între orbitali nu este foarte mare, este de preferat un aranjament electronic cu rotire ridicată: electronii de legare încearcă să se aranjeze în rotiri paralele în cât mai multe sub-nivele posibil (multiplicitate maximă); dacă, pe de altă parte, perturbația este foarte puternică și există o separare mare între orbitali, poate fi mai convenabil să împerecheați electronii de legătură în orbitalii cu energie inferioară (rotire redusă).
Când fierul se leagă de oxigen, molecula își asumă un aranjament de rotire scăzută, în timp ce atunci când fierul are a șasea legătură de coordonare liberă, molecula are un aranjament de rotire ridicat.
Datorită acestei diferențe de rotire, printr-o analiză spectrală a mioglobinei, putem înțelege dacă oxigenul (MbO2) este legat sau nu de acesta (Mb).
Mioglobina este o proteină musculară tipică (dar nu se găsește doar la nivelul mușchilor).
Mioglobina este extrasă din cachalota în care este prezentă în cantități mari și apoi este purificată.
Cetaceele au o respirație ca cea a ființelor umane: având plămâni trebuie să absoarbă aerul prin procesul respirator; cachalota trebuie să aducă cât mai mult oxigen posibil în mușchii capabili să acumuleze oxigen legându-l de mioglobina prezentă în ele; oxigenul este eliberat încet atunci când cetaceul este scufundat deoarece metabolismul său necesită oxigen: cu atât este mai mare cantitatea de oxigen pe care cașalotul este capabil să-l absoarbă și cu atât mai mult oxigen este disponibil în timpul scufundării.
Mioglibina leagă oxigenul într-o manieră reversibilă și este prezentă în țesuturile periferice într-un procent mai mare cu cât țesutul este obișnuit să lucreze cu rezervele de oxigen care sunt îndepărtate în timp.
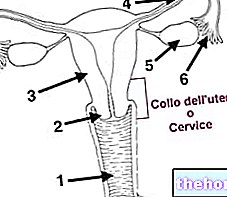
<--- Mioglobina este o proteină prezentă în mușchi, a cărei funcție este tocmai aceea de „rezervor” de oxigen.
Ceea ce face carnea mai mult sau mai puțin roșie este conținutul de hemoproteine (este hemul care face carnea roșie).
Hemoglobina are multe asemănări structurale cu mioglobina și este capabilă să lege oxigenul molecular într-un mod reversibil; dar, în timp ce mioglobina este limitată la mușchi și țesuturile periferice în general, hemoglobina se găsește în eritrocite sau celule roșii din sânge (sunt pseudo-celule, adică nu sunt celule reale) care reprezintă 40% din sânge.
Contrar mioglobinei, activitatea hemoglobinei este de a lua oxigen în plămâni, de a-l elibera în celulele unde este necesar, de a lua dioxid de carbon și de a-l elibera în plămâni unde ciclul începe din nou.
L "hemoglobină este un tetrameter, adică este alcătuit din patru lanțuri polipeptidice fiecare cu o grupă hem și identice două câte două (într-o ființă umană există două lanțuri alfa și două lanțuri beta).
Funcția principală a hemoglobinei este transportul oxigenului; o altă funcție a sângelui în care este implicată hemoglobina este transportul substanțelor către țesuturi.
În calea de la plămâni (bogată în oxigen) la țesuturi, hemoglobina transportă oxigen (în același timp, celelalte substanțe ajung la țesuturi), în timp ce în calea inversă, transportă cu sine deșeurile colectate de țesuturi, în special carbonul dioxid produs în metabolism.
În dezvoltarea unei ființe umane există gene care sunt exprimate doar pentru o anumită perioadă de timp; din acest motiv există diferite hemoglobine: fetale, embrionare, ale bărbatului adult.
Lanțurile care alcătuiesc aceste hemoglobine diferite au structuri diferite, dar cu unele asemănări, de fapt, funcția pe care o îndeplinesc este mai mult sau mai puțin aceeași.
O explicație a prezenței mai multor lanțuri diferite este următoarea: în cursul procesului evolutiv al organismelor, chiar și hemoglobina a evoluat specializându-se în transportul oxigenului din zonele bogate în acesta în zonele deficitare. La „început din lanțul evolutiv l "hemoglobina a transportat oxigenul în organismele mici; în cursul evoluției organismele au atins dimensiuni mai mari, prin urmare hemoglobina a fost modificată pentru a putea transporta oxigenul în zone mai îndepărtate de punctul în care era bogat în el; în acest sens, au fost codificate, în cursul procesului evolutiv, noi structuri ale lanțurilor care alcătuiesc hemoglobina.
Mioglobina leagă oxigenul chiar și la presiuni modeste; în țesuturile periferice există o presiune (PO2) de aproximativ 30 mmHg: mioglobina la această presiune nu eliberează oxigen, deci ar fi ineficientă ca purtător de oxigen. Pe de altă parte, hemoglobina , are un comportament mai elastic: leagă oxigenul de presiuni ridicate și îl eliberează atunci când presiunea scade.
Când o proteină este activă funcțional, își poate schimba puțin forma; de exemplu, mioglobina oxigenată are o formă diferită de mioglobina neoxigenată și această mutație nu își afectează vecinii.
Situația este diferită în cazul proteinelor asociate, cum ar fi hemoglobina: atunci când un lanț se oxigenează este indus să-și schimbe forma, dar această modificare este tridimensională, astfel încât sunt afectate și celelalte lanțuri ale tetrameterului. Faptul că lanțurile sunt asociate între ele., sugerează că modificarea unuia îi afectează pe ceilalți vecini chiar dacă într-o măsură diferită; atunci când un lanț se oxigenează, celelalte lanțuri ale tetrametrului își asumă o „atitudine mai puțin ostilă” față de oxigen: dificultatea cu care un lanț este oxigenează scade pe măsură ce lanțurile apropiate de acesta se oxigenează la rândul lor. Același lucru este valabil și pentru dezoxigenare.
Structura cuaternară a dezoxihemoglobinei se numește forma T (tensionată) în timp ce cea a oxihemoglobinei se numește forma R (eliberată); în starea tensionată există o serie de interacțiuni electrostatice destul de puternice între aminoacizii acizi și aminoacizii bazici care duc la o structură rigidă a deoxihemoglobinei (de aceea „forma tensionată”), în timp ce atunci când oxigenul este legat, entitatea acestor interacțiunile scad (de aici „forma eliberată”). Mai mult, în absența oxigenului, sarcina histidinei (vezi structura) este stabilizată de sarcina opusă a acidului aspartic în timp ce, în prezența oxigenului, există o tendință din partea proteinei de a pierde un proton; toate acestea implică faptul că hemoglobina oxigenată este un acid mai puternic decât hemoglobina dezoxigenată: efect bohr.
În funcție de pH, grupul hem se leagă mai mult sau mai puțin ușor de oxigen: într-un mediu acid, hemoglobina eliberează oxigenul mai ușor (forma tensionată este stabilă) în timp ce, într-un mediu bazic, legătura cu oxigenul este mai dură.

Fiecare hemoglobină eliberează 0,7 protoni pe mol de oxigen (O2) care intră.
Efectul Bohr permite hemoglobinei să-și îmbunătățească capacitatea de a transporta oxigen.
Hemoglobina care se deplasează de la plămâni la țesuturi trebuie să se echilibreze în funcție de presiune, pH și temperatură.
Să vedem efectul temperaturii.
Temperatura în alveolele pulmonare este cu aproximativ 1-1,5 ° C mai mică decât temperatura externă, în timp ce în mușchi temperatura este de aproximativ 36,5-37 ° C; pe măsură ce temperatura crește, factorul de saturație scade (la aceeași presiune): acest lucru se întâmplă deoarece energia cinetică crește și se favorizează disocierea.

Există alți factori care pot afecta capacitatea hemoglobinei de a se lega de oxigen, dintre care unul este concentrația de 2,3 bifosfoglicerat.
2,3 bifosfogliceratul este un metabolic prezent în eritrocite la o concentrație de 4-5 mM (în nicio altă parte a organismului nu este prezent într-o concentrație atât de mare).
La pH fiziologic, 2,3 bisfosfogliceratul este deprotonat și are cinci încărcături negative; este încastrat între cele două lanțuri beta ale hemoglobinei, deoarece aceste lanțuri au o concentrație mare de sarcini pozitive. Interacțiunile electrostatice dintre lanțurile beta și bifosfogliceratul de 2,3 conferă o anumită rigiditate sistemului: se obține o structură tensionată care are o afinitate mică pentru oxigen; în timpul oxigenării, bifosfogliceratul de 2,3 este apoi expulzat.
În eritrocite c "este un aparat special care transformă 1,3 bisfosfoglicerat (produs prin metabolism) în 2,3 bisfosfoglicerat astfel încât să atingă o concentrație de 4-5 mM și, prin urmare, hemoglobina este capabilă să schimbe" oxigenul din țesuturi.
Hemoglobina care ajunge la un țesut se află în starea eliberată (legată de oxigen), dar în vecinătatea țesutului, este carboxilată și trece la starea tensionată: proteina din această stare are o tendință mai mică de a se lega de oxigen, cu respect la starea eliberată, prin urmare hemoglobina eliberează oxigen în țesut; în plus, prin reacția dintre apă și dioxid de carbon, există producția de ioni H +, prin urmare, oxigen suplimentar datorită efectului bohr.
Dioxidul de carbon difuzează în eritrocit trecând prin membrana plasmatică; întrucât eritrocitele reprezintă aproximativ 40% din sânge, ar trebui să ne așteptăm ca doar 40% din dioxidul de carbon care difuzează din țesuturi să intre în ele, de fapt 90% din dioxidul de carbon intră în eritrocite deoarece conțin o enzimă care transformă dioxidul de carbon în acid carbonic, rezultă că concentrația staționară de dioxid de carbon în eritrocite este scăzută și, prin urmare, rata de intrare este mare.

Un alt fenomen care apare atunci când un eritrocit ajunge la un țesut este următorul: prin gradient, „HCO3- (derivatul dioxidului de carbon) părăsește„ eritrocitul și, pentru a echilibra ieșirea unei sarcini negative, avem „intrarea clorurilor care determină o creștere a presiunii osmotice: pentru a echilibra această variație există și intrarea apei care determină umflarea eritrocitului (efect HAMBURGER) .Fenomenul opus apare atunci când un eritrocit ajunge în alveolele pulmonare: o deflație a eritrocitelor (efect HALDANE) Prin urmare, eritrocitele venoase (direcționate către plămâni) sunt mai rotunde decât cele arteriale.