Ingrediente active: Docetaxel
TAXOTERE 20 mg / 0,5 ml concentrat și solvent pentru soluție perfuzabilă
Inserturile de pachete Taxotere sunt disponibile pentru pachete:- TAXOTERE 20 mg / 0,5 ml concentrat și solvent pentru soluție perfuzabilă
- TAXOTERE 80 mg / 2 ml concentrat și solvent pentru soluție perfuzabilă
- TAXOTERE 20 mg / 1 ml concentrat pentru soluție perfuzabilă
- TAXOTERE 80 mg / 4 ml concentrat pentru soluție perfuzabilă
- TAXOTERE 160 mg / 8 ml concentrat pentru soluție perfuzabilă
De ce se utilizează Taxotere? Pentru ce este?
Numele acestui medicament este TAXOTERE. Denumirea ingredientului activ este docetaxel.
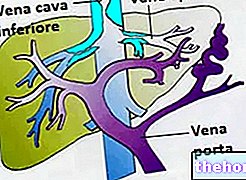
Docetaxel este o substanță derivată din frunzele asemănătoare acului plantei de tisa și aparține grupului de anticanceri numiți taxani.
TAXOTERE a fost prescris de medicul dumneavoastră pentru tratamentul cancerului de sân, a anumitor forme de cancer pulmonar (cancer pulmonar cu celule mici), cancer de prostată, cancer gastric sau cancer de cap și gât:
- Pentru tratamentul cancerului de sân avansat, TAXOTERE poate fi administrat singur sau în asociere cu doxorubicină sau trastuzumab sau capecitabină.
- Pentru tratamentul cancerului mamar precoce cu sau fără afectarea ganglionilor limfatici, TAXOTERE poate fi administrat în asociere cu doxorubicină și ciclofosfamidă.
- Pentru tratamentul cancerului pulmonar, TAXOTERE poate fi administrat singur sau în asociere cu cisplatină.
- pentru tratamentul cancerului de prostată, TAXOTERE se administrează în asociere cu prednison sau prednisolon.
- pentru tratamentul cancerului gastric metastatic, TAXOTERE se administrează în asociere cu cisplatină și 5-fluorouracil.
- pentru tratamentul cancerului de cap și gât, TAXOTERE se administrează în asociere cu cisplatină și 5-fluorouracil.
Contraindicații Când Taxotere nu trebuie utilizat
Nu trebuie să luați TAXOTERE
- dacă sunteți alergic (hipersensibil) la docetaxel sau la oricare dintre celelalte componente ale Taxotere;
- dacă numărul de celule albe din sânge este prea mic;
- dacă aveți probleme severe cu ficatul;
Precauții pentru utilizare Ce trebuie să știți înainte de a lua Taxotere
Înainte de fiecare tratament cu TAXOTERE este necesar să se efectueze analizele de sânge necesare pentru a stabili dacă există suficiente celule sanguine și dacă ficatul este suficient de activ.În cazul modificărilor globulelor albe din sânge, pot apărea și febră sau infecții.
Spuneți medicului dumneavoastră, farmacistului din spital sau asistentei medicale dacă aveți probleme de vedere.Dacă aveți probleme de vedere, în special vedere încețoșată, ar trebui să vi se verifice imediat ochii și vederea.
Dacă aveți probleme pulmonare acute sau dacă simptomele existente se agravează (febră, dificultăți de respirație sau tuse), spuneți imediat medicului dumneavoastră, farmacistului din spital sau asistentei medicului dumneavoastră.
Vi se va cere să luați un tratament preventiv cu corticosteroizi orali, cum ar fi dexametazona, cu o zi înainte de administrarea TAXOTERE și să continuați timp de una sau două zile după aceea, pentru a reduce unele reacții adverse care pot apărea în urma unei perfuzii de TAXOTERE, în special alergice. reacții și retenție de lichide (umflarea mâinilor, picioarelor, picioarelor sau creșterea în greutate).
În timpul tratamentului, este posibil să aveți nevoie de medicamente pentru a vă menține numărul de celule sanguine.
Interacțiuni Ce medicamente sau alimente pot modifica efectul Taxotere
Spuneți medicului dumneavoastră sau farmacistului din spital dacă luați sau ați luat recent orice alte medicamente, inclusiv dintre cele eliberate fără prescripție medicală. Acest lucru se datorează faptului că TAXOTERE sau alte medicamente pot să nu funcționeze conform așteptărilor și este posibil să fiți mai predispus la reacții adverse.
Avertismente Este important să știm că:
Sarcina, alăptarea și fertilitatea
Adresați-vă medicului dumneavoastră pentru recomandări înainte de a lua orice medicament.
TAXOTERE NU trebuie administrat dacă sunteți gravidă, cu excepția cazului în care medicul dumneavoastră vă indică în mod clar.
Nu trebuie să rămâneți gravidă în timpul tratamentului cu acest medicament și trebuie să utilizați măsuri contraceptive adecvate în timpul tratamentului, deoarece TAXOTERE poate fi periculos pentru copil. Dacă rămâneți gravidă în timpul tratamentului, vă rugăm să informați imediat medicul dumneavoastră. Nu trebuie să alăptați în timp ce luați TAXOTERE.
Dacă sunteți un bărbat care este tratat cu TAXOTERE, se recomandă să nu procreați în timpul și până la 6 luni după tratament și să întrebați despre depozitarea spermei înainte de tratament, deoarece docetaxel poate afecta fertilitatea masculină.
Conducerea vehiculelor și folosirea utilajelor:
Nu s-au efectuat studii privind efectele asupra capacității de a conduce vehicule și de a folosi utilaje.
Dozare și metoda de utilizare Cum se utilizează Taxotere: Doze
TAXOTERE vă va fi administrat de un profesionist din domeniul sănătății.
Doza uzuală:
Dozajul va depinde de greutatea dumneavoastră și de starea generală de sănătate. Medicul dumneavoastră vă va calcula suprafața corpului în metri pătrați (m2) și va determina doza pe care va trebui să o primiți.
Metoda și calea de administrare:
TAXOTERE vă va fi administrat prin perfuzie intravenoasă (administrare intravenoasă). Infuzia va dura aproximativ 1 oră și va avea loc în spital.
Frecvența administrării:
Perfuzia vi se va administra în mod normal o dată la 3 săptămâni.
Medicul dumneavoastră poate varia doza și frecvența de administrare în funcție de testele de sânge, starea generală și răspunsul dumneavoastră la TAXOTERE. Spuneți în special medicului dumneavoastră dacă aveți diaree, dureri în gură, amorțeală, furnicături, febră și prezentați rezultatele analizelor de sânge. Aceste informații îi vor permite să decidă dacă este necesară o reducere a dozei. Dacă aveți orice întrebări suplimentare cu privire la utilizarea acestui medicament, consultați medicul sau farmacistul din spital.
Efecte secundare Care sunt efectele secundare ale Taxotere
Ca toate medicamentele, acest medicament poate provoca reacții adverse, deși nu apar la toate persoanele.
Medicul dumneavoastră vă va discuta acest lucru și vă va explica riscurile și beneficiile potențiale ale tratamentului.
Cele mai frecvent raportate reacții adverse ale TAXOTERE în monoterapie sunt: scăderea numărului de celule roșii sau albe din sânge, căderea părului, greață, vărsături, inflamație la nivelul gurii, diaree și oboseală
Dacă TAXOTERE vi se administrează în asociere cu alți agenți chimioterapeutici, severitatea reacțiilor adverse poate fi crescută.
Următoarele reacții alergice pot apărea în timpul perfuziei în spital (pot afecta mai mult de 1 din 10 persoane):
- înroșirea feței, reacții cutanate, mâncărime
- strângere toracică, dificultăți de respirație
- febră sau frisoane
- dureri de spate
- presiune scăzută
Pot apărea reacții mai severe.
Starea dumneavoastră va fi atent monitorizată de personalul spitalului în timpul tratamentului. Spuneți imediat personalului spitalului dacă observați oricare dintre aceste efecte.
Efectele secundare enumerate mai jos pot apărea în timpul dintre două perfuzii de TAXOTERE, iar frecvența poate varia în funcție de combinația de medicamente pe care le luați:
Foarte frecvente (pot afecta mai mult de 1 din 10 persoane):
- infecții, scăderea numărului de globule roșii (anemie) sau de globule albe (acestea din urmă sunt importante în combaterea infecțiilor) și trombocite
- febră: în acest caz trebuie să vă informați imediat medicul
- reacții alergice descrise mai sus
- pierderea poftei de mâncare (anorexie)
- insomnie
- senzație de amorțeală sau furnicături sau durere la nivelul articulațiilor sau mușchilor
- durere de cap
- simțul gustului modificat
- inflamație a ochiului sau lacrimare crescută a ochiului
- umflarea cauzată de un drenaj limfatic insuficient
- dificultăți de respirație
- pierderea mucusului din nas; inflamația gâtului și nasului; tuse
- sângerări nazale
- inflamație în gură
- tulburări de stomac, inclusiv greață, vărsături și diaree, constipație
- durere abdominală
- indigestie
- căderea părului (creșterea părului revine la normal în majoritatea cazurilor)
- roșeață și umflarea palmelor mâinilor sau tălpilor picioarelor, care pot provoca descuamarea pielii (acest lucru se poate întâmpla și pe brațe, față sau corp)
- schimbarea culorii unghiilor, care se pot desprinde
- dureri musculare; dureri de spate sau dureri osoase
- modificări sau absența perioadei menstruale
- umflarea mâinilor, picioarelor, picioarelor
- oboseală sau simptome gripale
- creșterea sau pierderea în greutate
Frecvente (pot afecta până la 1 din 10 persoane):
- candidoză orală
- deshidratare
- ameţeală
- deficiențe de auz
- scăderea tensiunii arteriale; bătăi neregulate sau rapide ale inimii
- insuficienta cardiaca
- esofagită
- gură uscată
- dificultate sau durere la înghițire
- hemoragie
- creșterea enzimelor hepatice (de unde necesitatea testelor periodice de sânge)
Mai puțin frecvente (pot afecta până la 1 din 100 de persoane):
- leșin
- la locul injectării reacții cutanate, flebită (inflamație a venelor) sau umflături
- inflamație a colonului, intestinului subțire; perforație intestinală.
- formarea cheagurilor de sânge
Frecvență necunoscută:
- boală pulmonară interstițială (inflamație pulmonară care poate provoca tuse și dificultăți de respirație. Inflamația pulmonară se poate dezvolta și atunci când tratamentul cu docetaxel este administrat concomitent cu radioterapia)
- pneumonie (infecții pulmonare)
- fibroză pulmonară (cicatrizare și îngroșare în plămâni care provoacă dificultăți de respirație)
- vedere încețoșată din cauza umflării retinei în interiorul ochiului (edem macular cistoid)
- scăderea sodiului în sânge.
Raportarea efectelor secundare
Dacă manifestați orice reacții adverse, discutați cu medicul dumneavoastră, cu farmacistul din spital sau cu asistenta medicală.Acestea includ orice posibile reacții adverse nemenționate în acest prospect. De asemenea, puteți raporta reacțiile adverse direct prin intermediul sistemului național de raportare enumerat în Anexa V *. Raportând reacțiile adverse, puteți contribui la furnizarea mai multor informații despre siguranța acestui medicament.
Expirare și reținere
Nu lăsați acest medicament la vederea și îndemâna copiilor.
Nu utilizați acest medicament după data de expirare înscrisă pe cutie, blister și flacon.
A nu se păstra la temperaturi peste 25 ° C sau sub 2 ° C.
Păstrați medicamentul în ambalajul original pentru a-l proteja de lumina directă
Soluția prediluată trebuie utilizată imediat după preparare, chiar dacă stabilitatea chimico-fizică a soluției menționate a fost demonstrată pentru o perioadă de 8 ore dacă este depozitată între + 2 ° C și + 8 ° C sau la temperatura camerei (sub 25 C) .
Soluția trebuie utilizată în decurs de 4 ore dacă este păstrată la temperatura camerei (sub 25 ° C).
Ce conține flaconul de concentrat TAXOTERE:
Ingredientul activ este docetaxel (sub formă de trihidrat). Fiecare ml de soluție de docetaxel conține 40 mg de docetaxel (anhidru). Un flacon conține docetaxel 20 mg / 0,5 ml. Celelalte componente sunt polisorbat 80 și acid citric.
Ce conține flaconul cu solvent:
13% (greutate / greutate) 95% etanol în apă pentru preparate injectabile.
Descrierea aspectului TAXOTERE și conținutul ambalajului:
TAXOTERE 20 mg / 0,5 ml concentrat pentru soluție perfuzabilă este o soluție limpede, vâscoasă, de la galben la galben-maroniu.
Fiecare pachet conține
- un flacon cu doză unică de concentrat și,
- un flacon cu o singură doză de solvent
Următoarele informații sunt destinate numai profesioniștilor din domeniul sănătății.
GHID DE PREGĂTIRE PENTRU TAXOTERE 20 mg / 0,5 ml CONCENTRAT PENTRU SOLUȚIE PENTRU INFUZIE ȘI SOLVENT PENTRU TAXOTERE
Este important să citiți întregul conținut al acestui ghid înainte de a pregăti atât soluția TAXOTERE prediluată, cât și soluția TAXOTERE perfuzabilă.
1. FORMULARE
TAXOTERE 20 mg / 0,5 ml concentrat pentru soluție perfuzabilă este o soluție limpede, vâscoasă, de culoare galben până la galben-maro, conținând 40 mg / ml docetaxel (anhidru) în polisorbat 80 și acid citric. Solventul TAXOTERE este o soluție de 13% (greutate / greutate) de etanol 95% în apă pentru preparate injectabile.
2. PREZENTARE
TAXOTERE este furnizat în flacoane cu doză unică.
Fiecare ambalaj conține un flacon de TAXOTERE (20 mg / 0,5 ml) și un flacon cu solvent corespunzător pentru TAXOTERE în blistere.
Flacoanele TAXOTERE trebuie păstrate între + 2 ° C și + 25 ° C ferite de lumină.
TAXOTERE nu trebuie utilizat după data de expirare înscrisă pe cutie, blister și flacon.
2.1 Flacoane de TAXOTERE 20 mg / 0,5 ml:
- Flaconul de TAXOTERE 20 mg / 0,5 ml, are o capacitate de 7 ml, este fabricat din sticlă transparentă cu capac verde detașabil.
- Flaconul de TAXOTERE 20 mg / 0,5 ml conține o soluție de docetaxel în polisorbat 80 la o concentrație de 40 mg / ml.
- Fiecare flacon de TAXOTERE 20 mg / 0,5 ml conține 0,5 ml de 40 mg / ml soluție de docetaxel în polisorbat 80 (volum de umplere: 24,4 mg / 0,61 ml). Această supradoză a fost stabilită în timpul dezvoltării TAXOTERE pentru a compensa pierderea de lichid în timpul preparării soluției prediluate (vezi secțiunea 4) datorită spumării, aderenței la pereții flaconului și „spațiului mort”. Această supradoză asigură că după diluarea cu conținutul întreg al flaconului cu solvent inclus cu TAXOTERE, volumul minim extractibil de soluție prediluită este de 2 ml, conținând 10 mg / ml de docetaxel, care corespunde conținutului declarat pe etichetă de 20 mg / 0, 5 ml pe flacon.
2.2 Solvent pentru flacoane TAXOTERE 20 mg / 0,5 ml:
- Solventul pentru TAXOTERE 20 mg / 0,5 ml este conținut într-un flacon din sticlă transparentă de 7 ml, cu capac transparent.
- Solventul pentru TAXOTERE 20 mg / 0,5 ml constă dintr-o soluție de 13% (greutate / greutate) de 95% etanol în apă pentru preparate injectabile.
- Fiecare flacon de solvent pentru TAXOTERE 20 mg / 0,5 ml conține 1,98 ml de soluție. Acest volum a fost calculat pe baza volumului real al flacoanelor TAXOTERE 20 mg / 0,5 ml. Adăugarea întregului conținut al flaconului cu solvent la cea de TAXOTERE 20 mg / 0,5 ml asigură obținerea unei soluții prediluate de 10 mg / ml de docetaxel.
3. RECOMANDĂRI PENTRU MANIPULARE SIGURĂ
TAXOTERE este un medicament antineoplazic și, ca și în cazul altor produse potențial toxice, trebuie să se acorde prudență la manipularea și prepararea soluțiilor. Se recomandă utilizarea mănușilor.
Dacă TAXOTERE în formă concentrată, pre-diluată sau soluție perfuzabilă trebuie să intre în contact cu pielea, se spală imediat și bine cu apă și săpun. Dacă TAXOTERE în formă concentrată, pre-diluată sau în soluție perfuzabilă trebuie să intre în contact cu membranele mucoase, spălați imediat și bine cu apă.
4. PREGĂTIREA PENTRU ADMINISTRAREA INTRAVENOASĂ
4.1 Pregătirea soluției prediluate de TAXOTERE (10 mg docetaxel / ml)
4.1.1 Dacă flacoanele sunt depozitate la frigider, lăsați numărul necesar de cutii de TAXOTERE la temperatura camerei (sub 25 ° C) timp de 5 minute.
4.1.2 Folosind o seringă gradată cu un ac, retrageți aseptic întregul conținut al flaconului de solvent pentru TAXOTERE inversând parțial flaconul.
4.1.3 Injectați întregul conținut al seringii în flaconul corespunzător de TAXOTERE
4.1.4 Scoateți seringa și acul și amestecați soluția manual inversând în mod repetat timp de 45 de secunde. Nu agitați.
4.1.5 Lăsați flaconul cu soluție prediluită să stea 5 minute la temperatura camerei (sub 25 ° C) și apoi verificați dacă soluția este limpede și omogenă (spumarea este normală chiar și după 5 minute datorită conținutului de polisorbat 80 din formulare) .
Soluția prediluată conține 10 mg / ml docetaxel și trebuie utilizată imediat după preparare, chiar dacă stabilitatea chimico-fizică a acestei soluții a fost demonstrată pentru o perioadă de 8 ore dacă este depozitată între + 2 ° C și + 8 C sau în mediu temperatura (sub 25 C).
4.2 Pregătirea soluției perfuzabile
4.2.1 Pot fi necesare mai multe flacoane de soluție prediluată pentru a obține doza necesară pentru pacient. Pe baza dozei necesare pentru pacienți în mg, retrageți aseptic volumul corespunzător de soluție prediluată care conține docetaxel de 10 mg / ml dintr-un număr adecvat de flacoane folosind o seringă gradată cu ac. De exemplu, pentru o doză de 140 mg docetaxel, trebuie retrase 14 ml de soluție prediluită de docetaxel.
4.2.2 Se injectează volumul necesar de soluție prediluită într-o pungă sau flacon de 250 ml care conține soluție de glucoză 5% sau soluție perfuzabilă de 9 mg / ml clorură de sodiu (0,9%). Dacă este necesară o doză de docetaxel mai mare de 200 mg, utilizați un volum mai mare de soluție perfuzabilă, astfel încât concentrația de docetaxel să nu depășească 0,74 mg / ml.
4.2.3 Se amestecă manual punga sau sticla cu o mișcare de răsucire.
4.2.4 Soluția perfuzabilă TAXOTERE trebuie utilizată în decurs de 4 ore și trebuie administrată sub formă de perfuzie de 1 oră, aseptic, la temperatura camerei (sub 25 ° C) și în condiții normale de lumină. Document pus la dispoziție de AIFA la 27.05.2015 243
4.2.5 Ca și în cazul tuturor produselor de uz parenteral, soluția prediluită și soluția perfuzabilă de TAXOTERE trebuie examinate vizual înainte de utilizare, soluțiile care conțin precipitate trebuie aruncate.
5. METODA DE ELIMINARE
Toate dispozitivele care au fost utilizate pentru a dilua sau administra TAXOTERE ar trebui tratate în conformitate cu procedurile standard. Nu aruncați niciun medicament pe scurgere. Întrebați farmacistul cum să aruncați medicamentele pe care nu le mai utilizați. Acest lucru va ajuta la protejarea mediului.
Prospect sursă: AIFA (Agenția italiană pentru medicamente). Conținut publicat în ianuarie 2016. Este posibil ca informațiile prezente să nu fie actualizate.
Pentru a avea acces la cea mai actualizată versiune, este recomandabil să accesați site-ul web AIFA (Agenția italiană pentru medicamente). Declinare de responsabilitate și informații utile.
01.0 DENUMIREA PRODUSULUI MEDICAMENTAL
TAXOTERE 20 MG / 0,5 ML
02.0 COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ
Fiecare flacon cu doză unică de TAXOTERE 20 mg / 0,5 ml concentrat care conține docetaxel sub formă de trihidrat, corespunzător la 20 mg de docetaxel (anhidru). Soluția vâscoasă conține docetaxel 40 mg / ml (anhidru).
Excipient: Fiecare flacon cu o singură doză de solvent conține 13% (greutate / greutate) 95% etanol în apă pentru preparate injectabile.
Pentru lista completă a excipienților, vezi secțiunea 6.1.
03.0 FORMA FARMACEUTICĂ
Concentrat și solvent pentru soluție perfuzabilă.
Concentratul este o soluție limpede, vâscoasă, de la galben la galben-maro.
Solventul este o soluție incoloră.
04.0 INFORMAȚII CLINICE
04.1 Indicații terapeutice
Cancer mamar:
TAXOTERE în asociere cu doxorubicină și ciclofosfamidă este indicat pentru tratamentul adjuvant al pacienților cu:
- cancer mamar operabil ganglion limfatic pozitiv;
- cancer mamar negativ operabil.
La pacienții cu cancer de sân negativ operabil, tratamentul adjuvant ar trebui limitat la pacienții candidați la chimioterapie în conformitate cu criteriile internaționale pentru tratamentul primar al cancerului de sân în stadiu incipient. (vezi pct. 5.1).
TAXOTERE în asociere cu doxorubicină este indicat pentru tratamentul pacienților cu cancer de sân local avansat sau metastatic care nu au primit anterior tratament citotoxic pentru această boală.
TAXOTERE ca monoterapie este indicat pentru tratamentul pacienților cu cancer mamar local avansat sau metastatic după eșecul terapiei citotoxice. Chimioterapia anterioară trebuie să fi inclus o antraciclină sau un agent alchilant.
TAXOTERE în asociere cu trastuzumab este indicat pentru tratamentul pacienților cu cancer mamar metastatic cu supraexpresie HER2 și care nu au primit anterior chimioterapie pentru boala metastatică.
TAXOTERE în asociere cu capecitabină este indicat pentru tratamentul pacienților cu cancer mamar local avansat sau metastatic după eșecul chimioterapiei citotoxice.
Chimioterapia anterioară trebuie să fi inclus o antraciclină. Cancerul pulmonar fără celule mici TAXOTERE este indicat pentru tratamentul pacienților cu cancer pulmonar non-celular mic avansat local sau metastatic după eșecul chimioterapiei anterioare.
TAXOTERE în asociere cu cisplatină este indicat pentru tratamentul pacienților cu cancer pulmonar necelular, local avansat sau metastazat cu celule mici, care nu au primit chimioterapie anterioară pentru această afecțiune.
Cancer de prostată:
TAXOTERE în asociere cu prednison sau prednisolon este indicat pentru tratamentul pacienților cu cancer hormonal refractar de prostată metastatic.
Adenocarcinom gastric:
TAXOTERE în asociere cu cisplatină și 5-fluorouracil este indicat pentru tratamentul pacienților cu adenocarcinom gastric metastatic, inclusiv adenocarcinom de joncțiune gastroesofagiană, care nu au primit anterior chimioterapie pentru boala lor metastatică.
Cancer de cap și gât:
TAXOTERE în asociere cu cisplatină și 5-fluorouracil este indicat pentru tratamentul de inducție al pacienților cu carcinom cu celule scuamoase avansat local al capului și gâtului.
04.2 Doze și mod de administrare
Utilizarea docetaxel trebuie limitată la departamentele specializate în administrarea de terapii citotoxice, iar administrarea acestuia trebuie să fie sub supravegherea unui medic specializat în utilizarea chimioterapiei anticanceroase (vezi pct. 6.6).
Doza recomandată:
Pentru cancer de sân, cancer pulmonar cu celule mici, adenocarcinom gastric și cancer de cap și gât, premedicație cu un corticosteroid oral, cum ar fi dexametazona 16 mg / zi (de exemplu, 8 mg BID) timp de 3 zile începând cu o zi înainte de administrarea docetaxel (vezi secțiunea 4.4) Profilaxia G-CSF poate fi utilizată pentru a reduce riscul de toxicitate hematologică.
Pentru cancerul de prostată, având în vedere utilizarea concomitentă de prednison sau prednisolon, premedicația recomandată este dexametazona orală cu 8 mg cu 12 ore, 3 ore și 1 oră înainte de perfuzia cu docetaxel (vezi pct. 4.4).
Docetaxel se administrează sub formă de perfuzie de o oră la fiecare trei săptămâni.
Cancer mamar:
Pentru terapia adjuvantă a cancerului de sân operabil pozitiv și negativ la nod, doza recomandată de docetaxel este de 75 mg / m2 administrată la 1 oră după doxorubicină 50 mg / m2 și ciclofosfamidă 500 mg / m2 la fiecare 3 săptămâni timp de 6 cicluri. (Regim TAC ) (vezi și ajustarea dozei în timpul tratamentului).
Pentru tratamentul pacienților cu cancer mamar local avansat sau metastatic, doza recomandată de docetaxel în monoterapie este de 100 mg / m2. În tratamentul de primă linie, docetaxel 75 mg / m2 se administrează în asociere cu doxorubicină (50 mg / m2).
În asociere cu trastuzumab, doza recomandată de docetaxel este de 100 mg / m2 la fiecare 3 săptămâni, cu trastuzumab administrat săptămânal. În studiul pivot, perfuzia inițială de docetaxel a fost începută a doua zi după prima administrare de trastuzumab. Dozele ulterioare de docetaxel au fost administrate imediat după perfuzia cu trastuzumab dacă doza anterioară de trastuzumab a fost bine tolerată. Pentru doza și administrarea de trastuzumab, consultați rezumatul caracteristicilor produsului pentru trastuzumab.
În asociere cu capecitabină, doza recomandată de docetaxel este de 75 mg / m2 la fiecare trei săptămâni, în asociere cu capecitabină la o doză de 1250 mg / m2 de două ori pe zi (în termen de 30 de minute după masă) timp de 2 săptămâni, urmată de un interval de 1 săptămână. . Pentru calcularea dozei de capecitabină în funcție de suprafața corporală, consultați rezumatul caracteristicilor produsului de capecitabină.
Cancer pulmonar cu celule mici:
La pacienții care nu au primit niciodată chimioterapie pentru cancer pulmonar cu celule mici, doza recomandată este docetaxel 75 mg / m2 urmată imediat de cisplatină 75 mg / m2 timp de 30-60 minute. Pentru tratamentul după eșecul chimioterapiei anterioare care conține platină, doza recomandată este de 75 mg / m2 ca monoterapie.
Cancer de prostată:
Doza recomandată de docetaxel este de 75 mg / m2. Prednison sau prednisolon 5 mg pe cale orală de două ori pe zi se administrează pe durata tratamentului (vezi pct. 5.1).
Adenocarcinom gastric:
Doza recomandată de docetaxel este de 75 mg / m2 sub formă de perfuzie de 1 oră, urmată de cisplatină de 75 mg / m2, sub formă de perfuzie de 1-3 ore (ambele doar în ziua 1), urmată de 5-fluorouracil 750 mg / m2 pe zi administrată sub formă de perfuzie continuă de 24 de ore timp de 5 zile, începând de la sfârșitul perfuziei cu cisplatină. Tratamentul se repetă la fiecare trei săptămâni. Pacienții trebuie să primească premedicație cu antiemetice și hidratare adecvată pentru administrare. de cisplatină.
Profilaxia G-CSF trebuie utilizată pentru a atenua riscul de toxicitate hematologică (vezi și ajustarea dozei în timpul tratamentului).
Cancer de cap și gât:
Pacienții trebuie să primească antiemetice de premedicație și hidratare adecvată (înainte și după administrarea cisplatinei). Profilaxia G-CSF se poate face în așa fel încât să atenueze riscul toxicităților hematologice. Toți pacienții tratați cu docetaxel din studiile TAX 323 și TAX 324 au primit profilaxia antibioticelor.
Chimioterapie de inducție urmată de radioterapie (TAX 323):
Pentru tratamentul de inducție al pacienților cu carcinom cu celule scuamoase irezecabil la nivel local al capului și gâtului (SCCHN), doza recomandată de docetaxel este de 75 mg / m2 sub formă de perfuzie de 1 oră, urmată de 75 mg / m2 de cisplatină timp de peste 1 oră ziua 1, urmată de 5-fluorouracil 750 mg / m2 pe zi administrată sub formă de perfuzie continuă de 24 de ore timp de 5 zile. Acest program de dozare este administrat la fiecare 3 săptămâni timp de 4 cicluri. După chimioterapie, pacienții trebuie să primească radioterapie.
Chimioterapie de inducție urmată de chimioterapie (TAX 324):
Pentru tratamentul de inducție al pacienților cu carcinom scuamos cu celule scuamoase la nivelul capului și gâtului (SCCHN) (inoperabil din punct de vedere tehnic, cu o probabilitate redusă de succes chirurgical și în vederea conservării organelor) doza recomandată de docetaxel este de 75 mg / m2 sub formă de perfuzie de 1 oră în ziua 1, urmată de cisplatină 100 mg / m2 administrată sub formă de perfuzie de 30 minute până la trei ore, urmată de 5-fluorouracil 1000 mg / m2 zilnic, administrată în perfuzie continuă de 1 - 4 zile. Acest program de dozare este dat la fiecare trei săptămâni timp de trei cicluri. După chimioterapie, pacienții trebuie să primească chimioterapie.
Pentru modificarea dozei de 5-fluorouracil și cisplatină, consultați Rezumatul specific al caracteristicilor produsului. Ajustarea dozei în timpul tratamentului:
General
Docetaxel trebuie administrat atunci când numărul neutrofilelor este de 3 1500 celule / mm3.
La pacienții care au prezentat neutropenie febrilă, neuropatie periferică severă a neutrofilelor în timpul terapiei cu docetaxel, doza de docetaxel trebuie redusă de la 100 mg / m2 la 75 mg / m2 și / sau de la 75 la 60 mg / m2. Dacă, la 60 mg / m2, pacientul continuă să prezinte aceste reacții, tratamentul trebuie întrerupt.
Terapia adjuvantă pentru cancerul de sân:
Profilaxia primară G-CSF trebuie luată în considerare la pacienții care primesc terapie adjuvantă cu docetaxel, doxorubicină și ciclofosfamidă (TAC) pentru cancerul de sân. La pacienții care prezintă neutropenie febrilă și / sau infecție neutropenică, doza de docetaxel trebuie redusă la 60 mg / m2 în toate cursurile ulterioare (vezi pct. 4.4 și 4.8). La pacienții cu stomatită de gradul 3 sau 4, doza trebuie redusă la 60 mg / m2
În asociere cu cisplatina:
Pentru pacienții tratați inițial cu docetaxel 75 mg / m2 în asociere cu cisplatină și al căror număr scăzut de trombocite în cursul anterior al terapiei a fost
În asociere cu capecitabină:
Pentru ajustarea dozei de capecitabină, vezi Rezumatul caracteristicilor produsului pentru capecitabină.
La pacienții care prezintă prima apariție a toxicității de gradul 2 care persistă în momentul administrării ulterioare a docetaxel / capecitabină, tratamentul trebuie amânat până la rezoluție la gradul 0-1 și apoi reluat la 100% din doza inițială.
La pacienții care dezvoltă a doua apariție a toxicității de gradul 2 sau prima apariție a toxicității de gradul 3 în orice moment al cursului terapiei, tratamentul trebuie amânat până la rezoluție la gradul 0-1 și apoi reluat cu docetaxel 55 mg / m2 .
Pentru orice apariție ulterioară de toxicitate sau pentru orice toxicitate de gradul 4, întrerupeți tratamentul cu docetaxel.
Pentru modificări ale dozei de trastuzumab, consultați Rezumatul caracteristicilor produsului pentru trastuzumab.
În asociere cu cisplatină și 5-fluorouracil:
Dacă apare un episod de neutropenie febrilă, neutropenie prelungită sau neutropenie infecțională în ciuda utilizării G-CSF, doza de docetaxel trebuie redusă de la 75 la 60 mg / m2. Dacă apar alte episoade de neutropenie complicată, doza de docetaxel trebuie redusă de la 60 până la 45 mg / m2.Pentru trombocitopenia de gradul 4, doza de docetaxel trebuie redusă de la 75 la 60 mg / m2. Pacienții nu trebuie retrași cu alte cursuri de docetaxel până când neutrofilele nu revin la un nivel> 1.500 celule / mm3 și trombocitele revin la un nivel> 100.000 celule / mm3. Întrerupeți tratamentul dacă aceste toxicități persistă (vezi pct. 4.4). Modificări ale dozelor recomandate din cauza toxicității la pacienții tratați cu docetaxel în asociere cu cisplatină și 5-fluorouracil (5-FU):
Pentru modificări ale dozei de cisplatină și 5-fluorouracil, consultați Rezumatul specific al caracteristicilor produsului.
În studiul pivot SCCHN la pacienți care au prezentat neutropenie complicată (inclusiv neutropenie prelungită, neutropenie febrilă sau infecție), sa sugerat utilizarea GCSF pentru a asigura o acoperire profilactică (de exemplu, zilele 6-15) în toate ciclurile ulterioare.
Populații speciale:
Pacienți cu insuficiență hepatică:
Pe baza datelor farmacocinetice cu docetaxel la 100 mg / m2 administrat ca tratament unic, la pacienții cu creșteri ale transaminazelor (ALT și / sau AST) mai mari de 1,5 ori limita superioară a normalului și fosfataza alcalină mai mare de 2,5 ori limita superioară a normalului , doza recomandată de docetaxel este de 75 mg / m2 (vezi pct. 4.4 și 5.2). Pentru pacienții cu bilirubină serică peste limita superioară a normalului și / sau ALT și AST> 3,5 ori limita superioară a normalului asociată cu fosfatază alcalină mai mare de 6 ori limita superioară a normalului, nu se poate recomanda reducerea dozei și docetaxel nu trebuie administrat cu excepția cazurilor în care este strict indicat.
În combinație cu cisplatină și 5-fluorouracil pentru tratamentul pacienților cu adenocarcinom gastric, studiul clinic pivot a exclus pacienții cu ALT și / sau AST> 1,5 ori limita superioară a normalului asociată cu o valoare a fosfatazei alcaline.> 2,5 ori limita superioară de normal și la o valoare a bilirubinei> 1 ori limita superioară a normalului; la acești pacienți, nu se poate recomanda reducerea dozei și docetaxel nu trebuie utilizat decât dacă este indicat strict. Nu există date disponibile la pacienții cu insuficiență hepatică tratați cu docetaxel în asociere în celelalte indicații.
Populația pediatrică:
Siguranța și eficacitatea TAXOTERE în cancerul nazofaringian la copii cu vârsta cuprinsă între 1 lună și mai puțin de 18 ani nu au fost stabilite.
Nu există date privind utilizarea TAXOTERE la populația pediatrică în indicațiile cancerului de sân, cancerului pulmonar cu celule mici, cancer de prostată, cancer gastric și cancer de cap și gât, cu excepția cancerului nazofaringian de tip II și III mai puțin diferențiat.
Persoane în vârstă.
Pe baza farmacocineticii populației, nu există instrucțiuni speciale de utilizare la vârstnici.
În asociere cu capecitabină la pacienții cu vârsta de 60 de ani și peste, se recomandă o reducere a dozei inițiale la 75% (vezi Rezumatul caracteristicilor produsului pentru capecitabină).
04.3 Contraindicații
Hipersensibilitate la substanța activă sau la oricare dintre excipienți.
Docetaxel nu trebuie utilizat la pacienții cu un număr inițial de neutrofile
Docetaxel nu trebuie utilizat la pacienții cu insuficiență hepatică severă din cauza lipsei datelor disponibile (vezi pct. 4.2 și 4.4).
Contraindicațiile pentru alte medicamente se aplică și atunci când sunt utilizate în asociere cu docetaxel.
04.4 Avertismente speciale și precauții adecvate pentru utilizare
Cu excepția cazului în care este contraindicat, premedicația cu corticosteroizi orali, cum ar fi dexametazonă 16 mg pe zi (de exemplu, 8 mg BID) timp de 3 zile, începând cu o zi înainte de administrarea docetaxel, timp de 3 zile începând cu ziua înainte de administrarea docetaxel pentru cancerul de sân și celulele pulmonare non-mici, poate reduce „incidența și severitatea retenției de lichide, precum și severitatea reacțiilor de hipersensibilitate. Pentru cancerul de prostată, premedicația este dexametazonă orală cu 8 mg, 12 ore, 3 ore și 1 oră înainte de perfuzia cu docetaxel (vezi punctul 4.2).
Hematologie:
Neutropenia este cea mai frecventă dintre reacțiile adverse observate la docetaxel. Nadiurile neutrofile au apărut după 7 zile (valoare mediană), dar la pacienții puternic pretratați acest interval poate fi scurtat. O verificare completă a numărului de sânge trebuie efectuată frecvent la toți pacienții care primesc docetaxel. Pacienții nu trebuie tratați din nou cu docetaxel până când valoarea neutrofilelor nu revine la 3 1.500 celule / mm3 (vezi pct. 4.2).
În cazul neutropeniei severe (
La pacienții tratați cu docetaxel în asociere cu cisplatină și 5-fluorouracil (TCF), neutropenia febrilă și infecția neutropenică au apărut cu o incidență mai mică atunci când pacienții au primit G-CSF profilactic. Pacienții tratați cu TCF trebuie să primească G-CSF ca profilaxie pentru a atenua riscul de neutropenie complicată (neutropenie febrilă, neutropenie prelungită sau infecție neutropenică). Pacienții care primesc TCF trebuie monitorizați foarte atent (vezi pct. 4.2 și 4.8).
La pacienții tratați cu docetaxel în asociere cu doxorubicină și ciclofosfamidă (regim TAC), neutropenia febrilă și / sau infecția neutropenică au apărut cu o „incidență mai mică atunci când pacienții au primit profilaxie primară G-CSF. Profilaxia primară G-CSF. LCR ar trebui luată în considerare la pacienți tratamentul CT adjuvant pentru cancerul de sân pentru a atenua riscul de neutropenie complicată (neutropenie febrilă, neutropenie prelungită sau infecție neutropenică).
Reacții de hipersensibilitate:
Pacienții trebuie monitorizați îndeaproape pentru apariția posibilelor reacții de hipersensibilitate, în special în timpul primei și celei de-a doua perfuzii. Reacțiile de hipersensibilitate pot apărea în câteva minute de la începerea perfuziei cu docetaxel, prin urmare trebuie să fie disponibile mijloace pentru tratarea hipotensiunii și bronhospasmului. Dacă apar reacții de hipersensibilitate cu simptome minore precum înroșirea feței sau reacții cutanate localizate, nu este necesară întreruperea tratamentului. Cu toate acestea, reacțiile severe, cum ar fi hipotensiunea arterială severă, bronhospasmul sau erupția cutanată / eritemul generalizat necesită întreruperea imediată a perfuziei cu docetaxel și tratamentul adecvat. Pacienții care prezintă reacții severe de hipersensibilitate nu trebuie să mai ia docetaxel.
Reacții cutanate:
Au fost observate eriteme cutanate localizate la nivelul extremităților (palma și talpa piciorului) cu edem urmat de descuamare. Au fost raportate simptome severe, cum ar fi erupții cutanate, urmate de descuamare care duc la întreruperea temporară sau permanentă a tratamentului cu docetaxel (vezi pct. 4.2).
Retenție de fluide:
Pacienții cu retenție severă de lichide, cum ar fi revărsările pleurale, pericardice și ascite, trebuie monitorizați îndeaproape.
Pacienți cu disfuncție hepatică:
La pacienții tratați cu docetaxel la 100 mg / m2 administrat singur, care au niveluri serice de transaminaze (ALT și / sau AST) mai mari de 1,5 ori limita superioară a normalului concomitent cu niveluri serice de fosfatază alcalină mai mari de 2,5 ori limita superioară a normalului, c "este un risc mai mare de a dezvolta reacții adverse grave, cum ar fi moartea toxică, inclusiv sepsis gastro-intestinal și hemoragie, care pot fi fatale, neutropenie febrilă, infecții, trombocitopenie, stomatită și astenie. Prin urmare, la pacienții cu teste funcționale hepatice ridicate, doza recomandată de docetaxel este 75 mg / m2 și testele funcției hepatice trebuie efectuate înainte de începerea tratamentului și înainte de fiecare ciclu (vezi pct. 4.2).
La pacienții care au valori serice ale bilirubinei mai mari decât limita superioară a valorilor normale și / sau ALT și AST mai mari de 3,5 ori limita superioară a normalului cu fosfatază alcalină mai mare de 6 ori limita superioară a normalului, o reducere a dozei nu poate fi recomandat și docetaxel nu trebuie utilizat decât dacă este indicat strict.
În combinație cu cisplatină și 5-fluorouracil pentru tratamentul pacienților cu adenocarcinom gastric, studiul clinic pivot a exclus pacienții cu ALT și / sau AST> 1,5 ori limita superioară a normalului asociată cu o valoare a fosfatazei alcaline.> 2,5 ori limita superioară de normal și la o valoare a bilirubinei> 1 ori limita superioară a normalului; pentru acești pacienți, nu se poate recomanda reducerea dozei și docetaxel nu trebuie utilizat decât dacă este strict indicat.Nu sunt disponibile date privind pacienții cu insuficiență hepatică tratați cu docetaxel în asociere în celelalte indicații.
Pacienți cu insuficiență renală:
Nu există date disponibile la pacienții cu insuficiență renală severă care primesc tratament cu docetaxel.
Sistem nervos:
Apariția neurotoxicității periferice severe necesită reducerea dozei (vezi pct. 4.2).
Toxicitate cardiacă:
Insuficiența cardiacă a fost observată la pacienții tratați cu docetaxel în asociere cu trastuzumab, în special după chimioterapie care conține antracicline (doxorubicină sau epirubicină).
Aceasta sa dovedit a fi moderată până la severă și a fost asociată cu decesul (vezi pct. 4.8).
Când pacienții sunt candidați la docetaxel în combinație cu contrastuzumab, aceștia ar trebui să fie supuși unei evaluări cardiace inițiale. Funcția cardiacă trebuie monitorizată în continuare în timpul tratamentului (de exemplu, la fiecare trei luni) pentru a identifica pacienții care pot dezvolta anomalii cardiace. Consultați rezumatul caracteristicilor produsului pentru trastuzumab pentru mai multe detalii.
Alte:
Măsurile contraceptive trebuie utilizate în timpul tratamentului atât pentru bărbați cât și pentru femei și pentru bărbați timp de cel puțin șase luni după întreruperea acestuia (vezi pct. 4.6).
Precauții suplimentare pentru tratamentul adjuvant al cancerului de sân
Neutropenie complicată:
Pentru pacienții care prezintă neutropenie complicată (neutropenie prelungită, neutropenie febrilă sau infecție), trebuie avute în vedere terapia G-CSF și reducerea dozei (vezi pct. 4.2).
Evenimente adverse gastrointestinale:
Simptome precum dureri abdominale și stare generală de rău, febră, diaree cu sau fără neutropenie, ar putea fi manifestări timpurii ale toxicității gastrointestinale severe și ar trebui evaluate și tratate imediat.
Insuficiență cardiacă congestivă:
Pacienții trebuie urmăriți pentru simptome care pot duce la insuficiență cardiacă congestivă în timpul tratamentului și în perioada de urmărire.
Leucemie:
La pacienții tratați cu docetaxel, doxorubicină și ciclofosfamidă (TAC), riscul mielodisplaziei întârziate sau leucemiei mieloide necesită o urmărire hematologică.
Pacienți cu 4 sau mai mulți ganglioni limfatici pozitivi:
Bilanțul beneficiu-risc al terapiei CT la pacienții cu 4 sau mai mulți ganglioni limfatici pozitivi nu este pe deplin stabilit odată cu analiza intermediară (vezi pct. 5.1).
Persoane în vârstă:
Sunt disponibile date limitate la pacienții cu vârsta peste 70 de ani tratați cu docetaxel în asociere cu doxorubicină și ciclofosfamidă.
Într-un studiu de cancer de prostată efectuat pe 333 de pacienți tratați cu docetaxel la fiecare trei săptămâni, 209 aveau 65 de ani sau mai mult și 68 de pacienți cu vârsta peste 75 de ani. La pacienții tratați cu docetaxel la fiecare trei săptămâni, incidența modificărilor plăcilor de unghii legate de la pacienții cu vârsta de 65 de ani sau peste, au fost cu peste 10% mai mari decât la pacienții mai tineri. Incidența febrei legate de medicamente, diaree, anorexie și edem periferic la pacienții cu vârsta de 75 de ani și peste a fost cu peste 10% mai mare decât la pacienții cu vârsta sub 65 de ani.
Dintre cei 300 de pacienți (221 în studiul de fază III și 79 în studiul de fază II) tratați cu docetaxel în combinație cu cisplatină și 5-fluorouracil în studiul cancerului gastric, 74 aveau 65 de ani sau mai mult și 4 aveau 75 de ani sau mai mult. Incidența evenimentelor adverse grave a fost mai mare la vârstnici comparativ cu pacienții mai tineri.Incidența evenimentelor adverse a fost mai mare la vârstnici decât la pacienții tineri. Incidența următoarelor evenimente adverse (toate gradele): letargie, stomatită și infecție neutropenică a apărut cu o frecvență> 10% la pacienții cu vârsta de 65 de ani sau peste, comparativ cu pacienții mai tineri. Pacienții vârstnici tratați cu TCF trebuie monitorizați cu mare atenție.
04.5 Interacțiuni cu alte medicamente și alte forme de interacțiune
Studiile in vitro au arătat că metabolismul docetaxelului poate fi modificat prin administrarea concomitentă de compuși care induc sau inhibă citocromul P450-3A sau care sunt metabolizați de acesta (și, prin urmare, pot inhiba competitiv enzima), cum ar fi ciclosporina, terfenadina, ketoconazolul. , eritromicină și troleandomicină Prin urmare, trebuie să se acorde prudență la tratarea concomitentă a pacienților cu astfel de medicamente, din cauza riscului potențial de interacțiuni importante.
Docetaxel este puternic legat de proteine (> 95%). Deși posibila interacțiune in vivo dintre docetaxel și terapiile concomitente nu a fost investigată în mod specific, interacțiunile in vitro dintre medicamentele strâns legate de proteine, cum ar fi eritromicina, difenhidramina, propranololul, propafenona, fenitoina, salicilații, sulfametoxazolul și valproatul de sodiu nu au afectat legarea de docetaxel la proteine. Mai mult, dexametazona nu modifică legarea de proteine a docetaxelului. Docetaxel nu afectează legarea digitoxinei. Farmacocinetica docetaxelului, doxorubicinei și ciclofosfamidei nu a interferat în timpul administrării lor concomitente. Datele limitate dintr-un singur studiu necontrolat par să indice o interacțiune între docetaxel și carboplatină.Când a fost utilizat în asociere cu docetaxel, clearance-ul carboplatinei a fost cu aproximativ 50% mai mare decât valorile raportate anterior numai pentru utilizare.
Farmacocinetica docetaxelului în prezența prednisonului a fost studiată la pacienții cu cancer de prostată metastatic. Docetaxel este metabolizat de CYP3A4, iar prednisonul provoacă inducerea CYP3A4. Nu s-a observat niciun efect semnificativ statistic al prednisonului asupra farmacocineticii docetaxelului.
Docetaxel trebuie administrat cu precauție pacienților care iau concomitent un inhibitor puternic al CYP3A4 (de exemplu, inhibitori ai proteazei, cum ar fi ritonavir, antifungici azolici, cum ar fi ketoconazol sau itraconazol). Un studiu de interacțiune medicamentoasă efectuat la pacienții care au luat ketoconazol și docetaxel a arătat că clearance-ul docetaxelului este redus la jumătate din cauza ketoconazolului, posibil deoarece metabolismul docetaxelului implică CYP3A4 ca cale metabolică predominantă. Poate apărea o toleranță redusă la docetaxel, chiar și la doze mici.
04.6 Sarcina și alăptarea
Nu există informații despre utilizarea docetaxelului la femeile gravide. În studiile efectuate la șobolani și iepuri, docetaxel este embriotoxic și fetotoxic și reduce fertilitatea la șobolani. motiv pentru care docetaxel nu trebuie administrat gravidelor decât dacă este indicat în mod clar.
Femeile aflate la vârsta fertilă / contracepția:
Femeile aflate la vârsta fertilă, care sunt tratate cu docetaxel, trebuie sfătuite să evite riscul de sarcină și să anunțe imediat medicul dacă se întâmplă acest lucru.
În timpul tratamentului trebuie utilizată o metodă eficientă de contracepție.
În studiile non-clinice, docetaxel are efecte genotoxice și poate afecta fertilitatea masculină (vezi pct. 5.3). De aceea, bărbaților tratați cu docetaxel li se recomandă să nu procreeze în timpul și până la 6 luni după tratament și să se întrebe despre depozitarea spermei înainte de tratament.
Timp de hrănire:
Docetaxel este o substanță lipofilă, dar nu se știe dacă este excretat în laptele uman. În consecință, având în vedere potențialul de reacții adverse la sugar, alăptarea trebuie întreruptă în timpul tratamentului cu docetaxel.
04.7 Efecte asupra capacității de a conduce vehicule și de a folosi utilaje
Nu s-au efectuat studii privind efectele asupra capacității de a conduce vehicule sau de a folosi utilaje.
04.8 Efecte nedorite
Reacțiile adverse considerate posibil sau probabil legate de administrarea de docetaxel au fost obținute în:
1312 și 121 de pacienți care au primit docetaxel 100 mg / m2 și, respectiv, 75 mg / m2 ca monoterapie.
258 de pacienți cărora li s-a administrat docetaxel în asociere cu doxorubicină.
406 pacienți cărora li s-a administrat docetaxel în asociere cu cisplatină.
92 de pacienți tratați cu docetaxel în asociere cu trastuzumab.
255 pacienți cărora li s-a administrat docetaxel în asociere cu capecitabină.
332 de pacienți cărora li s-a administrat docetaxel în asociere cu prednison sau prednisolon (sunt prezentate reacții adverse relevante din punct de vedere clinic legate de tratament).
1276 pacienți (744 și 532 în TAX 316 și, respectiv, GEICAM 9805) care au primit docetaxel în asociere cu doxorubicină și ciclofosfamidă (sunt prezentate efecte nedorite legate de tratament relevante clinic).
300 de pacienți cu adenocarcinom gastric (221 în studiul de fază III și 79 în studiul de fază II) tratați cu docetaxel în combinație cu cisplatină și 5-fluorouracil (au apărut efecte nedorite legate de tratament din punct de vedere clinic).
174 de pacienți cu cancer de cap și gât tratați cu docetaxel în asociere cu cisplatină și 5-fluorouracil (au apărut efecte secundare importante clinic legate de tratament).
Aceste reacții au fost descrise cu criteriile comune de toxicitate NCI (gradul 3 = G3; gradul 3-4 = G3 / 4; gradul 4 = G4) și cu termenii COSTART și MedDRA. Frecvențele sunt definite ca:
foarte frecvente (≥ 1/10); frecvente (≥ 1/100 până la
În cadrul fiecărei clase de frecvență, reacțiile adverse sunt raportate în ordinea descrescătoare a severității.
Reacțiile adverse raportate cel mai frecvent în timpul utilizării docetaxelului în monoterapie sunt: neutropenia (reversibilă și necumulativă; ziua medie până la nadir a fost ziua 7 și durata medie a neutropeniei severe (anemie, alopecie, greață, vărsături, stomatită, diaree și astenie) a evenimentelor adverse de docetaxel poate fi crescută atunci când docetaxel este administrat în asociere cu alți agenți chimioterapeutici.
Pentru combinația cu trastuzumab, evenimentele adverse (toate clasele) au fost raportate ca procent de 10%. A existat o incidență crescută a evenimentelor adverse grave (40% vs. 31%) și evenimentele adverse de gradul 4 (34% vs. 23%) în grupul combinat cu trastuzumab versus monoterapia cu docetaxel. Pentru asocierea cu capecitabină, sunt raportate cele mai frecvente efecte nedorite legate de tratament (≥ 5%) observate într-un studiu clinic de fază III la pacienții cu cancer mamar după eșecul terapiei cu antraciclină (vezi rezumatul caracteristicilor produsului. Al capecitabinei).
Următoarele reacții adverse au fost frecvent observate la docetaxel:
Tulburări ale sistemului imunitar:
Reacțiile de hipersensibilitate au apărut de obicei în câteva minute de la începerea perfuziei cu docetaxel și au fost, în general, ușoare până la moderate ca severitate. Cele mai frecvente simptome raportate au fost bufeuri, erupții cutanate cu sau fără mâncărime, senzație de apăsare în piept, dureri de spate, dispnee și febră sau frisoane. Reacțiile severe au fost caracterizate prin hipotensiune arterială și / sau bronhospasm sau erupție cutanată / eritem generalizat (vezi pct. 4.4)
Tulburări ale sistemului nervos:
Dezvoltarea neurotoxicității periferice severe necesită reducerea dozei (vezi pct. 4.2 și 4.4).
Semnele senzorneurale ușoare până la moderate se caracterizează prin parestezie, disestezie sau durere, inclusiv arsură. Evenimentele neuromotorii se caracterizează în principal prin slăbiciune.
Tulburări ale pielii și ale țesutului subcutanat:
Au fost observate reacții cutanate reversibile și, în general, sunt considerate a fi ușoare până la moderate ca severitate. Reacțiile au fost caracterizate prin erupții cutanate, incluzând erupții localizate în principal la picioare și mâini (inclusiv sindromul sever mână-picior), dar și la nivelul brațelor, feței sau pieptului, asociate frecvent cu pruritul. Erupțiile au apărut, în general, în decurs de o săptămână de la perfuzia cu docetaxel. Au fost raportate mai puțin frecvent simptome severe, cum ar fi erupții urmate de descuamare, care rareori au necesitat întreruperea temporară sau permanentă a tratamentului (vezi pct. 4.2 și 4.4). Au fost raportate simptome grave. prin hipopigmentare sau hiperpigmentare, uneori durere și onicoliză.
Tulburări generale și condiții la locul administrării:
Reacțiile la locul perfuziei au fost în general ușoare și au fost caracterizate prin hiperpigmentare, inflamație, roșeață și uscăciune a pielii, flebită sau extravazare, „permeabilitate crescută” a venei.
Retenție de lichide care include cazuri de edem periferic și mai rar cazuri de revărsături pleurale, pericardice, ascită și creștere în greutate. Edemul periferic apare de obicei începând cu extremitățile inferioare și poate deveni generalizat cu o creștere în greutate de 3 kg sau mai mult. Retenția de lichid este cumulativă ca incidență și intensitate (vezi pct. 4.4).
TAXOTERE 100 mg / m2 ca monoterapie
Tulburări ale sistemului sanguin și limfatic
Rare: episoade de sângerare asociate cu trombocitopenie de grad 3/4.
Tulburări ale sistemului nervos
Datele privind reversibilitatea sunt disponibile la 35,3% dintre pacienții care au dezvoltat neurotoxicitate după tratamentul cu docetaxel 100 mg / m2 în monoterapie. Evenimentele au fost reversibile spontan în decurs de 3 luni.
Afecțiuni ale pielii și ale țesutului subcutanat
Foarte rar: un caz de alopecie nereversibilă la sfârșitul studiului. 73% din reacțiile cutanate au fost reversibile în decurs de 21 de zile.
Tulburări generale și condiții la locul administrării
Doza medie cumulativă la întreruperea tratamentului a fost mai mare de 1.000 mg / m2 și timpul mediu până la reversibilitatea retenției de lichide a fost de 16,4 săptămâni (interval 0 - 42 săptămâni). Debutul retenției moderate până la severe (doza medie cumulativă: 818,9 mg / m2) este întârziat la pacienții care au primit premedicație comparativ cu pacienții fără premedicație (doza medie cumulativă: 489,7 mg / m2); cu toate acestea, la unii pacienți, aceasta a fost raportată în timpul primelor cure de terapie.
TAXOTERE 75 mg / m2 ca monoterapie
TAXOTERE 75 mg / m2 în asociere cu doxorubicină
TAXOTERE 75 mg / m2 în asociere cu cisplatină
TAXOTERE 100 mg / m2 în asociere cu trastuzumab
Patologii cardiace
Insuficiența cardiacă simptomatică a fost raportată la 2,2% dintre pacienții care au primit docetaxel în asociere cu trastuzumab, comparativ cu 0% dintre pacienții care au primit docetaxel singur. În grupul cu docetaxel și trastuzumab, 64% dintre pacienți au primit anterior antracicline ca terapie adjuvantă, comparativ cu 55% dintre pacienții tratați numai cu docetaxel.
Tulburări ale sistemului sanguin și limfatic
Foarte frecvente: toxicitatea hematologică a fost crescută la pacienții tratați cu trastuzumab și docetaxel comparativ cu cei tratați numai cu docetaxel (neutropenie de grad 3/4 32% față de 22% conform criteriilor NCI-CTC). Rețineți că aceasta este probabil o subestimare, deoarece docetaxel în monoterapie la o doză de 100 mg / m2 este cunoscut pentru a duce la neutropenie la 97% dintre pacienți, gradul 4 la 76%, pe baza numărului redus al numărului de neutrofile. Incidența neutropeniei febrile / sepsisului neutropenic a fost, de asemenea, crescută la pacienții tratați cu Herceptin și docetaxel (23% față de 17% dintre pacienții tratați numai cu docetaxel).
TAXOTERE 75 mg / m2 în asociere cu capecitabină
TAXOTERE 75 mg / m2 în asociere cu prednison sau prednisolon
Terapia adjuvantă cu TAXOTERE 75 mg / m2 în combinație cu doxorubicină și ciclofosfamidă la pacienții cu cancer de sân nod pozitiv (TAX 316) și nod negativ (GEICAM 9805) - date cumulative:
Tulburări ale sistemului nervos
În timpul urmăririi, 12 din cei 83 de pacienți care au prezentat neuropatie senzorială periferică la sfârșitul chimioterapiei au prezentat în continuare simptome de neuropatie senzorială periferică.
Patologii cardiace
Insuficiența cardiacă congestivă (CHF) a fost raportată la 18 din 1276 de pacienți în perioada de urmărire. În studiul cu nod pozitiv (TAX316), un pacient din fiecare grup de tratament a murit din cauza insuficienței cardiace.
Afecțiuni ale pielii și ale țesutului subcutanat
În timpul urmăririi, 25 dintre cei 736 de pacienți care au prezentat alopecie la sfârșitul chimioterapiei au avut încă alopecie.
Boli ale sistemului reproductiv și ale sânului
În timpul urmăririi, 140 din cei 251 de pacienți care au prezentat amenoree la sfârșitul chimioterapiei au prezentat în continuare simptome de amenoree.
Tulburări generale și condiții la locul administrării
În timpul urmăririi, 18 din cei 112 pacienți care au prezentat edem periferic la sfârșitul chimioterapiei în studiul TAX 316 aveau încă simptome de edem periferic, în timp ce 4 din cei 5 pacienți care au prezentat limfoedem la sfârșitul chimioterapiei în GEICAM 9805 aveau încă simptome de edem periferic.simptome de limfoedem.
Leucemie acută / sindrom mielodisplazic.
La o urmărire medie de 77 de luni, leucemia acută a apărut la 1 din 532 (0,2%) pacienți care au primit docetaxel, doxorubicină și ciclofosfamidă în GEICAM 9805. Nu au fost raportate cazuri la pacienții cărora li s-a administrat fluorouracil., Doxorubicină și ciclofosfamidă. Niciunul dintre grupurile de tratament nu a fost diagnosticat niciun caz de sindrom mielodisplazic. Tabelul de mai jos arată că incidența neutropeniei de gradul 4, a neutropeniei febrile și a infecției neutropenice a fost redusă la pacienții care au primit profilaxie primară G-CSF după ce a devenit obligatorie în brațul TAC - studiul GEICAM.
Complicații neutropenice la pacienții care au primit CT cu sau fără profilaxie primară G-CSF (GEICAM 9805)
TAXOTERE 75 mg / m2 în asociere cu cisplatină și 5-fluorouracil pentru adenocarcinom gastric
Tulburări ale sistemului sanguin și limfatic
Neutropenia febrilă și infecția neutropenică au apărut la 17,2% și, respectiv, 13,5% dintre pacienți, indiferent de utilizarea G-CSF. G-CSF a fost utilizat pentru profilaxia secundară la 19,3% dintre pacienți (10,7% din cursuri). Neutropenia febrilă și infecția neutropenică au apărut, respectiv, la 12,1% și 3,4% dintre pacienții care au primit G-CSF ca profilaxie, la 15,6% și 12,9% dintre pacienții fără profilaxie cu G-CSF (vezi pct. 4.2).
TAXOTERE 75 mg / m2 în asociere cu cisplatină și 5-fluorouracil pentru cancerele de cap și gât
Chimioterapie de inducție urmată de radioterapie (TAX 323)
Chimioterapie de inducție urmată de chimioterapie (TAX324)
Experiență post-marketing:
Neoplasme benigne, maligne și nespecificate (inclusiv chisturi și polipi)
Au fost raportate cazuri foarte rare de leucemie mieloidă acută și sindrom mielodisplazic atunci când docetaxel este utilizat în asociere cu alți agenți chimioterapeutici și / sau radioterapici.
Tulburări ale sistemului sanguin și limfatic
S-au raportat supresia măduvei osoase și alte reacții adverse hematologice. Coagularea intravasculară diseminată a fost raportată adesea în asociere cu sepsis sau insuficiență multi-organică.
Tulburări ale sistemului imunitar
Au fost raportate câteva cazuri de șoc anafilactic, unele fatale.
Tulburări ale sistemului nervos
Au fost observate cazuri rare de convulsii sau pierderea temporară a cunoștinței după administrarea docetaxelului. Aceste reacții apar uneori în timpul perfuziei.
Tulburări oculare
Cazuri foarte rare de modificări vizuale tranzitorii (flash-uri, flash-uri de lumină, scotom) și în asociere cu reacții de hipersensibilitate au apărut în mod obișnuit în timpul perfuziei medicamentului, acestea fiind reversibile după întreruperea perfuziei. Au fost raportate rareori cazuri de lacrimare cu sau fără conjunctivită, cum ar fi cazurile de obstrucție a canalelor lacrimale ca urmare a unei rupturi excesive.
Tulburări ale urechii și labirintului
Au fost raportate cazuri rare de ototoxicitate, tulburări auditive și / sau pierderi auditive.
Patologii cardiace
Au fost raportate cazuri rare de infarct miocardic.
Patologii vasculare
Au fost raportate rareori evenimente tromboembolice venoase.
Tulburări respiratorii, toracice și mediastinale
S-au raportat rareori sindromul de detresă respiratorie acută, pneumonia interstițială și fibroza pulmonară. Au fost raportate cazuri rare de pneumonie indusă de radiații la pacienții supuși, de asemenea, la radioterapie.
Tulburări gastrointestinale
Au fost raportate episoade rare de deshidratare ca o consecință a tulburărilor gastro-intestinale, a perforației gastro-intestinale, a colitei ischemice, a colitei și a enterocolitei neutropenice. Au fost raportate cazuri rare de obstrucție ileală și intestinală.
Tulburări hepatobiliare
Au fost raportate cazuri foarte rare de hepatită, uneori letală, la pacienții cu boală hepatică preexistentă.
Afecțiuni ale pielii și ale țesutului subcutanat
Cazuri de lupus eritematos erupții cutanate și buloase, cum ar fi eritemul multiform, sindromul Stevens-Johnson, necroliza epidermică toxică. În unele cazuri, alți factori concomitenți ar fi putut contribui la dezvoltarea acestor efecte. Manifestări asemănătoare schlerodermiei, de obicei precedate de limfedem periferic, au fost raportate în timpul tratamentului cu docetaxel.
Tulburări generale și condiții la locul administrării
Rareori au fost raportate fenomene de rechemare a radiațiilor.
Retenția de lichide nu a fost asociată cu episoade acute de oligurie sau hipotensiune arterială. Deshidratarea și edemul pulmonar au fost rareori raportate.
04.9 Supradozaj
Au fost raportate unele cazuri de supradozaj. Nu se cunoaște un antidot pentru supradozajul cu docetaxel. În caz de supradozaj, pacientul trebuie ținut într-o unitate specializată și funcțiile vitale trebuie monitorizate cu atenție.În caz de supradozaj, se poate aștepta o exacerbare a evenimentelor adverse. Principalele complicații de așteptat în caz de supradozaj sunt supresia măduvei osoase, neurotoxicitatea periferică și mucozita. Pacienții trebuie să primească G-CSF terapeutic cât mai curând posibil după dovezi de supradozaj. Trebuie luate alte măsuri simptomatice adecvate, după cum este necesar.
05.0 PROPRIETĂȚI FARMACOLOGICE
05.1 Proprietăți farmacodinamice
Grupa farmacoterapeutică: taxani, codul ATC: L01CD 02
Date preclinice:
Docetaxel este un medicament antineoplazic care acționează prin promovarea agregării tubulinei în microtubuli stabili și inhibă descompunerea acestora, ducând astfel la o scădere semnificativă a tubulinei libere. Legarea docetaxelului la microtubuli nu modifică numărul de protofilamente. in vitro rupe sistemul microtubular celular, care este esențial pentru funcțiile celulare vitale, cum ar fi mitoza și interfaza.
Docetaxel in vitro este citotoxic pentru diferite linii tumorale umane și șoareci și tumori umane îndepărtate recent în testele clonogene efectuate. Docetaxel atinge concentrații intracelulare ridicate și de lungă durată. Mai mult, docetaxel este activ pe unele dintre liniile celulare (dar nu pe toate) care exprimă un exces de glicoproteină p, codificată de gena de rezistență la mai multe medicamente. In vivo, docetaxel are un spectru larg de acțiune împotriva tumorilor murine avansate și a tumorilor umane altoite, indiferent de regimul de dozare.
Date clinice:
Cancer mamar
TAXOTERE în combinație cu doxorubicină și ciclofosfamidă: tratament adjuvant.
Pacienți cu cancer mamar operabil pozitiv la nod (TAX 316)
Datele dintr-un studiu deschis, randomizat, multicentric, susțin utilizarea docetaxelului ca tratament adjuvant la pacienții cu cancer mamar operabil pozitiv și KPS 3 80% cu vârsta cuprinsă între 18 și 70 de ani. După stratificarea după numărul de ganglioni limfatici pozitivi (1-3 , peste 4), 1491 de pacienți au fost randomizați pentru a primi docetaxel 75 mg / m2 administrat la 1 oră după doxorubicină 50 mg / m2 și ciclofosfamidă 500 mg / m2 (grup TAC) sau doxorubicină 50 mg / m2 urmată de fluorouracil 500 mg / m2 și ciclofosfamidă 500 mg / m2 (grup FAC). Ambele regimuri au fost administrate o dată la 3 săptămâni timp de 6 cicluri. Docetaxel a fost administrat sub formă de perfuzie de 1 oră, toate celelalte medicamente au fost administrate sub formă de bolus intravenos în ziua 1. G-CSF a fost administrat ca profilaxie secundară la pacienții cu neutropenie complicată (neutropenie febrilă, neutropenie prelungită sau infecție).
Pacienții din grupul TAC au primit profilaxie cu antibiotice cu ciprofloxacină 500 mg pe cale orală sau antibiotice echivalente de două ori pe zi timp de 10 zile începând cu ziua 5 a fiecărui ciclu. În ambele grupuri, după ultimul curs de chimioterapie, pacienții pozitivi pentru receptorii de estrogen și / sau progestogen au primit tamoxifen 20 mg / zi timp de 5 ani. % dintre pacienții care au primit TAC și până la 72% dintre pacienții care au primit FAC.
O analiză intermediară a fost efectuată la o monitorizare mediană de 55 de luni. Supraviețuirea fără boală a fost semnificativ crescută în grupul TAC comparativ cu grupul FAC.
Incidența recidivei de 5 ani a fost redusă la pacienții care au primit TAC comparativ cu cei care au primit FAC (25% vs 32%, respectiv), adică o reducere absolută a riscului de 7% (p = 0,001). Supraviețuirea globală la 5 ani a fost a crescut cu TAC comparativ cu FAC (87% vs 81% respectiv) adică o reducere absolută cu 6% a riscului de deces (p = 0,008). Au fost analizate subgrupurile de pacienți tratați cu TAC în conformitate cu principalii factori de prognostic definiți a priori:
* raportul de pericol mai mic de 1 indică faptul că TAC este asociat cu supraviețuirea fără boală și supraviețuirea generală superioară FAC
La analiza intermediară, avantajul terapeutic al TAC la pacienții cu 4 sau mai mulți ganglioni limfatici (37% din populație) nu a fost demonstrat. Avantajul terapeutic al TAC pare a fi mai puțin evident decât cel observat la pacienții cu 1 până la 3 limfa pozitivă Prin urmare, raportul risc / beneficiu la pacienții cu 4 sau mai mulți ganglioni limfatici pozitivi nu a fost complet definit în acest stadiu de analiză.
Pacienți cu candidați la cancer de sân cu nod negativ operabili pentru chimioterapie (GEICAM 9805):
Datele dintr-un studiu multicentric, deschis, randomizat, susțin utilizarea TAXOTERE pentru terapia adjuvantă la pacienții cu cancer de sân operabil cu nod negativ care sunt candidați la chimioterapie.1060 de pacienți au fost randomizați pentru a primi TAXOTERE 75 mg / m2 administrat la 1 oră după doxorubicină. mg / m2 și ciclofosfamidă 500 mg / m2 (539 pacienți în brațul TAC), sau doxorubicină 50 mg / m2 urmată de fluorouracil 500 mg / m2 și ciclofosfamidă 500 mg / m2 (521 pacienți din brațul FAC) ca terapie adjuvantă în cancer a ganglionului limfatic operabil cu sân negativ cu risc crescut de recidivă conform criteriilor St. Gallen din 1998 (dimensiunea tumorii> 2 cm și / sau ER și PR negativ și / sau grad histologic / nuclear ridicat (gradul 2 până la 3) și / sau vârstă
Durata mediană a urmăririi a fost de 77 de luni. O creștere semnificativă statistic a supraviețuirii fără boală a fost demonstrată pentru brațul TAC comparativ cu brațul FAC. Pacienții tratați cu TAC au avut o reducere cu 32% a riscului de recidivă comparativ cu cei tratați cu FAC (raport de pericol = 0,68, IC 95% (0,49-0,93), p = 0,01). Supraviețuirea globală (OS) a fost, de asemenea, mai lungă în brațul TAC, cu o reducere de 24% a riscului de deces la pacienții tratați cu TAC comparativ cu FAC (raport de risc = 0,76, IC 95% (0,46-1, 26, p = 0,29) Cu toate acestea, distribuția supraviețuirii globale nu a fost semnificativ diferită între cele două grupuri.
Subgrupurile de pacienți tratați cu TAC au fost analizate împărțite în funcție de factorii prognostici majori definiți prospectiv (a se vedea tabelul de mai jos):
Analiza subgrupurilor - Studiul terapiei adjuvante la pacienții cu cancer de sân cu nod negativ (analiza intenției de a trata)
* un raport de pericol (TAC / FAC) mai mic de 1 indică faptul că TAC este asociat cu o supraviețuire mai lungă fără boală decât FAC.
Au fost efectuate analize de subgrupuri exploratorii pentru supraviețuirea fără boală la pacienții care îndeplinesc criteriile St. Gallen din 2009 pentru chimioterapie - (populația ITT) și sunt prezentate în tabelul de mai jos:
TAC = docetaxel, doxorubicină și ciclofosfamidă
FAC = 5-fluorouracil, doxorubicină și ciclofosfamidă
CI = interval de încredere; ER = receptor de estrogen
PR = receptor de progesteron
un ER / PR-negativ sau de gradul 3 sau dimensiunea tumorii> 5 cm
Raportul de pericol a fost estimat cu modelul de pericol proporțional Cox folosind grupul de terapie ca factor.
TAXOTERE ca singurul tratament
Două studii comparative randomizate de fază III cu docetaxel la dozele recomandate și un regim de 100 mg / m2 la fiecare 3 săptămâni au fost efectuate la pacienții cu cancer de sân metastatic, dintre care 326 după eșecul tratamentului alchilant și 392 după eșec.un tratament cu antracicline.
La pacienții la care tratamentul cu agenți alchilanți sa dovedit a fi ineficient, docetaxel a fost comparat cu doxorubicina (75 mg / m2 la fiecare 3 săptămâni). Docetaxel a crescut rata de răspuns (52% față de 37%, p = 0,01) și a scăzut timpul de răspuns (12 săptămâni față de 23 săptămâni, p = 0,007), fără a modifica timpul de supraviețuire (15 luni pentru docetaxel față de 14 luni pentru doxorubicină, p = 0,38) sau timpul până la progresie (27 săptămâni pentru docetaxel versus 23 săptămâni pentru doxorubicină, p = 0,54). Trei pacienți tratați cu docetaxel (2%) au trebuit să întrerupă tratamentul din cauza retenției de lichide, în timp ce 15 pacienți tratați cu doxorubicină (9%) au trebuit să întrerupă din cauza toxicității cardiace (trei decese din cauza insuficienței cardiace congestive).
La pacienții al căror tratament cu antraciclină a fost ineficient, docetaxel a fost comparat cu combinația de mitomicină C și vinblastină (12 mg / m2 la fiecare 6 săptămâni și 6 mg / m2 la fiecare 3 săptămâni). Docetaxel a crescut rata de răspuns (33% vs 12%, p
Profilul de tolerabilitate al docetaxelului în timpul acestor două studii de fază III a fost în conformitate cu profilul de tolerabilitate găsit în studiile de fază II (vezi pct. 4.8).
Un studiu randomizat, deschis, multicentric, de fază III, care a comparat monoterapia cu docetaxel cu paclitaxel, a fost efectuat în tratamentul cancerului de sân avansat la pacienții la care terapia anterioară a inclus deja o „antraciclină. Un total de 449 de pacienți au fost randomizați pentru a primi fie monoterapia cu docetaxel 100 mg / m2 sub formă de perfuzie de 1 oră sau paclitaxel 175 mg / m2 sub formă de perfuzie de 3 ore, cele două tratamente fiind administrate la fiecare 3 săptămâni.
Docetaxel a prelungit timpul mediu până la progresie (24,6 săptămâni vs 15,6 săptămâni; p
TAXOTERE în asociere cu doxorubicină
Un studiu randomizat de fază III a fost efectuat la 429 pacienți cu cancer metastatic netratat, comparând doxorubicina (50 mg / m2) în asociere cu docetaxel (75 mg / m2) (brațul AT) cu doxorubicina (60 mg / m2). ciclofosfamidă (600 mg / m2) (braț AC). Ambele regimuri au fost administrate în ziua 1 la fiecare trei săptămâni.
Timpul până la progresie (TTP) a fost semnificativ crescut în brațul AT comparativ cu cel al brațului AC, p = 0,0138. TTP median a fost de 37,3 săptămâni (IC 95%: 33,4 - 42,1) în brațul AT și 31,9 săptămâni (IC 95%: 27,4 - 36,0) în brațul AC.
Rata de răspuns observată a fost semnificativ mai mare în brațul AT decât în brațul AC, p = 0,009. Această rată a fost de 59,3% (IC 95%: 52,8 - 65,9) în brațul AT comparativ cu 46,5% (IC 95%: 39,8 - 53,2) în brațul CA.
În acest studiu, brațul AT a avut o incidență mai mare decât brațul AC de neutropenie severă (90% vs 68,6%), neutropenie febrilă (33,3% vs 10%), infecții (8% vs 2,4%), diaree (7,5% vs. 1,4%), astenie (8,5% vs 2,4%) și durere (2,8% vs 0%). Pe de altă parte, brațul cu AC a prezentat o incidență mai mare a anemiei severe decât brațul AT (15,8% față de 8,5%) și o incidență mai mare a toxicității cardiace: insuficiență cardiacă congestivă (3,8% față de 2, 8%), scădere absolută a LVEF 3 20% (13,1% vs 6,1%), scăderea absolută a FEVS ≥ 30% (6,2% vs 1,1%). Moartea toxică a apărut la 1 pacient din brațul AT (insuficiență cardiacă congestivă) și la 4 pacienți din brațul CA (1 din cauza șocului septic și 3 din cauza insuficienței cardiace congestive).
În ambele brațe, calitatea vieții, măsurată cu chestionarul EORTC, a fost comparabilă și stabilă în timpul tratamentului și al monitorizării.
TAXOTERE în asociere cu trastuzumab
Docetaxel în asociere cu trastuzumab a fost evaluat în tratamentul pacienților cu cancer de sân metastatic care supraexprimă HER2 și care nu au primit anterior chimioterapie pentru boala metastatică. 186 de pacienți au fost randomizați pentru a primi docetaxel (100 mg / m2) cu sau fără trastuzumab; 60% dintre pacienți au primit anterior chimioterapie adjuvantă cu antracicline. Docetaxel cu trastuzumab a fost eficient la pacienții care au primit sau nu au primit anterior terapie adjuvantă cu antraciclină. Testul cel mai frecvent utilizat pentru a determina pozitivitatea HER2 în acest studiu pivot a fost imunohistochimia (IHC). Fluorescența test in situ (FISH) a fost utilizată pentru un număr mai mic de pacienți. În acest studiu, 87% dintre pacienți au prezentat boală cu IHC 3+ și 95% dintre pacienții înrolați au avut boală IHC 3+ și / sau FISH pozitiv. Rezultatele eficacității sunt rezumate în tabelul de mai jos:
TTP = timpul până la progresie; „ne” indică faptul că nu poate fi estimat sau nu a fost încă
întinse mâna.
1 Populația intenționată de tratat
2 Supraviețuirea mediană estimată
TAXOTERE în asociere cu capecitabină
Datele dintr-un studiu clinic multicentric, randomizat, controlat de fază III, susțin utilizarea docetaxelului în asociere cu capecitabină pentru tratamentul pacienților cu cancer de sân local avansat sau metastatic după eșecul chimioterapiei citotoxice care a inclus o antraciclină. În acest studiu, 255 pacienți au fost randomizați la tratament cu docetaxel (75 mg / m2 sub formă de perfuzie intravenoasă de 1 oră la fiecare 3 săptămâni) și capecitabină (1250 mg / m2 de două ori pe zi timp de 2 săptămâni, urmată de o perioadă de odihnă de 1 săptămână). 256 de pacienți au fost randomizați la tratament cu docetaxel singur (100 mg / m2 sub formă de perfuzie intravenoasă de 1 oră la fiecare 3 săptămâni). Supraviețuirea a fost superioară în brațul combinat docetaxel + capecitabină (p = 0,0126). Supraviețuirea mediană a fost de 442 zile (docetaxel + capecitabină) comparativ cu 352 zile (docetaxel singur). Rata generală de răspuns obiectiv în întreaga populație randomizată (evaluarea investigatorului) a fost de 41,6% (docetaxel + capecitabină) comparativ cu 29,7% (docetaxel singur); p = 0,0058.
Cancer pulmonar cu celule mici
Pacienți tratați anterior cu chimioterapie cu sau fără radioterapie
Într-un studiu clinic de fază III, la pacienții tratați în prealabil, timpul până la progresie (12,3 săptămâni față de 7 săptămâni) și supraviețuirea au fost semnificativ crescute cu docetaxel la 75 mg / m2 comparativ cu cel mai bun tratament de susținere (MTS).
Rata de supraviețuire la 1 an a fost semnificativ mai mare cu docetaxel (40%) decât cu MTS (16%).
Mai puțină morfină a fost utilizată la pacienții tratați cu docetaxel la 75 mg / m2 (p analgezice non-morfine (p
La pacienții evaluabili, rata generală de răspuns a fost de 6,8%, iar durata medie a răspunsului a fost de 26,1 săptămâni.
TAXOTERE în combinație cu derivați de platină la pacienții tratați niciodată cu chimioterapie
Într-un studiu de fază III, 1218 pacienți cu cancer pulmonar in stadiul IIIB sau IV inoperabil cu celule non-mici, cu statutul de performanță Karnofsky de 70% și peste, care nu primiseră chimioterapie anterioară pentru această afecțiune, au fost randomizați la docetaxel (T) 75 mg / m2 ca perfuzie de o oră urmată imediat de cisplatină (TCis) 75 mg / m2 peste 30-60 minute la fiecare trei săptămâni, docetaxel 75 mg / m2 ca perfuzie de o oră în combinație cu carboplatină (ASC 6 mg / ml. min) peste 30-60 minute la fiecare trei săptămâni, sau vinorelbină (VCis) 25 mg / m2 administrată timp de 6-10 minute în zilele 1, 8, 15, 22 urmată de cisplatină 100 mg / m2 administrată în prima zi a ciclului repetată la fiecare 4 săptămâni.
Datele privind supraviețuirea, timpul mediu până la progresie și rata de răspuns pentru două brațe de studiu sunt prezentate în tabelul de mai jos.
*: Corectat pentru comparații multiple și ajustat pentru factorii de stratificare (stadiul bolii și regiunea de tratament), pe baza populației de pacienți evaluabili.
Obiectivele secundare au inclus schimbarea durerii, evaluarea globală a calității vieții prin EuroQoL-5D, scala simptomelor cancerului pulmonar (LCSS) și schimbarea stării de performanță Karnofsky. Rezultatele acestor obiective au confirmat rezultatele obiectivelor primare.
Pentru combinația docetaxel / carboplatină, nu a fost posibilă demonstrarea echivalenței sau a non-inferiorității eficacității în ceea ce privește tratamentul de referință: combinația VCis.
Cancer de prostată
Tolerabilitatea și eficacitatea docetaxelului în asociere cu prednison sau prednisolon la pacienții cu cancer hormonal refractar de prostată metastatic au fost evaluate într-un studiu randomizat multicentric de fază III. Un total de 1006 pacienți cu KPS 60 au fost randomizați la următoarele grupuri terapeutice:
Docetaxel 75 mg / m2 la fiecare 3 săptămâni timp de 10 cicluri.
Docetaxel 30 mg / m2 administrat săptămânal în primele 5 săptămâni ale unui ciclu de 6 săptămâni pentru un total de 5 cicluri.
Mitoxantronă 12 mg / m2 la fiecare 3 săptămâni timp de 10 cicluri.
Toate cele trei regimuri au fost administrate în asociere cu prednison sau prednisolon 5 mg de două ori pe zi, continuu.
Pacienții care au primit docetaxel la fiecare trei săptămâni au demonstrat o supraviețuire globală semnificativ mai lungă decât pacienții tratați cu mitoxantronă. Creșterea supraviețuirii observată în grupul tratat cu docetaxel în fiecare săptămână nu a fost semnificativă statistic în comparație cu grupul de control tratat cu mitoxantronă.
† Test stratificat de rang jurnal
* Limita pentru semnificația statistică = 0,0175
** PSA: Antigen specific prostatei
Întrucât docetaxel în fiecare săptămână a avut un profil de tolerabilitate ușor mai bun decât docetaxel la fiecare 3 săptămâni, este posibil ca unii pacienți să beneficieze de tratament săptămânal cu docetaxel.
Nu a existat nicio diferență semnificativă statistic în Calitatea generală a vieții între grupurile de tratament.
Adenocarcinom gastric
Un studiu multicentric, randomizat, deschis a fost realizat pentru a evalua siguranța și eficacitatea docetaxelului în tratamentul pacienților cu adenocarcinom gastric metastatic, inclusiv adenocarcinom de joncțiune gastroesofagiană, care nu primiseră anterior chimioterapie pentru boala lor metastatică. Un total de 445 de pacienți cu KPS> 70 au fost tratați cu docetaxel (T) (75 mg / m2 în ziua 1) în combinație cu cisplatină (C) (75 mg / m2 în ziua 1) și 5-fluorouracil (F) (750 mg / m2 pe zi timp de 5 zile) sau cu cisplatină (100 mg / m2 în ziua 1) și 5-fluorouracil (1000 mg / m2 pe zi timp de 5 zile). Durata unui ciclu de tratament a fost de 3 săptămâni pentru brațul TCF și de 4 săptămâni pentru brațul CF. Numărul mediu de cicluri administrate per pacient a fost de 6 (cu un interval de 1-16) pentru brațul TCF și de 4 (cu un interval de 1-12) pentru brațul CF. Timpul până la progresie (TTP) a fost punctul final principal. Reducerea riscului de progresie a fost de 32,1% și a fost asociată cu un TTP semnificativ mai lung (p = 0,0004) pentru brațul TCF. Supraviețuirea generală a fost, de asemenea, semnificativ mai lungă (p = 0,0201) pentru brațul TCF cu o reducere a riscului de mortalitate de 22,7%. Rezultatele eficacității sunt rezumate în tabelul următor:
Eficacitatea docetaxelului în tratamentul pacienților cu adenocarcinom gastric
* Test de logrank nestratificat
Analizele de subgrup pentru vârstă, sex și rasă au favorizat în mod constant brațul TCF peste brațul CF.
O analiză de supraviețuire actualizată efectuată cu un timp mediu de urmărire de 41,6 luni nu a mai arătat o diferență semnificativă statistic, deși întotdeauna în favoarea regimului TCF și a evidențiat că beneficiul TCF față de FC este evident. Între 18 și 30 de luni de la urmărire -sus.
În general, rezultatele calității vieții (QoL) și ale beneficiilor clinice au indicat în mod constant îmbunătățiri în favoarea brațului TCF. Pacienții tratați cu TCF au avut cu 5% mai mult timp până la deteriorarea stării de sănătate la chestionarul QLQ-C30 (p = 0,0121) și un timp mai lung până la înrăutățirea definitivă a stării de performanță Karnofsky (p = 0, 0088) comparativ cu pacienții tratați cu CF .
Cancer de cap și gât
Chimioterapie de inducție urmată de radioterapie (TAX 323)
Siguranța și eficacitatea docetaxelului în tratamentul de inducție al pacienților cu carcinom cu celule scuamoase la nivelul capului și gâtului (SCCHN) au fost evaluate într-un studiu randomizat de fază III, multicentric deschis (TAX323). În acest studiu, 358 de pacienți cu SCCHN avansat inoperabil cu starea de performanță OMS 0-1 au fost randomizați de la una la două brațe Pacienții care au primit docetaxel (T) 75 mg / m2 urmat de cisplatină (P) 75 mg / m2 urmat de 5- fluorouracil (F) 750 mg / m2 zilnic ca perfuzie continuă timp de 5 zile Această schemă de dozare se administrează la fiecare trei săptămâni timp de 4 cicluri, un răspuns minim (> 25% contracție tumorală măsurată în două dimensiuni) a fost observat după 2 cicluri. La sfârșitul chimioterapiei, cu o interval minim de 4 săptămâni și maxim șapte săptămâni, pacienții pentru care boala nu progresează primesc radioterapie (RT), în conformitate cu liniile directoare instituționale, timp de 7 săptămâni. și (TPF / RT). Pacienții din brațul comparator au primit cisplatină (P) 100 mg / m2 urmat de 5-fluorouracil (F) 1000 mg / m2 zilnic timp de 5 zile. Acest regim de dozare a fost administrat la fiecare trei săptămâni timp de 4 cicluri dacă cel puțin un răspuns (reducere ≥ 25% a dimensiunii tumorale bidimensionale măsurate) a fost observat după 2 cicluri. La încheierea chimioterapiei, cu un interval minim de 4 săptămâni și un interval maxim de 7 săptămâni, pacienții la care boala nu progresase au primit radioterapie (RT) conform ghidului timp de 7 săptămâni (PF / RT). Radioterapia locoregională a fost aplicată unei fracțiuni convenționale (1,8 Gy-2,0 Gy o dată pe zi, 5 zile pe săptămână pentru o doză totală de 66 până la 70 Gy) sau regimurilor de radioterapie accelerată / hiperfracționată (de două ori pe zi, cu un interval minim de fracțiuni de 6 ore, de 5 zile pe săptămână). S-au sugerat în total 70 Gy pentru regimurile accelerate și 74 Gy pentru schemele hiperfracționate. Rezecția chirurgicală este permisă după chimioterapie, înainte sau după radioterapie. Pacienții din brațul TPF au primit ciprofloxacină orală 500 mg de două ori pe zi timp de 10 zile începând cu ziua 5 a fiecărui ciclu sau echivalent, ca profilaxie. Punctul final principal în acest studiu, supraviețuirea fără progresie (PFS), a fost semnificativ mai lung în brațul TPF decât în brațul PF, p = 0,0042 (PFS mediană: 11,4 față de 8,3 luni, respectiv) cu timp median de 33,7 luni. supraviețuirea a fost, de asemenea, semnificativ mai lungă pentru brațul TPF comparativ cu PF (OS median: 18,6 vs 14,5 luni, respectiv) cu o reducere de 28% a riscului de mortalitate, p = 0,0128. Rezultatele eficacității sunt prezentate în tabelul de mai jos:
Eficacitatea docetaxelului în tratamentul de inducție al pacienților cu SCCHN inoperabil local avansat. (Analiza intenției de a trata).
Raport de pericol mai mic de 1 în favoarea combinației docetaxel + cisplatină + 5-FU
* Model Cox (ajustare pentru locul tumorii primare, stadializare pe T și N și PS-OMS)
** Test logrank
*** Testul Chi-pătrat
Parametrii pentru a defini calitatea vieții.
Pacienții tratați cu TPF prezintă o deteriorare semnificativă a stării generale de sănătate, comparativ cu cei tratați cu PF (p = 0,01, folosind scala EORTC QLQ-C30).
Parametrii pentru a defini beneficiile clinice
Scala de performanță, pentru cap și gât (PSS-HN), care urmărea să măsoare înțelegerea vorbirii, posibilitatea de a mânca în public și normalitatea dietei, sa dovedit a fi semnificativ în favoarea brațului TPF comparativ cu brațul PF . Timpul mediu până la prima deteriorare a stării de performanță a OMS a fost semnificativ mai lung în brațul TPF comparativ cu brațul PF. Scara intensității durerii arată îmbunătățiri în timpul tratamentului în ambele grupuri, indicând faptul că gestionarea durerii este adecvată.
Chimioterapie de inducție urmată de chimioterapie (TAX324)
Siguranța și eficacitatea docetaxelului în tratamentul de inducție la pacienții cu carcinom cu celule scuamoase (SCCHN) avansat local au fost evaluate într-un studiu clinic de fază III, randomizat, deschis, multicentric (TAX 324). Studiu, 501 pacienți cu SCCHN avansat local cu starea de performanță OMS 0 sau 1 au fost randomizați la una dintre cele două brațe. Populația studiată a inclus, de asemenea, pacienți inoperabili din punct de vedere tehnic, pacienți cu probabilitate redusă de rezecție chirurgicală cu succes și pacienți care au urmărit conservarea organelor. profilul de siguranță și eficacitate a luat în considerare doar obiectivele de supraviețuire, în timp ce succesul în conservarea organelor nu a fost luat în considerare în mod formal.
Pacienții tratați cu docetaxel au primit docetaxel (T) 75 mg / m2 ca perfuzie intravenoasă în ziua 1 urmată de cisplatină (P) 100 mg / m2 administrată ca perfuzie intravenoasă cu durata de 30 minute până la trei ore, urmată de perfuzie intravenoasă continuă de 5- fluorouracil (F) 1000 mg / m2 / zi din ziua 1 până în ziua 4. Ciclurile au fost repetate la fiecare trei săptămâni timp de 3 cicluri.
Toți pacienții care nu aveau progresia bolii urmau să primească chimioterapie (CRT) conform protocolului (TPF / CRT). Pacienții din brațul de comparare au primit cisplatină (P) 100 mg / m2 administrat sub formă de perfuzie cu durata de 30 de minute până la trei ore în ziua 1, urmat de 5-fluorouracil (F) 1000 mg / m2 / zi din ziua 1 în zi. Ciclurile au fost repetate la fiecare trei săptămâni timp de 3 cicluri. Toți pacienții care nu aveau progresia bolii urmau să primească CRT-uri conforme cu protocolul (PF / CRT).
Pacienții din ambele brațe de tratament au primit 7 zile de CRT după chimioterapie de inducție cu un interval minim de 3 săptămâni și nu mai mult de 8 săptămâni după începerea ultimului ciclu (ziua 22 până în ziua 56. În timpul radioterapiei, s-a administrat carboplatină (ASC 1,5) sub formă de perfuzie intravenoasă de o oră pentru până la 7 doze. Radiația a fost administrată cu un instrument de înaltă tensiune folosind fracționarea zilnică (2Gy pe zi, 5 zile pe săptămână timp de 7 săptămâni, pentru o doză totală de 70-72 Gy). Chirurgia la locul tumorii primare și / sau gâtul ar putea fi luată în considerare în orice moment după finalizarea CRT. Toți pacienții aflați în studiu în brațul cu docetaxel au primit profilaxie cu antibiotice. Obiectivul principal al eficacității acestui studiu, supraviețuirea (OS) a fost semnificativ mai lungă (test log-rank p = 0,0058) cu regimul care conține docetaxel comparativ cu PF (OS median: 70,6 vs 30,1 luni, respectiv), cu o reducere de 30% în riscul de deces prin PF (raportul de risc (HP) = 0,70, interval de încredere 95% (IC) = 0,54-0,90) la o urmărire mediană de 41,9 luni. Obiectivul secundar, PFS, a demonstrat o riscul de progresie sau deces și o îmbunătățire a SFP mediană de 22 de luni (35,5 luni pentru TPF și 13,1 pentru FP). Acest lucru a fost, de asemenea, semnificativ statistic, cu o FC de 0,71, 95% CI 0,56-0,90; test log-rank p = 0,004. Rezultatele eficacității sunt prezentate în tabelul următor:
Raport de pericol mai mic de 1 în favoarea combinației docetaxel + cisplatină + 5-fluorouracil
* ajustare test log rank
** ajustarea testului de rang log, fără ajustări pentru comparații multiple
*** Test Chi-pătrat, fără ajustări pentru comparații multiple
NA - nu se aplică
Agenția Europeană a Medicamentului a acordat o derogare de la obligația de a furniza rezultatele studiilor cu TAXOTERE la toate subseturile de pacienți din populația pediatrică cu cancer de sân, cancer pulmonar cu celule mici, cancer de prostată, cancer gastric și cancer de cap și gât, excluzând carcinomul nazofaringian de tip II și de tip III mai puțin diferențiat (a se vedea secțiunea 4.2 pentru informații privind utilizarea la copii și adolescenți).
05.2 "Proprietăți farmacocinetice
Farmacocinetica docetaxelului a fost studiată la pacienții cu cancer după administrarea a 20-115 mg / m2 în studiile de fază I. Profilul cinetic al docetaxelului nu este dependent de doză și este în concordanță cu un model farmacocinetic cu trei compartimente, cu perioade de înjumătățire pe fază. a, b și respectiv b de 4 min., 36 min. și 11,1 ore. Faza târzie se datorează parțial revenirii relativ lente a docetaxelului din compartimentul periferic. După administrarea a 100 mg / m2 sub formă de perfuzie de o oră, s-a obținut un nivel plasmatic mediu maxim de 3,7 mcg / ml, cu o ASC corespunzătoare de 4,6 h mcg / ml. Valorile medii ale clearance-ului total și volumul de distribuție la starea de echilibru au fost 21 1 / h / m2 și 113 L. Modificările interindividuale ale clearance-ului total au fost de aproximativ 50% .Docetaxel este legat de peste 95% de proteinele plasmatice.
Un studiu cu 14C-docetaxel a fost efectuat la trei pacienți cu cancer. Docetaxel a fost eliminat atât în urină, cât și în materiile fecale prin oxidarea mediată de citocromul P 450 a grupării ester tertbutilice; în termen de șapte zile, aproximativ 6% și 75% din radioactivitatea administrată este excretată în urină și, respectiv, în materiile fecale. Aproximativ 80% din radioactivitatea găsită în materiile fecale este excretată în primele 48 de ore ca un metabolit major și trei metaboliți minori inactivi și cantități foarte mici de medicament părinte.
Un studiu farmacocinetic populațional a fost efectuat la 577 de pacienți. Parametrii farmacocinetici calculați de model au fost foarte apropiați de cei observați în studiile de fază I. Farmacocinetica docetaxelului nu a fost modificată în funcție de vârsta sau sexul pacientului. La un număr mic de pacienți (n = 23) cu rezultate biochimice. Sugerând hepatice moderate disfuncție (ALAT, ASAT 3 de 1,5 ori limita superioară a normalului, asociată cu fosfataza alcalină 3 2,5 limita superioară a normalului), clearance-ul total a scăzut în medie cu 27% (vezi pct. 4.2). Clearance-ul docetaxel nu este afectat la pacienții cu ușoară sau moderată retenție de lichide Nu există date disponibile la pacienții cu retenție severă de lichide.
Când este utilizat în asociere, docetaxel nu afectează clearance-ul doxorubicinei și nivelurile plasmatice ale doxorubicinolului (un metabolit al doxorubicinei). Farmacocinetica docetaxelului, doxorubicinei și ciclofosfamidei nu este afectată de administrarea lor concomitentă.
Un studiu de fază I care a evaluat efectele capecitabinei asupra farmacocineticii docetaxelului și invers a demonstrat că nu există niciun efect al capecitabinei asupra farmacocineticii docetaxelului (Cmax și ASC) și că nu există niciun efect al docetaxelului asupra farmacocineticii unui metabolit. relevante pentru capecitabină, 5 "-DFUR.
Clearance-ul docetaxelului în terapia combinată cu cisplatină a fost similar cu cel observat în timpul monoterapiei. Profilul farmacocinetic al cisplatinei administrat la scurt timp după perfuzia cu docetaxel este similar cu cel observat numai cu cisplatină.
Administrarea combinată de docetaxel, cisplatină și 5-fluorouracil la 12 pacienți cu tumori solide nu a avut nicio influență asupra farmacocineticii medicamentelor individuale.
Efectul prednisonului asupra farmacocineticii docetaxelului administrat cu premedicație standard cu dexametazonă a fost studiat la 42 de pacienți. Nu s-a observat niciun efect al prednisonului asupra farmacocineticii docetaxelului.
05.3 Date preclinice de siguranță
Potențialul cancerigen al docetaxelului nu a fost studiat.
Docetaxel s-a dovedit a fi mutagen în test in vitro de aberație cromozomială în celulele CHO-K1 e in vivo în testul micronucleului mouse-ului. Cu toate acestea, docetaxelul nu este mutagen în testul Ames sau testul mutației genei CHO / HGPRT. Aceste rezultate sunt în concordanță cu activitatea farmacologică a docetaxelului.
Efectele nedorite asupra organelor genitale masculine, observate în studiile de toxicitate la rozătoare, sugerează că docetaxel poate afecta fertilitatea masculină.
06.0 INFORMAȚII FARMACEUTICE
06.1 Excipienți
Flacon de concentrat:
polisorbat 80, acid citric.
Flacon cu solvent:
95% etanol, apă pentru preparate injectabile.
06.2 Incompatibilitate
Medicamentul nu trebuie amestecat cu alte produse, cu excepția celor menționate la punctul 6.6.
06.3 Perioada de valabilitate
2 ani.
Soluție pre-amestecată: soluția pre-diluată conține 10 mg / ml docetaxel și trebuie utilizată imediat după preparare, chiar dacă stabilitatea chimico-fizică a acestei soluții a fost demonstrată pentru o perioadă de 8 ore dacă este păstrată între + 2 ° C și +8 ° C sau la temperatura camerei (sub 25 ° C).
Soluție perfuzabilă: Soluția perfuzabilă, păstrată la temperatura camerei (sub 25 ° C), trebuie utilizată în decurs de 4 ore.
06.4 Precauții speciale pentru depozitare
A nu se păstra la temperaturi peste 25 ° C sau sub 2 ° C.
A se păstra în ambalajul original pentru a-l ține departe de lumină.
Pentru condițiile de păstrare a medicamentului diluat, vezi pct. 6.3.
06.5 Natura ambalajului imediat și conținutul ambalajului
Fiecare blister conține:
un flacon cu doză unică de concentrat și un flacon cu doză unică de solvent.
Flacon de TAXOTERE 20 mg / 0,5 ml concentrat pentru soluție perfuzabilă:
Flacon de sticlă transparentă de 7 ml de tip I, cu capac verde.
Flaconul conține o soluție de docetaxel în 0,5 ml de polisorbat 80 și o concentrație de 40 mg / ml (volum de umplere: 24,4 mg / 0,61 ml). Acest volum de umplere a fost stabilit în timpul dezvoltării TAXOTERE pentru a compensa pierderea de lichid în timpul preparării soluției prediluate datorită spumării, aderenței la pereții flaconului și „spațiului mort”. din flaconul cu solvent inclus cu TAXOTERE, volumul minim extractibil de soluție prediluită este de 2 ml, conținând 10 mg / ml de docetaxel care corespunde conținutului declarat pe etichetă de 20 mg / 0,5 ml pe flacon.
Flacon cu solvent:
Flacon de sticlă transparentă de tip I de 7 ml cu capac transparent incolor.
Flaconul cu solvent conține 1,5 ml soluție 13% (greutate / greutate) de etanol 95% în apă pentru preparate injectabile (volum de umplere: 1,98 ml). Adăugând întregul conținut al flaconului cu solvent la cel de TAXOTERE 20 mg / 0,5 ml, concentratul pentru soluție perfuzabilă asigură obținerea unei soluții premixate cu o concentrație de 10 mg / ml de docetaxel.
06.6 Instrucțiuni de utilizare și manipulare
TAXOTERE este un medicament antineoplazic și, ca și în cazul altor produse potențial toxice, trebuie să se acorde prudență la manipularea și prepararea soluțiilor. Se recomandă utilizarea mănușilor Dacă TAXOTERE în formă concentrată, pre-diluată sau soluție perfuzabilă trebuie să intre în contact cu pielea, se spală imediat și bine cu apă și săpun. Dacă TAXOTERE în formă concentrată, pre-diluată sau soluție perfuzabilă trebuie să intre în contact cu membranele mucoase, să se spele imediat și bine cu apă.
Pregătirea pentru administrare intravenoasă
a) Pregătirea soluției gata de utilizare a TAXOTERE (10 mg docetaxel / ml)
Dacă flacoanele sunt păstrate în frigider, lăsați numărul necesar de cutii de TAXOTERE la temperatura camerei (sub 25 ° C) timp de 5 minute.
Folosind o seringă gradată cu ac, retrageți întregul conținut al flaconului de solvent pentru TAXOTERE inversând parțial flaconul.
Injectați întregul conținut al seringii în flaconul corespunzător de TAXOTERE.
Scoateți seringa și acul și amestecați soluția manual inversând în mod repetat timp de 45 de secunde. Nu agitați.
Lăsați flaconul cu soluție prediluită să stea timp de 5 minute la temperatura camerei (sub 25 ° C) și apoi verificați dacă soluția este clară și omogenă. (Spumarea este normală chiar și după 5 minute din cauza conținutului de polisorbat 80 din formulare).
Soluția prediluată conține 10 mg / ml docetaxel și trebuie utilizată imediat după preparare, chiar dacă stabilitatea chimico-fizică a acestei soluții a fost demonstrată pentru o perioadă de 8 ore dacă este păstrată între + 2 ° C și + 8 ° C sau la temperatura camerei (sub 25 ° C).
b) Pregătirea soluției pentru perfuzie
Pot fi necesare mai multe flacoane cu soluție prediluită pentru a obține doza necesară pentru pacient. Pe baza dozei necesare pentru pacient, exprimată în mg, retrageți aseptic volumul corespunzător de soluție prediluată care conține docetaxel de 10 mg / ml dintr-un număr adecvat de flacoane cu soluție prediluată folosind o seringă gradată cu ac. De exemplu, pentru o doză de 140 mg docetaxel, trebuie retrase 14 ml de soluție prediluită de docetaxel. Se injectează volumul necesar de soluție prediluită într-o pungă sau flacon de 250 ml care conține soluție de glucoză 5% sau soluție perfuzabilă cu 9 mg / ml clorură de sodiu (0,9%).
Dacă este necesară o doză de docetaxel mai mare de 200 mg, utilizați un volum mai mare de soluție perfuzabilă, astfel încât concentrația de docetaxel să nu depășească 0,74 mg / ml. Se amestecă manual punga sau sticla cu o mișcare de răsucire.
Soluția perfuzabilă TAXOTERE trebuie utilizată în decurs de 4 ore și trebuie administrată sub formă de perfuzie de 1 oră, aseptic, la temperatura camerei (sub 25 ° C) și în condiții de lumină normală.
Ca și în cazul tuturor produselor de uz parenteral, soluția prediluită și soluția de perfuzie a TAXOTERE trebuie examinate vizual înainte de utilizare, soluțiile care conțin precipitate trebuie aruncate.
Produsul neutilizat și deșeurile derivate din acest medicament trebuie eliminate în conformitate cu cerințele legale locale.
07.0 DEȚINĂTORUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
Aventis Pharma S.A., 20 Avenue Raymond Aron, 92165 Antony Cedex, Franța
08.0 NUMĂRUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
EU / 1/95/002/001
09.0 DATA PRIMEI AUTORIZĂRI SAU REÎNNOIREA AUTORIZAȚIEI
Data primei autorizații: 27 noiembrie 1995
Data ultimei reînnoiri: 27 noiembrie 2005.