Ingrediente active: Etanercept
Enbrel 25 mg pulbere și solvent pentru soluție injectabilă
Inserturile de pachete Enbrel sunt disponibile pentru dimensiunile ambalajului:- Enbrel 25 mg pulbere și solvent pentru soluție injectabilă
- Enbrel 25 mg soluție injectabilă în seringi preumplute
- Enbrel 50 mg soluție injectabilă în seringi preumplute
- Enbrel 50 mg soluție injectabilă în stilou injector (pen) preumplut
- Enbrel 10 mg pulbere și solvent pentru soluție injectabilă pentru uz pediatric
De ce se utilizează Enbrel? Pentru ce este?
Enbrel este un medicament biologic fabricat din două proteine umane. Blochează activitatea unei alte proteine care provoacă inflamații în corpul uman. Enbrel acționează prin reducerea inflamației asociate cu unele boli.
La adulți (cu vârsta de 18 ani sau peste), Enbrel poate fi utilizat pentru tratamentul artritei reumatoide moderate până la severe, a artritei psoriazice, a spondiloartritei axiale severe, inclusiv a spondilitei anchilozante și a psoriazisului moderat până la sever. nu au funcționat suficient de bine sau nu sunt potrivite pentru dvs.
Pentru artrita reumatoidă, Enbrel este de obicei utilizat în asociere cu metotrexat, deși poate fi utilizat și singur dacă tratamentul cu metotrexat nu este potrivit pentru dvs. Dacă este utilizat singur sau în combinație cu metotrexat, Enbrel poate încetini deteriorarea articulațiilor cauzată de artrita reumatoidă. și îmbunătățește capacitatea de a efectua activități zilnice normale.
Pentru pacienții cu artrită psoriazică care implică articulații multiple, Enbrel poate îmbunătăți capacitatea de a efectua activități zilnice. Pentru pacienții cu articulații simetrice multiple dureroase sau umflate (de exemplu, mâini, încheieturi și picioare), Enbrel poate încetini deteriorarea structurală a acestor articulații cauzată de boală.
Enbrel este, de asemenea, prescris pentru tratarea următoarelor afecțiuni la copii și adolescenți:
- Pentru următoarele tipuri de artrită idiopatică juvenilă, atunci când tratamentul cu metotrexat nu a dat un răspuns suficient de bun sau este inadecvat: poliartrită (factor reumatoid pozitiv sau negativ) și oligoartrită extinsă la pacienți cu vârsta de 2 ani; artrită psoriazică la pacienți începând cu vârsta din 12.
- Pentru artrita legată de entezită la pacienții de la vârsta de 12 ani, când alte tratamente utilizate pe scară largă nu au dat un răspuns suficient de bun sau nu sunt adecvate.
- Psoriazis sever la pacienții de la 6 ani care au avut un răspuns inadecvat la (sau nu pot lua) fototerapii sau alte terapii sistemice.
Contraindicații Când nu trebuie utilizat Enbrel
Nu utilizați Enbrel:
- dacă dumneavoastră sau copilul sunteți alergic la etanercept sau la oricare dintre celelalte componente ale Enbrel (enumerate la punctul 6). Dacă dumneavoastră sau copilul experimentați reacții alergice, cum ar fi senzația de apăsare a pieptului, respirație șuierătoare, amețeli sau erupții cutanate, nu injectați mai mult Enbrel și contactați imediat medicul dumneavoastră.
- dacă dumneavoastră sau copilul aveți sau riscați să dezvoltați o „infecție sanguină gravă numită sepsis. Dacă nu sunteți sigur, vă rugăm să vă adresați medicului dumneavoastră.
- dacă dumneavoastră sau copilul aveți o infecție de orice fel. Dacă nu sunteți sigur, discutați cu medicul dumneavoastră.
Precauții pentru utilizare Ce trebuie să știți înainte de a lua Enbrel
- Reacții alergice: Dacă dumneavoastră sau copilul experimentați reacții alergice, cum ar fi senzația de apăsare a pieptului, respirație șuierătoare, amețeli sau erupții cutanate, nu injectați mai mult Enbrel și contactați imediat medicul dumneavoastră.
- Infecții / Chirurgie: Dacă dumneavoastră sau copilul dumneavoastră dezvoltați o nouă infecție sau sunteți pe cale să aveți o intervenție chirurgicală majoră, medicul dumneavoastră ar putea dori să vă verifice tratamentul cu Enbrel.
- Infecții / diabet: spuneți medicului dumneavoastră dacă dumneavoastră sau copilul aveți antecedente de infecții recurente sau aveți diabet sau alte afecțiuni care cresc riscul de infecție.
- Infecții / monitorizare: Spuneți medicului dumneavoastră despre orice călătorie recentă în afara Europei. Dacă dumneavoastră sau copilul dumneavoastră prezentați simptome ale unei infecții precum febră, frisoane sau tuse, spuneți imediat medicului dumneavoastră. Medicul dumneavoastră poate decide să monitorizeze în continuare dumneavoastră sau copilul dumneavoastră pentru infecții după ce dumneavoastră sau copilul dumneavoastră ați încetat să luați Enbrel.
- Tuberculoza: Deoarece au fost raportate cazuri de tuberculoză la pacienții tratați cu Enbrel, medicul dumneavoastră vă va verifica semnele și simptomele tuberculozei înainte de a începe tratamentul cu Enbrel. Aceasta ar putea include o colecție detaliată a istoricului medical, a radiografiei toracice și a unui test de tuberculină. Rezultatele acestor teste trebuie menționate pe cardul de alertă al pacientului. Este foarte important să spuneți medicului dumneavoastră dacă dumneavoastră sau copilul ați contractat vreodată tuberculoză sau dacă ați fost în contact strâns cu cineva cu tuberculoză. tuse, scădere în greutate, slăbiciune, febră ușoară) sau orice altă infecție care apare în timpul sau după tratament, spuneți imediat medicului dumneavoastră.
- Hepatita B: Spuneți medicului dumneavoastră dacă dumneavoastră sau copilul dumneavoastră ați avut sau ați avut vreodată hepatită B. Medicul dumneavoastră trebuie să testeze hepatita B înainte ca dumneavoastră sau copilul dumneavoastră să începeți tratamentul cu Enbrel. Tratamentul cu Enbrel poate determina reactivarea hepatitei B la pacienții cu hepatită anterioară Infecția cu virusul B. Dacă da, ar trebui să încetați să utilizați Enbrel.
- Hepatita C: Spuneți medicului dumneavoastră dacă dumneavoastră sau copilul aveți hepatită C. Medicul dumneavoastră poate dori să vă monitorizeze tratamentul cu Enbrel dacă infecția se agravează.
- Tulburări ale sângelui: solicitați asistență medicală imediată dacă dumneavoastră sau copilul aveți semne sau simptome precum febră persistentă, dureri în gât, vânătăi, sângerări sau paloare. Aceste simptome pot indica prezența unor afecțiuni ale sângelui potențial periculoase pentru viață, care ar putea necesita să încetați să luați Enbrel.
- Tulburări ale sistemului nervos și ale ochilor: spuneți medicului dumneavoastră dacă dumneavoastră sau copilul aveți scleroză multiplă, nevrită optică (inflamație a nervilor optici) sau mielită transversă (inflamație a măduvei spinării). Medicul dumneavoastră va lua în considerare dacă Enbrel este un tratament adecvat.
- Insuficiență cardiacă congestivă: spuneți medicului dumneavoastră dacă dumneavoastră sau copilul aveți antecedente de insuficiență cardiacă congestivă, deoarece Enbrel trebuie utilizat cu precauție în aceste circumstanțe.
- Cancer: Spuneți medicului dumneavoastră dacă aveți sau ați avut vreodată limfom (un tip de cancer de sânge) sau orice alt cancer înainte de a lua Enbrel. Pacienții cu artrită reumatoidă severă de lungă durată pot prezenta un risc mai mare decât media de a dezvolta limfom. Copiii și adulții care iau Enbrel pot avea un risc crescut de a dezvolta limfom sau un alt cancer. Unii copii și adolescenți care au fost tratați cu Enbrel sau cu alte medicamente care funcționează ca Enbrel au dezvoltat tipuri de cancer, inclusiv tipuri neobișnuite, uneori cu un rezultat fatal. Unii pacienți care au primit Enbrel au dezvoltat cancer de piele. Spuneți medicului dumneavoastră dacă dumneavoastră sau copilul prezentați modificări ale aspectului pielii sau creșteri ale pielii.
- Varicela: Spuneți medicului dumneavoastră dacă dumneavoastră sau copilul sunteți expus la varicelă atunci când utilizați Enbrel. Medicul dumneavoastră va lua în considerare dacă tratamentul preventiv al varicelei este adecvat.
- Latex: Capacul acului este fabricat din latex (cauciuc natural uscat). Contactați medicul înainte de a utiliza Enbrel dacă capacul acului este manipulat sau dacă Enbrel este administrat unei persoane cu hipersensibilitate (alergie) cunoscută sau posibilă la latex.
- Abuzul de alcool: Enbrel nu trebuie utilizat pentru tratarea hepatitei asociate alcoolului. Spuneți medicului dumneavoastră dacă dumneavoastră sau copilul aveți antecedente de abuz de alcool.
- Granulomatoza Wegener: Enbrel nu este recomandat pentru tratamentul granulomatozei Wegener, o boală inflamatorie rară. Dacă dumneavoastră sau copilul aveți granulomatoza Wegener, vă rugăm să vă adresați medicului dumneavoastră.
- Medicamente anti-diabet: Spuneți medicului dumneavoastră dacă dumneavoastră sau copilul aveți diabet sau dacă luați medicamente pentru tratamentul diabetului. Medicul dumneavoastră poate decide dacă dumneavoastră sau copilul dumneavoastră aveți nevoie de mai puține medicamente pentru diabet în timp ce luați Enbrel.
Copii și adolescenți
- Vaccinări: dacă este posibil, copiii trebuie să fie la curent cu toate vaccinările înainte de a utiliza Enbrel. Unele vaccinuri, cum ar fi vaccinul oral împotriva poliomielitei, nu trebuie administrate în timp ce luați Enbrel. Consultați-vă medicul înainte ca dumneavoastră sau copilul dumneavoastră să primiți vaccinuri.
- Boală inflamatorie intestinală (IBD): Au existat cazuri de boală inflamatorie intestinală la pacienții cu artrită idiopatică juvenilă (AIJ) tratați cu Enbrel. Spuneți medicului dumneavoastră dacă copilul dumneavoastră are crampe abdominale și dureri, diaree, scădere în greutate sau sânge în scaun.
Enbrel nu trebuie utilizat în mod normal la copii cu poliartrită sau oligoartrită extinsă cu vârsta mai mică de 2 ani sau la copii cu artrită asociată cu entezită sau artrită psoriazică cu vârsta mai mică de 12 ani sau la copii cu psoriazis cu vârsta sub 6 ani. .
Interacțiuni Ce medicamente sau alimente pot schimba efectul Enbrel
Spuneți medicului dumneavoastră sau farmacistului dacă dumneavoastră sau copilul luați, ați luat recent sau ați putea lua orice alte medicamente (inclusiv anakinra, abatacept sau sulfasalazină), chiar și cele obținute fără prescripție medicală. Tu sau copilul nu trebuie să utilizați Enbrel împreună cu substanța activă anakinra sau abatacept.
Avertismente Este important să știm că:
Sarcina și alăptarea
Efectele Enbrel asupra femeilor gravide nu sunt cunoscute, prin urmare nu se recomandă utilizarea Enbrel în timpul sarcinii. Femeile care utilizează Enbrel ar trebui să evite să rămână gravide.
Dacă dumneavoastră sau fata / fetița rămâneți gravidă, trebuie să vă adresați medicului dumneavoastră. Dacă dumneavoastră sau fata / fetița ați primit Enbrel în timpul sarcinii, copilul poate avea un risc crescut de infecție. Este important să avertizați pediatrii sugari și alți profesioniști din domeniul sănătății cu privire la utilizarea Enbrel în timpul sarcinii înainte ca sugarul să primească vreun vaccin (pentru mai multe informații, consultați secțiunea 2, „Vaccinări”).
Femeile care utilizează Enbrel nu trebuie să alăpteze, deoarece Enbrel este excretat în laptele matern.
Efecte asupra capacității de a conduce vehicule și de a folosi utilaje
Nu este de așteptat ca utilizarea Enbrel să vă afecteze capacitatea de a conduce vehicule sau de a folosi utilaje.
Doză, metodă și timp de administrare Cum se utilizează Enbrel: Doze
Utilizați întotdeauna Enbrel exact așa cum v-a spus medicul dumneavoastră. Dacă aveți dubii, consultați medicul sau farmacistul.
Dacă aveți impresia că efectul Enbrel este prea puternic sau prea slab, discutați cu medicul dumneavoastră sau cu farmacistul.
Doze pentru adulți (cu vârsta de 18 ani sau peste)
Artrita reumatoidă, artrita psoriazică și spondiloartrita axială, inclusiv spondilita anchilozantă
Doza uzuală este de 25 mg administrată de două ori pe săptămână sau 50 mg o dată pe săptămână prin injecție subcutanată. În fiecare caz, medicul dumneavoastră poate stabili o frecvență diferită la care să injectați Enbrel.
Psoriazisul plăcii
Doza uzuală este de 25 mg administrată de două ori pe săptămână sau 50 mg administrată o dată pe săptămână.
Alternativ, se poate administra o doză de 50 mg administrată de două ori pe săptămână timp de până la 12 săptămâni, urmată de o doză de 25 mg administrată de două ori pe săptămână sau o doză de 50 mg administrată o dată pe săptămână.
Medicul dumneavoastră va decide cât timp trebuie să luați Enbrel și dacă, pe baza răspunsului dumneavoastră, este necesar un nou tratament. Dacă, după 12 săptămâni, Enbrel nu are niciun efect asupra bolii dumneavoastră, medicul dumneavoastră vă poate spune să întrerupeți tratamentul.
Utilizare la copii și adolescenți
Doza și frecvența de dozare adecvate pentru copilul sau adolescentul dvs. vor depinde de greutatea corporală și de boală. Medicul dumneavoastră vă va oferi informații detaliate despre modul de preparare și măsurare a dozei adecvate.
Pentru poliartrită sau oligoartrită extinsă la pacienți cu vârsta de 2 ani sau artrită legată de entezită sau artrită psoriazică la pacienți cu vârsta de peste 12 ani, doza uzuală este de 0,4 mg Enbrel per kg de greutate corporală (până la maximum 25 mg ), administrat de două ori pe săptămână sau 0,8 mg de Enbrel pe kg de greutate corporală (până la maximum 50 mg) administrat o dată pe săptămână.
Pentru psoriazis la pacienții cu vârsta de 6 ani și peste, doza uzuală este de 0,8 mg Enbrel pe kilogram de greutate corporală (până la maximum 50 mg) și trebuie administrată o dată pe săptămână. Dacă Enbrel nu are niciun efect asupra stării bebelușului dumneavoastră după săptămâni, medicul dumneavoastră vă poate spune să încetați să luați acest medicament.
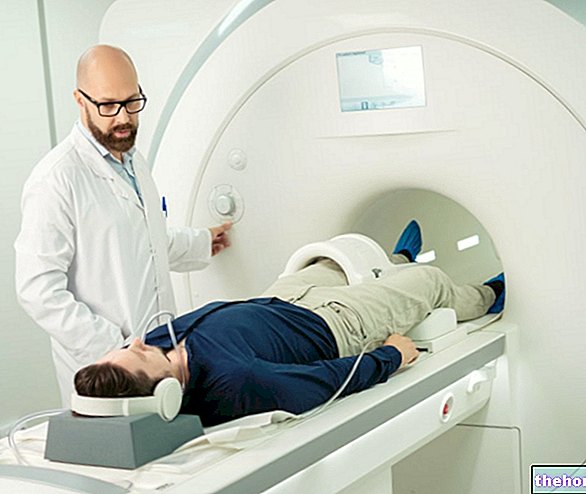
Metoda și calea de administrare
Enbrel se administrează prin injecție sub piele (injecție subcutanată).
Enbrel poate fi luat cu sau fără alimente și băuturi.
Pulberea trebuie dizolvată înainte de utilizare Instrucțiuni detaliate despre modul de preparare și injectare a Enbrel sunt furnizate în secțiunea 7, Instrucțiuni pentru prepararea și administrarea unei injecții cu Enbrel. Nu amestecați soluția Enbrel cu alte medicamente.
Pentru a vă ajuta să vă amintiți, poate fi util să scrieți într-un jurnal care zi (zile) din săptămână trebuie utilizat Enbrel.
Instrucțiuni pentru pregătirea și administrarea unei injecții cu Enbrel
Introducere
Următoarele instrucțiuni explică modul de preparare și injectare a Enbrel. Citiți cu atenție instrucțiunile și urmați-le pas cu pas. Veți fi instruit de către medicul sau asistenta dumneavoastră cu privire la tehnica de auto-injectare sau la administrarea unei injecții la un copil. Un "ghid de preparare a dozelor" (special realizat pe partea inferioară a tăvii) este furnizat pentru a vă ajuta să aliniați flaconul și seringa cu solvent. Nu încercați să administrați o injecție până nu sunteți sigur că înțelegeți cum să vă pregătiți și cum să faceți injecţie. Această injecție nu trebuie amestecată cu niciun alt medicament.
Pregătirea injecției
- Spălați-vă bine mâinile.
- Tava pentru doze trebuie să conțină materialele enumerate mai jos (dacă nu, nu utilizați tava și consultați farmacistul). Folosiți numai materialele enumerate. NU utilizați alte seringi Flacon cu Enbrel Seringă preumplută care conține solvent limpede, incolor (apă pentru preparate injectabile) Piston pentru seringă 2 tampoane cu alcool Ghid de preparare a dozei (partea inferioară a tăvii).
- Verificați datele de expirare atât pe eticheta flaconului, cât și pe seringă. Nu trebuie utilizate după luna și anul indicat. c.
Pregătiți doza de Enbrel pentru injecție folosind „Ghidul de pregătire a dozelor” (pe spatele tăvii)
- Îndepărtați conținutul tăvii și întoarceți tava cu capul în jos. Partea inferioară a tăvii este un „ghid de preparare a dozelor.” Este special conceput pentru a menține flaconul și seringa în loc în timp ce soluția Enbrel este pregătită.
- Scoateți capacul din plastic din flaconul Enbrel. NU scoateți capacul gri sau inelul de aluminiu din jurul gâtului flaconului.
- Folosiți un nou tampon cu alcool pentru a curăța dopul gri de pe flaconul Enbrel. După curățare, nu atingeți capacul gri cu mâinile.
- Împingeți flaconul Enbrel în spațiul din dreapta marcajului din ghidul de preparare a dozelor; capacul gri va indica spre centrul tăvii (vezi Figura 1).
- Scoateți capacul acului seringii trăgându-l ferm, având grijă să nu atingeți acul sau lăsați acul să atingă orice suprafață (vezi Figura 2) Aveți grijă să nu îndoiți sau răsuciți capacul pentru a evita deteriorarea acului.
- Întoarceți flaconul astfel încât fanta din dop să fie orientată în sus și vizibilă. Cu acul îndreptat spre flacon, aliniați semnul "0,5 ml" de pe seringă cu marginea ghidului de preparare a dozelor. Păstrați atât acul, cât și seringa orizontală, astfel încât acul să nu atingă tava. Glisați seringa în ghidul de preparare a dozelor până când acul a trecut prin centrul inelului de oprire gri al flaconului (vezi Figura 3). Dacă acul este aliniat în mod corespunzător, veți simți o ușoară rezistență și apoi un "pop" care indică faptul că acul a trecut prin centrul capacului. Uită-te la vârful acului prin fanta din dop (vezi Figura 4) .Dacă acul nu este aliniat corect, vei simți o rezistență constantă când trece prin dop, fără niciun „pop”. Introduceți acul fără a-l înclina; acest lucru ar putea determina acul să se îndoaie și / sau să împiedice introducerea corectă a solventului în flacon (vezi Figura 5).
- Glisați pistonul în seringă.
- Rotiți pistonul în sensul acelor de ceasornic până când se simte o ușoară rezistență (vezi Figura 6).
Adăugarea solventului
- Împingeți pistonul PENTRU ÎNCET, până când tot solventul a trecut în flacon. Acest lucru va ajuta la reducerea spumei (numeroase bule) (vezi Figura 7).
- Lăsați seringa în poziție. Pentru a dizolva pulberea, mișcați ușor ghidul de preparare a dozelor de câteva ori în mișcări circulare (a se vedea Figura 8). NU agitați ghidul de preparare a dozelor. Așteptați până când toată pulberea s-a dizolvat (de obicei mai puțin de 10 minute). Soluția trebuie să pară limpede și incoloră, fără fragmente, fulgi sau particule. O cantitate de spumă albă poate rămâne în flacon - acest lucru este normal. NU utilizați Enbrel dacă toată pulberea din flacon nu se dizolvă în decurs de 10 minute. Începeți cu o altă tavă pentru dozare.
Retragerea soluției Enbrel din flacon
- Cu acul încă în flacon, țineți ghidul de preparare a dozelor cu flaconul cu susul în jos la nivelul ochilor. Trageți încet pistonul înapoi pentru a trage lichid în seringă (vezi Figura 9). De îndată ce nivelul lichidului din flacon scade, este posibil ca acul să fie necesar să fie parțial retras pentru a menține vârful în lichid. Pentru pacienții adulți, retrageți întregul volum. Pentru copii, retrageți doar porția de lichid așa cum a fost prescris de medicul copilului.
- Cu acul încă în flacon, verificați dacă seringa nu prezintă bule de aer. Bateți ușor seringa astfel încât toate bulele de aer să se ridice în partea superioară a seringii, lângă ac (vezi Figura 10). Împingeți pistonul încet pentru a împinge bulele de aer din seringă în flacon. Dacă lichidul este returnat accidental în flacon în timpul acestui pas, trageți încet pistonul înapoi pentru a trage lichidul înapoi în seringă.
- Trageți seringa complet din ghidul de preparare a dozelor. Din nou, nu atingeți acul și nu-l lăsați să atingă nicio suprafață (a se vedea Figura 11). (Notă: După parcurgerea acestor pași, o cantitate mică de lichid poate rămâne în flacon. Acest lucru este normal).
Alegeți un loc de injectare
- Cele trei locuri de injectare recomandate pentru Enbrel includ: partea din față a coapselor, abdomenul, cu excepția zonei aflate la 5 cm distanță în jurul buricului; și zona exterioară a brațelor superioare (vezi Figura 12). Dacă vă faceți o injecție, nu trebuie să utilizați zona exterioară a brațelor superioare.
- Pentru fiecare nouă injecție trebuie utilizat un loc diferit. Fiecare injecție nouă trebuie administrată la cel puțin 3 cm de un loc anterior. Nu injectați în zonele în care pielea este fragedă, învinețită, roșie sau dură. Evitați zonele cu cicatrici sau vergeturi. (Poate fi util să rețineți locația locurilor de injectare anterioare).
- Dacă dumneavoastră sau copilul dumneavoastră aveți psoriazis, încercați să nu vă injectați direct în zone umflate, îngroșate, roșii sau solzoase ale pielii („leziuni ale pielii psoriazis”). g. Pregătiți locul de injectare și injectați soluția Enbrel.
- Ștergeți locul de injectare unde Enbrel urmează să fie injectat cu tampon cu alcool folosind o mișcare circulară. NU atingeți din nou această zonă înainte de injectare.
- Când zona curățată a pielii s-a uscat, strângeți-o și țineți-o ferm cu o mână. Cu cealaltă mână, țineți seringa ca un creion.
- Cu o mișcare rapidă și scurtă, pătrundeți complet acul în piele la un unghi de 45 ° până la 90 ° (a se vedea Figura 13). Cu experiență, veți găsi unghiul cel mai confortabil pentru dvs. sau pentru bebeluș. Aveți grijă să nu pentru a împinge acul în piele prea încet sau cu mare forță.
- Când acul a intrat complet în piele, eliberați pielea pe care o țineți. Cu mâna liberă, țineți seringa aproape de bază pentru a o stabiliza. Apoi împingeți pistonul pentru a injecta toată soluția într-un ritm lent și constant. (vezi Figura 14).
- Când seringa este goală, scoateți acul de pe piele, având grijă să-l mențineți în același unghi în care a fost când a fost introdusă.
- Apăsați un tampon de bumbac peste locul injectării timp de 10 secunde. Poate să apară sângerări ușoare. NU frecați locul injectării. Un bandaj este opțional.
Eliminarea materialului
- Seringa și acul NU trebuie refolosite NICIODATĂ Nu închideți niciodată acul. Eliminați acul și seringa conform recomandărilor medicului, asistentei sau farmacistului.
Dacă aveți întrebări, discutați cu un medic, asistent medical sau farmacist care este familiarizat cu Enbrel.
Supradozaj Ce trebuie făcut dacă ați luat prea mult Enbrel
Dacă utilizați mai mult Enbrel decât ar trebui:
Dacă ați utilizat mai mult decât trebuie din Enbrel (fie injectând prea mult cu o ocazie, fie folosindu-l prea frecvent), discutați imediat cu medicul dumneavoastră sau cu farmacistul. Luați întotdeauna cutia cu medicamente, chiar dacă este goală.
Dacă uitați să luați Enbrel:
Dacă uitați o doză, administrați-o imediat ce observați doza uitată, cu excepția cazului în care doza următoare este programată pentru a doua zi, caz în care trebuie să săriți doza uitată. Apoi continuați să administrați medicamentul în ziua (zilele) desemnată (e). Dacă ați uitat doza până în ziua următoarei dozei următoare, nu luați o doză dublă (două doze în aceeași zi) pentru a compensa doza uitată.
Dacă încetați să luați Enbrel:
Simptomele bolii pot reveni după oprirea tratamentului Dacă aveți întrebări suplimentare cu privire la utilizarea acestui medicament, adresați-vă medicului dumneavoastră sau farmacistului.
Efecte secundare Care sunt efectele secundare ale Enbrel
Ca toate medicamentele, Enbrel poate provoca reacții adverse, deși nu apar la toate persoanele.
Reactii alergice
Dacă apare oricare dintre următoarele reacții adverse, nu mai injectați Enbrel. Spuneți imediat medicului dumneavoastră sau mergeți la cea mai apropiată cameră de urgență a spitalului.
- Dificultăți la înghițire sau respirație
- Umflarea feței, gâtului, mâinilor sau picioarelor
- Senzație de nervozitate sau anxietate, palpitații, roșeață bruscă a pielii și / sau senzație de căldură
- Erupție cutanată severă, mâncărime, urticarie (pete ridicate de piele roșie sau deschisă care deseori prurit)
Reacțiile alergice severe sunt rare. Cu toate acestea, oricare dintre simptomele de mai sus poate indica o reacție alergică la Enbrel; prin urmare, trebuie să solicitați imediat asistență medicală.
Efecte secundare grave
Dacă observați oricare dintre următoarele, este posibil ca dumneavoastră sau copilul dumneavoastră să aveți nevoie de asistență medicală urgentă.
- Simptomele infecțiilor grave, cum ar fi febra mare, care poate fi însoțită de tuse, dificultăți de respirație, frisoane, slăbiciune sau o zonă fierbinte, roșie, fragedă, dureroasă în piele sau articulații.
- Simptome ale tulburărilor de sânge, cum ar fi sângerări, vânătăi sau paloare.
- Simptomele modificărilor nervoase, cum ar fi amorțeală sau furnicături, modificări ale vederii, dureri la nivelul ochilor sau apariția slăbiciunii la un braț sau la un picior.
- Simptome de agravare a insuficienței cardiace, cum ar fi oboseala sau dificultăți de respirație în timpul activității, umflarea gleznelor, senzație de umflare la nivelul gâtului sau abdomenului, respirație dificilă noaptea sau tuse, culoare albăstruie a unghiilor sau a buzelor.
- Simptomele tumorilor: tumorile pot afecta orice parte a corpului, inclusiv pielea și sângele, iar posibilele simptome depind de tipul și localizarea tumorii. Aceste simptome pot include pierderea în greutate, febră, umflături (cu sau fără durere), tuse persistentă, prezența chisturilor sau creșteri pe piele.
- Simptome ale reacțiilor autoimune (în care se creează anticorpi care pot deteriora țesuturile normale ale corpului), cum ar fi durerea, mâncărimea, slăbiciunea, anomaliile în respirație, gândire, senzație sau vedere.
- Simptomele lupusului sau sindromului asemănător lupusului, cum ar fi modificări ale greutății corporale, erupții persistente, febră, dureri articulare sau musculare sau oboseală.
- Simptome de inflamație a vaselor de sânge, cum ar fi durere, febră, roșeață sau căldură a pielii sau mâncărime.
Aceste reacții adverse sunt rare sau mai puțin frecvente, dar sunt afecțiuni grave (dintre care unele pot provoca rar moartea). Dacă apar aceste simptome, spuneți imediat medicului dumneavoastră sau mergeți la cea mai apropiată cameră de urgență a spitalului.
Efectele secundare cunoscute ale Enbrel includ următoarele, grupate în funcție de frecvența descrescătoare:
- Foarte frecvente (pot afecta mai mult de 1 din 10 pacienți): infecții (inclusiv răceli, sinuzită, bronșită, infecții ale tractului urinar și infecții ale pielii); reacții la locul injectării (inclusiv sângerări, vânătăi, roșeață, mâncărime, durere și umflături).
- Frecvente (pot afecta până la 1 din 10 pacienți): reacții alergice; febră; mâncărime; anticorpi direcționați împotriva țesutului normal (formarea de autoanticorpi)
- Mai puțin frecvente (pot afecta până la 1 din 100 de persoane): infecții grave (inclusiv pneumonie, infecții profunde ale pielii, infecții articulare, infecții cu sânge și infecții la diferite locuri); număr redus de trombocite în sânge; cancer de piele (cu excepția melanomului); umflarea localizată a pielii (angioedem); urticarie (pete ridicate de piele roșie sau deschisă care deseori prurit); inflamația ochilor; psoriazis (prima apariție sau agravare), erupție cutanată; inflamație sau cicatrizare a plămânilor; inflamația vaselor de sânge care afectează mai multe organe.
- Rare (pot afecta până la 1 din 1000 de persoane): reacții alergice severe (inclusiv umflături severe localizate ale pielii și dificultăți de respirație); limfom (un tip de cancer de sânge); melanom (un tip de cancer de piele); reducerea articulațiilor în numărul de trombocite, celule roșii din sânge și celule albe din sânge; modificări ale sistemului nervos (cu slăbiciune musculară severă și semne și simptome similare cu cele ale sclerozei multiple sau inflamației nervilor din ochi sau măduva spinării); tuberculoză; agravarea insuficienței cardiace; convulsii; lupus sau sindrom asemănător lupusului (simptomele pot include „erupție persistentă, febră, dureri articulare și oboseală); număr scăzut de celule roșii din sânge, număr scăzut de celule albe din sânge, număr scăzut de neutrofile (un tip de celule albe din sânge); ficat crescut din sânge; erupție cutanată care poate duce la formarea de vezicule și descuamare severă a pielii; inflamație a ficatului cauzată de sistemul imunitar (hepatită autoimună); tulburări imune care pot afecta plămânii, pielea și ganglionii limfatici (sarcoidoză).
- Foarte rare (pot afecta până la 1 din 10.000 de persoane): incapacitatea măduvei osoase de a produce celule sanguine esențiale.
- Cu frecvență necunoscută (frecvența nu poate fi estimată din datele disponibile): leucemie (un cancer care afectează sângele și măduva osoasă); Carcinom cu celule Merkel (un tip de cancer de piele); activarea excesivă a celulelor albe din sânge asociate cu inflamația (sindromul de activare a macrofagelor); revenirea hepatitei B (o infecție hepatică);
Efecte secundare la copii și adolescenți
Efectele secundare și frecvența lor observate la copii și adolescenți sunt similare cu cele descrise mai sus.
Raportarea efectelor secundare
Dacă manifestați orice reacții adverse, adresați-vă medicului dumneavoastră sau farmacistului, inclusiv orice reacții adverse posibile care nu sunt enumerate în acest prospect. De asemenea, puteți raporta reacțiile adverse direct prin intermediul sistemului național de raportare enumerat în Anexa V. Raportând reacțiile adverse puteți contribui la furnizarea mai multor informații cu privire la siguranța acestui medicament.
Expirare și reținere
Nu lăsați acest medicament la vederea și îndemâna copiilor.
Nu utilizați Enbrel după data de expirare înscrisă pe cutie și etichetă după „EXP”. Data de expirare se referă la ultima zi a lunii respective.
A se păstra la frigider (între 2 ° C și 8 ° C). Nu înghețați.
Înainte de a prepara soluția Enbrel, medicamentul poate fi păstrat din frigider la o temperatură maximă de 25 ° C timp de până la 4 săptămâni, pentru o singură dată; după această perioadă nu mai poate fi pus la loc în frigider. Dacă nu este utilizat în decurs de 4 săptămâni în afara frigiderului, Enbrel trebuie aruncat. Se recomandă să rețineți data la care Enbrel este plasat din frigider și data până la care trebuie eliminat Enbrel (nu mai mult de 4 săptămâni din frigider).
Se recomandă utilizarea imediată după prepararea soluției Enbrel, însă soluția poate fi utilizată în decurs de 6 ore dacă este depozitată la o temperatură maximă de 25 ° C.
Nu utilizați Enbrel dacă observați că soluția nu este limpede sau dacă conține particule. Soluția trebuie să pară limpede și incoloră sau de culoare galben pal, fără bulgări, flocuri sau particule.
Aruncați temeinic orice soluție Enbrel care nu a fost injectată în decurs de 6 ore.
Nu aruncați niciun medicament pe calea apei uzate sau a deșeurilor menajere. Întrebați farmacistul cum să aruncați medicamentele pe care nu le mai utilizați. Acest lucru va ajuta la protejarea mediului.
Compoziție și formă farmaceutică
Ce conține Enbrel
Substanța activă a Enbrel este etanercept. Fiecare flacon de Enbrel 25 mg conține etanercept 25 mg.
Ceilalți excipienți sunt:
Pulbere: manitol (E421), zaharoză și trometamol
Solvent: apă pentru preparate injectabile
Cum arată Enbrel și conținutul ambalajului
Enbrel 25 mg este furnizat sub formă de pulbere albă și solvent pentru soluție injectabilă. Fiecare ambalaj conține 4 flacoane cu doză unică, 4 seringi preumplute cu apă pentru preparate injectabile și 8 tampoane cu alcool.
Este posibil ca nu toate mărimile de ambalaj să fie comercializate.
Prospect sursă: AIFA (Agenția italiană pentru medicamente). Conținut publicat în ianuarie 2016. Este posibil ca informațiile prezente să nu fie actualizate.
Pentru a avea acces la cea mai actualizată versiune, este recomandabil să accesați site-ul web AIFA (Agenția italiană pentru medicamente). Declinare de responsabilitate și informații utile.
01.0 DENUMIREA PRODUSULUI MEDICAMENTAL
ENBREL 25 MG / ML
02.0 COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ
Fiecare flacon conține 25 mg etanercept. După reconstituire, soluția conține 25 mg / ml etanercept.
Etanercept este o proteină de fuziune a receptorului p75 al factorului de necroză tumorală umană cu Fc, obținută prin tehnici de ADN recombinant printr-un sistem de expresie a mamiferelor în celulele ovarului de hamster chinezesc (CHO). Etanercept este un dimer al unei proteine himerice. Preparat genetic prin fuziunea domeniul extracelular al factorului de necroză tumorală umană receptor-2 (TNFR2 / p75) responsabil de legarea cu ligandul, cu fracția Fc a imunoglobulinei IgG1 umane. Această fracțiune Fc conține regiunea balama, regiunile CH2 și CH3, dar nu regiunea CH1 a IgG1. Etanercept conține 934 aminoacizi și are o greutate moleculară aparentă de aproximativ 150 kilodalton.
Activitatea specifică a etanerceptului este de 1,7 x 106 unități / mg.
Soluția conține 9 mg / ml alcool benzilic ca conservant (vezi pct. 4.4). Pentru lista completă a excipienților, vezi secțiunea 6.1.
03.0 FORMA FARMACEUTICĂ
Pulbere și solvent pentru soluție injectabilă (pulbere pentru injecție).
Pulberea este albă. Solventul este un lichid limpede, incolor.
04.0 INFORMAȚII CLINICE
04.1 Indicații terapeutice
Artrita idiopatică juvenilă
Tratamentul poliartritei (factor reumatoid pozitiv sau negativ) și a oligoartritei extinse la copii și adolescenți de la 2 ani care au prezentat un răspuns inadecvat sau care s-au dovedit a fi intoleranți la metotrexat.
Tratamentul artritei psoriazice la adolescenți de la vârsta de 12 ani care au prezentat un răspuns inadecvat sau care s-au dovedit a fi intoleranți la metotrexat.
Tratamentul artritei legate de entezită la adolescenți cu vârsta de 12 ani care au prezentat un răspuns inadecvat sau care s-au dovedit a fi intoleranți la terapia convențională.
Enbrel nu a fost studiat la copii cu vârsta sub 2 ani.
Psoriazisul plăcii pediatrice
Tratamentul psoriazisului cronic sever în plăci la copii și adolescenți de la 6 ani care nu sunt controlați în mod adecvat de alte terapii sistemice sau fototerapii sau care sunt intoleranți la acestea.
04.2 Doze și mod de administrare
Tratamentul cu Enbrel trebuie inițiat și supravegheat de un medic specialist cu experiență în diagnosticul și tratamentul artritei idiopatice juvenile sau al psoriazisului pe plăci pediatric.
Pacienții tratați cu Enbrel trebuie să primească cardul de alertă pentru pacienți.
Fiecare flacon de Enbrel 25 mg / ml trebuie utilizat pentru maximum 2 doze administrate aceluiași pacient.
Dozare
Populații speciale
Insuficiență renală și hepatică
Nu este necesară ajustarea dozelor.
Populația pediatrică
Artrita idiopatică juvenilă
Doza recomandată este de 0,4 mg / kg (până la maximum 25 mg per doză), administrată de două ori pe săptămână prin injecție subcutanată cu un interval de 3-4 zile între doze sau 0,8 mg / kg (până la maximum 50 mg pe administrată o dată pe săptămână. La pacienții care nu prezintă niciun răspuns după 4 luni de tratament, trebuie luată în considerare întreruperea tratamentului.
Copiii cu artrită idiopatică juvenilă cu o greutate mai mică de 25 kg pot fi mai adecvați pentru a administra flaconul cu tăria de 10 mg.
Nu s-au efectuat studii clinice la copii cu vârsta cuprinsă între 2 și 3 ani. Cu toate acestea, datele limitate de siguranță dintr-un registru de pacienți indică faptul că profilul de siguranță la copiii cu vârsta de 2-3 ani este similar cu cel observat la adulți și copii cu vârsta de 4 ani și peste când produsul este administrat săptămânal. Cu o doză de 0,8 mg / kg subcutanat (vezi pct. 5.1).
Enbrel nu este, în general, adecvat pentru copiii cu vârsta sub 2 ani pentru indicația de artrită idiopatică juvenilă.
Psoriazisul plăcii pediatrice (de la vârsta de 6 ani)
Doza recomandată este de 0,8 mg / kg (până la maximum 50 mg pe doză) o dată pe săptămână timp de până la 24 de săptămâni. Tratamentul trebuie întrerupt la pacienții care nu prezintă niciun răspuns după 12 săptămâni.
În cazul în care tratamentul cu Enbrel este indicat din nou, trebuie respectate instrucțiunile de mai sus privind durata tratamentului. Doza trebuie să fie de 0,8 mg / kg (până la maximum 50 mg pe doză) o dată pe săptămână.
Enbrel nu este, în general, potrivit pentru copii sub 6 ani pentru indicația psoriazisului în plăci.
Mod de administrare
Enbrel se administrează prin injecție subcutanată (vezi pct. 6.6).
Instrucțiuni detaliate pentru prepararea, administrarea și reutilizarea flaconului reconstituit cu Enbrel sunt furnizate în prospect, secțiunea 7, „Instrucțiuni pentru pregătirea și administrarea unei„ injecții cu Enbrel ”.
04.3 Contraindicații
Hipersensibilitate la substanța activă sau la oricare dintre excipienții enumerați la pct. 6.1.
Sepsis sau risc de sepsis.
Tratamentul cu Enbrel nu trebuie inițiat la pacienții cu infecție activă, inclusiv infecții cronice sau localizate.
Enbrel nu trebuie administrat copiilor prematuri sau nou-născuților, deoarece solventul conține alcool benzilic.
04.4 Avertismente speciale și precauții adecvate pentru utilizare
Infecții
Pacienții trebuie testați pentru infecții înainte, în timpul și după tratamentul cu Enbrel, considerând că timpul de înjumătățire mediu al etanerceptului este de aproximativ 70 de ore (interval de 7 până la 300 de ore).
La utilizarea Enbrel au fost raportate infecții grave, sepsis, tuberculoză și alte infecții oportuniste, inclusiv infecții fungice invazive, listerioză și legioneloză (vezi pct. 4.8).
Aceste infecții au fost cauzate de bacterii, micobacterii, ciuperci, viruși și paraziți (inclusiv protozoare). În unele cazuri, anumite ciuperci sau alte infecții oportuniste nu au fost recunoscute, determinând întârzierea tratamentului adecvat și, în unele cazuri, moartea. La examinarea pacienților pentru infecții, trebuie luat în considerare riscul pacientului de infecții oportuniste relevante (de exemplu, expunerea la micoza endemică).
Pacienții care dezvoltă o nouă infecție în timpul tratamentului cu Enbrel trebuie monitorizați îndeaproape.Dacă pacientul dezvoltă o infecție severă, administrarea Enbrel trebuie întreruptă. Siguranța și eficacitatea Enbrel la pacienții cu infecții cronice nu au fost evaluate. Medicii trebuie să fie precauți atunci când evaluează utilizarea Enbrel la pacienții cu antecedente de infecții recurente sau cronice sau cu afecțiuni de bază care pot predispune pacienții la infecție, precum și cu diabet avansat sau slab controlat.
Tuberculoză
Au fost raportate cazuri de tuberculoză activă, inclusiv tuberculoză miliară și tuberculoză cu localizare extra-pulmonară, la pacienții tratați cu Enbrel.
Înainte de a începe tratamentul cu Enbrel, toți pacienții trebuie testați pentru tuberculoză activă și inactivă („latentă”). Această evaluare ar trebui să includă un istoric medical detaliat, inclusiv antecedente personale de tuberculoză sau posibile contacte anterioare cu tuberculoză și terapie imunosupresoare anterioară și / sau actuală. La toți pacienții trebuie efectuate teste adecvate de screening, de exemplu testul cutanat al tuberculinei și radiografia toracică (se pot aplica recomandări locale). Se recomandă înregistrarea acestor teste pe cardul de alertă al pacientului. Doctorilor li se amintește de riscul unui test cutanat fals negativ asupra tuberculinei, în special la pacienții grav bolnavi sau imunocompromiși.
Dacă este diagnosticată tuberculoza activă, terapia cu Enbrel nu trebuie inițiată. Dacă este diagnosticată tuberculoza inactivă („latentă”), tratamentul pentru tuberculoza latentă trebuie început cu terapie antituberculoză înainte de a începe terapia Enbrel și conform reglementărilor locale.
În această situație, raportul risc / beneficiu cu tratamentul cu Enbrel trebuie luat în considerare cu atenție.
Toți pacienții trebuie sfătuiți să solicite asistență medicală dacă apar semne / simptome sugestive de tuberculoză (de exemplu, tuse persistentă, irosire / scădere în greutate, febră de grad scăzut) în timpul sau după tratamentul cu Enbrel.
Reactivarea virusului hepatitei B.
Reactivarea virusului hepatitei B (VHB) a fost raportată la purtătorii cronici ai acestui virus care primesc anti-TNF, cum ar fi Enbrel. Pacienții cu risc de infecție cu VHB trebuie supuși testelor preliminare pentru infecția cu VHB înainte de a începe tratamentul cu Enbrel.
Ar trebui să se acorde o atenție deosebită la administrarea Enbrel la pacienții cu VHB. Dacă Enbrel este utilizat la purtătorii de VHB, pacienții trebuie monitorizați pentru semne și simptome de infecție activă cu VHB și, dacă este necesar, trebuie inițiat un tratament adecvat.
Agravarea hepatitei C
S-a raportat agravarea hepatitei C la pacienții tratați cu Enbrel. Enbrel trebuie utilizat cu precauție la pacienții cu antecedente de hepatită C.
Tratament simultan cu anakinra
Administrarea concomitentă de Enbrel și anakinra a fost asociată cu un risc crescut de infecții grave și neutropenie, comparativ cu utilizarea Enbrel în monoterapie. Această combinație nu a demonstrat o creștere a beneficiului clinic. Prin urmare, utilizarea combinată a Enbrel și anakinra nu. recomandat (vezi pct. 4.5 și 4.8).
Tratament simultan cu abatacept
În studiile clinice, tratamentul concomitent cu abatacept și Enbrel a dus la o incidență crescută a evenimentelor adverse grave. Această combinație nu a demonstrat o creștere a beneficiului clinic; prin urmare, utilizarea nu este recomandată (vezi pct. 4.5).
Reactii alergice
Au fost raportate frecvent reacții alergice asociate cu administrarea Enbrel.
Reacțiile alergice au inclus angioedem și urticarie; au existat reacții severe. Dacă apare orice reacție alergică sau anafilactică severă, terapia cu Enbrel trebuie oprită imediat și trebuie inițiată terapia adecvată.
Imunosupresia
Există posibilitatea ca antagoniștii TNF, inclusiv Enbrel, să afecteze apărarea gazdei împotriva infecțiilor și malignităților, deoarece TNF mediază inflamația și modulează răspunsurile imune celulare. Într-un studiu efectuat pe 49 de pacienți adulți cu poliartrită reumatoidă tratați cu Enbrel, nu au existat dovezi de depresie a hipersensibilității de tip întârziat, scăderea nivelului de imunoglobulină sau modificări ale numărului de populații de celule efectoare.
Doi pacienți cu artrită idiopatică juvenilă au dezvoltat infecție cu varicelă și semne și simptome ale meningitei aseptice, care s-au rezolvat fără sechele. Pacienții cu expunere semnificativă la virusul varicelei trebuie să întrerupă temporar terapia cu Enbrel și trebuie luat în considerare tratamentul profilactic cu imunoglobulină varicelo-zosteriană.
Siguranța și eficacitatea Enbrel la pacienții cu imunosupresie nu au fost evaluate.
Tulburări limfoproliferative și tumori maligne
Tumori maligne solide și hematopoietice (cu excepția cancerelor de piele)
Dezvoltarea tumorilor maligne (inclusiv cancer de sân și plămâni și limfom) a fost raportată în perioada de după punerea pe piață (vezi pct. 4.8).
În studiile clinice cu medicamente anti-TNF cu grup de control, au fost observate mai multe cazuri de limfom la pacienții care au primit un medicament anti-TNF decât în grupul de control. Cu toate acestea, cazurile au fost rare și perioada de observație pentru pacienții tratați cu placebo a fost mai scurtă decât pentru pacienții tratați cu TNF. De la introducere pe piață, au fost raportate cazuri de leucemie la pacienții tratați cu medicamente anti-TNF. Există un risc subiacent crescut de limfom și leucemie la pacienții cu artrită reumatoidă cu boală inflamatorie de lungă durată și sever activă, ceea ce complică estimarea riscului.
Pe baza cunoștințelor actuale, dezvoltarea limfoamelor, leucemiilor sau a altor tumori solide sau hematopoietice la pacienții tratați cu medicamente anti-TNF nu poate fi exclusă. La pacienții cu antecedente de malignitate sau la continuarea terapiei la pacienții care dezvoltă malignitate, trebuie utilizată precauție atunci când se ia în considerare tratamentul anti-TNF.
Au fost raportate tumori maligne, uneori letale, la copii, adolescenți și adulți tineri (până la 22 de ani) tratați cu medicamente anti-TNF (inițierea tratamentului
Tumori cutanate
Au fost raportate melanoame și cancere cutanate non-melanom (NMSC) la pacienții tratați cu antagoniști ai TNF, inclusiv Enbrel. Cazurile de carcinom cu celule Merkel la pacienții tratați cu Enbrel au fost raportate foarte rar în experiența de după punerea pe piață. Se recomandă examinări cutanate periodice pentru toți pacienții, în special cei cu factori de risc pentru apariția cancerelor de piele.
Combinând rezultatele studiilor clinice controlate, s-au observat mai multe cazuri de NMSC la pacienții tratați cu Enbrel decât la pacienții de control, în special la pacienții cu psoriazis.
Vaccinări
Vaccinurile vii nu trebuie administrate concomitent cu Enbrel. Nu sunt disponibile date privind transmiterea secundară a infecției din vaccinurile vii la pacienții cărora li s-a administrat Enbrel. Într-un studiu clinic randomizat, dublu-orb, controlat cu placebo, la pacienți adulți cu artrită psoriazică, 184 de pacienți au primit, de asemenea, un vaccin pneumococic polivalent multivalent în săptămâna 4. În acest studiu, majoritatea pacienților cu artrită psoriazică care au primit Enbrel au fost capabili să producă un tratament eficient Răspunsul imun al celulelor B la vaccinul polizaharidic pneumococic, dar titrul din bazin a fost moderat mai mic și puțini pacienți au prezentat o creștere dublă a titrului în comparație cu pacienții care nu au primit Enbrel. Semnificația clinică a acestuia este necunoscută.
Formarea autoanticorpilor
Tratamentul cu Enbrel poate determina formarea de anticorpi autoimuni (vezi pct. 4.8).
Reacții hematologice
La pacienții tratați cu Enbrel au fost raportate cazuri rare de pancitopenie și cazuri foarte rare de anemie aplastică, unele cu rezultate fatale. Se recomandă prudență la pacienții tratați cu Enbrel care au „antecedente de discrazie sanguină. Toți pacienții și părinții / profesioniștii din domeniul sănătății trebuie sfătuiți că, dacă pacientul dezvoltă semne și simptome sugestive de discrazie sanguină sau infecții (de exemplu, febră persistentă, dureri în gât) , învinețire, sângerare, paloare) în timpul tratamentului cu Enbrel, trebuie să solicite asistență medicală imediată. Acești pacienți ar trebui să fie consultați imediat, inclusiv o hemoleucogramă completă; dacă discraziile sanguine sunt confirmate, tratamentul cu Enbrel trebuie oprit.
Patologii neurologice
Există cazuri rare de boli demielinizante ale SNC la pacienții tratați cu Enbrel (vezi pct. 4.8). În plus, au existat rapoarte foarte rare de polineuropatii demielinizante periferice (inclusiv sindromul Guillain-Barré, polineuropatia inflamatorie cronică demielinizantă, polineuropatia demielinizantă și neuropatia motorie multifocală).
Deși nu au fost efectuate studii clinice pentru evaluarea terapiei cu Enbrel la pacienții cu scleroză multiplă, studiile clinice la pacienții cu scleroză multiplă tratați cu alți antagoniști ai TNF au arătat o activitate crescută a bolii.
Se recomandă o evaluare atentă a riscului / beneficiului, inclusiv evaluarea neurologică, atunci când se prescrie Enbrel pacienților cu boală demielinizantă cu debut preexistent sau recent sau pentru acei pacienți care sunt considerați a fi cu risc crescut de a dezvolta boala demielinizantă.
Terapie combinată
Într-un studiu clinic controlat de doi ani la pacienți adulți cu poliartrită reumatoidă, combinația de Enbrel și metotrexat nu a dat rezultate neașteptate de siguranță, iar profilul de siguranță al Enbrel, administrat în asociere cu metotrexat, a fost similar cu cel al profilului în studiile cu Enbrel și metotrexat administrat singur. Studiile pe termen lung care vizează terapia combinată sunt în curs de desfășurare.
Siguranța pe termen lung a Enbrel în combinație cu alte medicamente antireumatice care modifică boala (DMARD) nu a fost evaluată.
În tratamentul psoriazisului, utilizarea Enbrel în combinație cu alte terapii sistemice sau fototerapie nu a fost studiată.
Insuficiență renală și hepatică
Pe baza datelor farmacocinetice (vezi pct. 5.2) nu este necesară modificarea dozei la pacienții cu insuficiență renală sau hepatică; datele clinice privind acești pacienți sunt limitate.
Insuficiență cardiacă congestivă
Medicii trebuie să fie precauți atunci când utilizează Enbrel la pacienții cu insuficiență cardiacă congestivă (Insuficiență cardiacă congestivă, CHF). Există rapoarte după punerea pe piață a agravării CHF, cu și fără factori de precipitare identificabili, la pacienții tratați cu Enbrel. Două studii clinice de mari dimensiuni care au evaluat utilizarea Enbrel în tratamentul CHF au fost întrerupte precoce din cauza lipsei de eficacitate. .
Hepatita alcoolică
Într-un studiu randomizat, controlat cu placebo, de fază II, care a implicat 48 de pacienți spitalizați tratați cu Enbrel sau placebo pentru hepatită alcoolică moderată până la severă, Enbrel nu a fost eficient și, după 6 luni, rata mortalității pacienților tratați cu Enbrel a fost semnificativ mai mare.
În consecință, Enbrel nu trebuie utilizat la pacienții pentru tratamentul hepatitei alcoolice. Medicii trebuie să fie precauți atunci când utilizează Enbrel la pacienții cu hepatită alcoolică moderată până la severă.
Granulomatoza lui Wegener
Într-un studiu controlat cu placebo, în care 89 de pacienți adulți au fost tratați cu Enbrel pe lângă terapia standard (care a inclus ciclofosfamidă sau metotrexat și glucocorticoizi) pentru o durată medie de 25 de luni, nu s-a constatat că Enbrel este un tratament eficient pentru granulomatoză. de Wegener. Incidența malignităților non-cutanate de diferite tipuri a fost semnificativ mai mare la pacienții tratați cu Enbrel decât în grupul martor. Enbrel nu este recomandat pentru tratamentul granulomatozei Wegener.
Hipoglicemie la pacienții tratați pentru diabet
După inițierea tratamentului cu Enbrel la pacienții cărora li se administrează medicamente pentru diabet, au fost raportate hipoglicemii care necesită reducerea medicamentului anti-diabet la unii dintre acești pacienți.
Populații speciale
Pacienți vârstnici (≥ 65 ani)
În studiile de fază 3 privind artrita reumatoidă, artrita psoriazică și spondilita anchilozantă, în general nu au existat diferențe în apariția evenimentelor adverse, a evenimentelor adverse grave și a infecțiilor grave între pacienții cu vârsta de 65 de ani și pacienții mai în vârstă și cei mai tineri. Cu toate acestea, pacienții vârstnici trebuie tratați cu prudență și trebuie acordată o atenție deosebită apariției infecțiilor.
Populația pediatrică
Vaccinări
Se recomandă ca pacienții copii și adolescenți, înainte de inițierea terapiei cu Enbrel, să fi finalizat, dacă este posibil, toate imunizările în conformitate cu ghidurile actuale de imunizare (vezi Vaccinările de mai sus).
Boala inflamatorie a intestinului (Boala inflamatorie a intestinului, IBD) și uveită la pacienții cu artrită idiopatică juvenilă (Artrita idiopatică juvenilă, JIA)
Au fost raportate cazuri de IBD și uveită la pacienții cu AIJ tratați cu Enbrel (vezi pct. 4.8).
Alcool benzilic
Enbrel conține excipientul alcool benzilic, care poate provoca reacții toxice și anafilactoide la sugari și copii cu vârsta de până la 3 ani și nu trebuie administrat copiilor prematuri sau nou-născuților.
04.5 Interacțiuni cu alte medicamente și alte forme de interacțiune
Tratament simultan cu anakinra
O incidență mai mare a infecțiilor grave a fost observată la pacienții adulți tratați cu Enbrel și anakinra decât la pacienții tratați separat cu Enbrel sau anakinra (date istorice).În plus, într-un studiu clinic dublu-orb controlat cu placebo la pacienți adulți care au primit deja metotrexat, pacienții tratați cu Enbrel și anakinra au avut o incidență mai mare de infecții grave (7%) și neutropenie decât pacienții tratați cu Enbrel (vezi pct. 4.4 și 4.8 ). Combinația dintre Enbrel și anakinra nu a demonstrat un beneficiu clinic crescut și, prin urmare, nu este recomandată.
Tratament simultan cu abatacept
În studiile clinice, tratamentul concomitent cu abatacept și Enbrel a dus la o incidență crescută a evenimentelor adverse grave. Această combinație nu a demonstrat o creștere a beneficiului clinic; prin urmare, utilizarea nu este recomandată (vezi pct. 4.4).
Tratament simultan cu sulfasalazină
Într-un studiu clinic pe pacienți adulți cărora li s-au administrat doze stabilite de sulfasalazină, la care s-a adăugat Enbrel, pacienții din grupul combinat au arătat o scădere semnificativă statistic a numărului mediu de celule albe din sânge comparativ cu grupurile tratate numai cu Enbrel sau numai cu sulfasalazină. din această interacțiune este necunoscută Medicii trebuie să fie precauți atunci când iau în considerare terapia combinată cu sulfasalazină.
Nu interacțiuni
În timpul studiilor clinice, nu s-au observat interacțiuni atunci când Enbrel a fost administrat cu glucocorticoizi, salicilați (cu excepția sulfasalazinei), antiinflamatoare nesteroidiene (AINS), analgezice sau metotrexat. Vezi pct. 4.4 pentru avertismentele privind vaccinarea.
Nu s-au observat interacțiuni farmacocinetice semnificative medicamente în studiile cu metotrexat, digoxină sau warfarină.
04.6 Sarcina și alăptarea
Femeile aflate la vârsta fertilă
Femeile aflate la vârsta fertilă trebuie informate cu privire la necesitatea de a utiliza măsuri contraceptive adecvate pentru a evita să rămână gravide în timpul și până la trei săptămâni după întreruperea tratamentului cu Enbrel.
Sarcina
Studiile de toxicitate asupra dezvoltării la șobolani și iepuri nu au evidențiat nicio dovadă de vătămare datorată etanerceptului pentru făt sau șobolan nou-născut. Nu există studii cu Enbrel la femeile gravide.
Prin urmare, Enbrel nu este recomandat în timpul sarcinii.
Timp de hrănire
După administrarea subcutanată, a fost raportată excreția etanerceptului în laptele uman. La șobolanii care alăptează, după administrarea subcutanată, etanerceptul a fost excretat în lapte și recuperat în serul puilor.
Deoarece imunoglobulinele, la fel ca multe alte medicamente, pot fi secretate în laptele matern, trebuie luată o decizie dacă întreruperea alăptării sau întreruperea tratamentului cu Enbrel ținând seama de beneficiul alăptării pentru copil și de beneficiul terapiei pentru femeia.
Fertilitate
Nu există date preclinice cu privire la toxicitatea peri- și postnatală a etanerceptului și asupra efectelor etanerceptului asupra fertilității și performanței reproductive generale.
04.7 Efecte asupra capacității de a conduce vehicule și de a folosi utilaje
Nu s-au efectuat studii privind capacitatea de a conduce vehicule și de a folosi utilaje.
04.8 Efecte nedorite
Rezumatul profilului de siguranță
Populația pediatrică
Efecte nedorite la copii și adolescenți cu artrită idiopatică juvenilă
În general, evenimentele adverse la pacienții pediatrici cu artrită idiopatică juvenilă au fost similare ca frecvență și tip cu cele observate la pacienții adulți (vezi mai jos Reacții adverse la adulți). Diferențele față de adulți și alte considerații speciale sunt discutate în paragrafele următoare.
Tipurile de infecții observate în timpul studiilor clinice la pacienții cu artrită idiopatică juvenilă cu vârste cuprinse între 2 și 18 ani au fost, în general, ușoare până la moderate și similare cu cele observate în mod obișnuit la o populație ambulatorie de copii. Evenimentele adverse grave raportate au inclus varicela cu semne și simptome de meningită aseptică care s-au rezolvat fără sechele (vezi și pct. 4.4), apendicită, gastroenterită, depresie / modificări ale personalității, ulcer cutanat, esofagită / gastrită, șoc septic streptococic de grup A, diabet de tip I mellitus, infecția țesuturilor moi și infecția chirurgicală a plăgii.
Într-un studiu efectuat pe copii cu artrită idiopatică juvenilă cu vârsta cuprinsă între 4 și 17 ani, 43 din 69 de copii (62%) au dezvoltat o infecție în timp ce primeau Enbrel pe parcursul celor 3 luni de studiu (partea 1 etichetă deschisă) și frecvența și gravitatea infecțiilor a fost similară la 58 de pacienți care au finalizat terapia în extensia deschisă de 12 luni. Tipul și proporția evenimentelor adverse la pacienții cu artrită idiopatică juvenilă au fost similare cu cele observate în studiile Enbrel la pacienții adulți cu poliartrită reumatoidă și au fost în mare parte ușoare. evenimentele adverse au fost raportate mai frecvent la cei 69 de pacienți cu artrită idiopatică juvenilă care au luat Enbrel timp de 3 luni, comparativ cu 349 de adulți cu poliartrită reumatoidă. pe pacient / an), dureri abdominale (19%, 0,74 evenimente pe pacient / an) nu) și vărsături (13%, 0,74 evenimente per pacient / an).
Patru cazuri de sindrom de activare a macrofagelor au fost raportate în studiile clinice cu artrită idiopatică juvenilă.
În experiența de după punerea pe piață, au existat cazuri de boală inflamatorie intestinală și uveită la pacienții cu AIJ tratați cu Enbrel, inclusiv un număr foarte limitat de cazuri cu rechalare pozitivă (vezi pct. 4.4).
Efecte nedorite la copii și adolescenți cu psoriazis în plăci
Într-un studiu de 48 de săptămâni care a implicat 211 copii cu vârsta cuprinsă între 4-17 ani cu psoriazis în plăci pediatrică, evenimentele adverse raportate au fost similare cu cele observate în studiile anterioare la adulți cu psoriazis în plăci.
Populația adultă
Efecte secundare la adulți
Cele mai frecvent raportate reacții adverse sunt reacțiile la locul injectării (cum ar fi durerea, umflarea, mâncărimea, roșeața și sângerarea la locul injectării), infecțiile (cum ar fi infecțiile tractului respirator superior, bronșita, infecțiile vezicii urinare și infecțiile pielii), reacțiile alergice, dezvoltarea de anticorpi, mâncărime și febră.
De asemenea, au fost raportate reacții adverse grave cu Enbrel. Antagoniștii TNF, cum ar fi Enbrel, afectează sistemul imunitar, iar utilizarea lor poate afecta apărarea organismului împotriva infecțiilor și cancerului. Au fost găsite infecții grave la mai puțin de 1 din 100 de pacienți tratați cu Enbrel. Rapoartele au inclus și cazuri de sepsis și infecții cu rezultate fatale sau care pun viața în pericol. Au fost raportate diferite afecțiuni maligne asociate cu utilizarea Enbrel, inclusiv cancere de sân, plămâni, piele și glande limfatice (limfom).
De asemenea, au fost raportate reacții hematologice, neurologice și autoimune severe. Aceste reacții includ cazurile rare de pancitopenie și cazurile foarte rare de anemie aplastică. Evenimente de demielinizare centrală și periferică au fost raportate rar și foarte rar la utilizarea Enbrel, respectiv. Au fost raportate lupus, afecțiuni legate de lupus și vasculită.
Lista reacțiilor adverse
Următoarea listă de reacții adverse se bazează pe experiența din studiile clinice la adulți și experiența după punerea pe piață.
În cadrul clasei de organe și sisteme, reacțiile adverse sunt enumerate în funcție de clasele de frecvență (numărul presupus de pacienți cu acea reacție), utilizând următoarele categorii: foarte frecvente (≥1 / 10); frecvente (≥1 / 100,
Infecții și infestări:
Foarte frecvente: infecții (inclusiv infecții ale tractului respirator superior, bronșită, cistită, infecții ale pielii) *
Mai puțin frecvente: infecții severe (inclusiv pneumonie, celulită, artrită septică, sepsis și infecții parazitare) *
Rare: tuberculoză, infecții oportuniste (inclusiv fungice invazive, protozoare, infecții atipice bacteriene și micobacteriene și Legionella).
Cu frecvență necunoscută: Listeria, reactivarea hepatitei B.
Neoplasme benigne, maligne și nespecificate (inclusiv chisturi și polipi):
Mai puțin frecvente: cancer de piele non-melanom * (vezi pct. 4.4)
Rare: limfom, melanom (vezi pct. 4.4)
Cu frecvență necunoscută: leucemie, carcinom cu celule Merkel (vezi pct. 4.4)
Tulburări ale sistemului sanguin și limfatic:
Mai puțin frecvente: trombocitopenie
Rare: anemie, leucopenie, neutropenie, pancitopenie *
Foarte rare: anemie aplastică *
Tulburări ale sistemului imunitar:
Frecvente: reacții alergice (vezi tulburări ale pielii și ale țesutului subcutanat), formarea de autoanticorpi *
Mai puțin frecvente: vasculită sistemică (inclusiv vasculită asociată cu anticorpi citoplasmatici antineutrofili)
Rare: Reacții alergice și anafilactice severe (inclusiv angioedem și bronhospasm), sarcoidoză
Cu frecvență necunoscută: sindrom de activare a macrofagelor †
Tulburări ale sistemului nervos:
Rare: convulsii,
Episoade de demielinizare SNC care indică scleroză multiplă sau situații localizate de demielinizare, cum ar fi nevrita optică și mielita transversă (vezi pct. 4.4)
Foarte rare: evenimente periferice de demielinizare, inclusiv sindromul Guillain-Barré, polineuropatie inflamatorie cronică demielinizantă, polineuropatie demielinizantă și neuropatie motorie multifocală (vezi pct. 4.4)
Tulburări oculare:
Mai puțin frecvente: uveită, sclerită
Patologii cardiace
Rare: agravarea insuficienței cardiace congestive (vezi pct. 4.4)
Tulburări respiratorii, toracice și mediastinale:
Mai puțin frecvente: tulburări pulmonare interstițiale (inclusiv pneumonie și fibroză pulmonară) *
Tulburări hepato-biliare:
Rare: enzime hepatice crescute, hepatită autoimună
Afecțiuni ale pielii și ale țesutului subcutanat:
Frecvente: mâncărime
Mai puțin frecvente: angioedem, urticarie, erupție cutanată, erupție psoriaziformă, psoriazis (inclusiv debut nou sau agravare și pustular, în principal palmele și tălpile)
Rare: vasculită cutanată (inclusiv vasculită leucocitoclastică), sindrom Steven-Johnson, eritem multiform
Foarte rare: necroliză epidermică toxică
Tulburări musculo-scheletice și ale țesutului conjunctiv:
Rare: lupus eritematos cutanat subacut, lupus eritematos discoid, sindrom asemănător lupului
Tulburări generale și condiții la locul administrării:
Foarte frecvente: reacții la locul injectării (inclusiv sângerări, vânătăi, eritem, mâncărime, durere, umflături) *
Frecvente: febră
* vezi „Descrierea reacțiilor adverse selectate” de mai jos.
† A se vedea subsecțiunea „Efecte nedorite la pacienții pediatrici cu artrită idiopatică juvenilă” de mai sus.
Descrierea reacțiilor adverse selectate
Tumori maligne și tulburări limfoproliferative
O sută douăzeci și nouă de malignități noi de diferite tipuri. Frecvența și incidența observate în aceste studii clinice au fost similare cu cele așteptate pentru populația studiată. Au fost raportate în total 2 tumori maligne în studiile clinice care au durat aproximativ 2 ani, implicând 240 de pacienți cu artrită psoriazică tratați cu Enbrel.
În studiile clinice efectuate de mai bine de doi ani la 351 pacienți cu spondilită anchilozantă, au fost raportate 6 tumori maligne la pacienții tratați cu Enbrel.
Într-un grup de 2.711 pacienți cu psoriazis în plăci tratați cu Enbrel în studii dublu-orb și deschise, cu o durată de până la 2,5 ani, au fost raportate 30 de tumori maligne și 43 de cancer de piele non-melanom.
Au fost raportate 18 limfoame la un grup de 7.416 pacienți tratați cu Enbrel în studiile clinice privind artrita reumatoidă, artrita psoriazică, spondilita anchilozantă și psoriazisul.
Rapoarte privind diferite afecțiuni maligne (inclusiv carcinom mamar și pulmonar și limfom) au fost, de asemenea, primite în perioada de după punerea pe piață (vezi pct. 4.4).
Reacții la locul injectării
În comparație cu placebo, pacienții cu boli reumatice tratați cu Enbrel au avut o incidență semnificativ mai mare a reacțiilor la locul injectării (36% față de 9%). dintre reacțiile la locul de injectare care au apărut la grupurile care au primit Enbrel nu au fost tratate, în timp ce majoritatea pacienților care au primit terapie au primit preparate topice, cum ar fi corticosteroizii. împreună cu apariția simultană a reacțiilor la locul de injectare de la locurile de injectare anterioare. De obicei, aceste reacții au fost tranzitorii și nu s-au repetat în timpul tratamentului.
În primele 12 săptămâni de tratament în studiile clinice controlate la pacienții cu psoriazis în plăci, aproximativ 13,6% dintre pacienții tratați cu Enbrel au dezvoltat reacții la locul injectării, comparativ cu 3,4% dintre pacienții tratați cu placebo.
Infecții severe
În studiile controlate cu placebo, nu s-a observat nicio creștere a incidenței infecțiilor grave (letale, care pun viața în pericol sau care necesită spitalizare sau antibiotice intravenoase).
Infecții grave au apărut la 6,3% dintre pacienții cu poliartrită reumatoidă tratați cu Enbrel timp de până la 48 de luni. Acestea includ abcesul (în diferite locuri), bacteremie, bronșită, bursită, celulită, colecistită, diaree, diverticulită, endocardită (suspectată), gastroenterită, hepatită B herpes zoster, ulcer la picioare, infecție a gurii, osteomielită, otite peritonită, pneumonie, pielonefrită, sepsis, artrită septică, sinuzită, infecții ale pielii, ulcer de piele, infecție a tractului urinar, vasculită și infecție a plăgii.În studiul clinic de doi ani controlat activ, în care pacienții au fost tratați cu Enbrel singur sau cu metotrexat singur sau cu Enbrel în asociere cu metotrexat, rata infecțiilor grave a fost similară între grupurile tratate. Cu toate acestea, nu se poate exclude faptul că asocierea Enbrel cu metotrexatul ar putea fi asociată cu o rată crescută de infecții.
Nu au existat diferențe în ceea ce privește incidența infecțiilor între pacienții tratați cu Enbrel și cei tratați cu placebo pentru psoriazisul în plăci în studiile clinice controlate cu placebo cu durata de până la 24 de săptămâni. Au fost raportate infecții grave, inclusiv celulită, gastroenterită, pneumonie. , gastrită, apendicită, fasciită streptococică, miozită, șoc septic, diverticulită și abcese la pacienții tratați cu Enbrel. În studiile artritei psoriazice dublu-orb și deschise, 1 pacient a raportat o infecție severă (pneumonie).
Au fost raportate infecții grave și fatale în timpul utilizării Enbrel; agenții patogeni găsiți includ bacterii, micobacterii (inclusiv tuberculoza), viruși și ciuperci. Unele au apărut în câteva săptămâni de la inițierea tratamentului cu Enbrel la pacienții care aveau afecțiuni care stau la baza predispozitorilor (de exemplu, diabet, insuficiență cardiacă congestivă, antecedente de infecții curente sau cronice) pe lângă artrita reumatoidă (vezi pct. 4.4). Tratamentul cu Enbrel poate crește mortalitatea la pacienții cu sepsis diagnosticat.
Au fost raportate infecții oportuniste în asociere cu Enbrel, inclusiv fungice invazive, parazitare (inclusiv protozoare) și bacteriene (inclusiv Listeria Și Legionella) și micobacterii atipice. Într-un set de date din studiile clinice, incidența generală a infecțiilor oportuniste a fost de 0,09% pentru 15 402 de subiecți care au primit Enbrel. Rata ajustată la expunere a fost de 0,06 evenimente la 100 de pacienți. -An. În experiența post-comercializare, aproximativ jumătate din toate cazurile de infecții oportuniste globale au fost infecții fungice invazive. Cele mai frecvent raportate infecții fungice invazive au fost de la
Pneumocistis Și Aspergillus. Infecțiile fungice invazive reprezintă mai mult de jumătate din evenimentele fatale la pacienții care au dezvoltat infecții oportuniste. Majoritatea cazurilor cu un rezultat fatal au fost la pacienții cu pneumonie Pneumocistis, infecții fungice sistemice nespecifice și aspergiloză (vezi pct. 4.4).
Autoanticorpi
Probele de ser de la pacienții adulți au fost testate pentru autoanticorpi în diferite momente de timp. Dintre pacienții cu poliartrită reumatoidă testați pentru anticorpi antinucleari (ANA), proporția pacienților care au dezvoltat o nouă pozitivitate față de ANA (≥1: 40) a fost mai mare la pacienții tratați cu Enbrel (11%) comparativ cu pacienții tratați cu placebo (5%) . Procentul pacienților care au dezvoltat un nou anticorp ADN-dublu helix pozitiv a fost chiar mai mare prin radioimunotest (15% dintre pacienții tratați cu Enbrel comparativ cu 4% dintre pacienții tratați cu placebo) și prin test Crithidia luciliae (3% dintre pacienții tratați cu Enbrel comparativ cu niciunul dintre pacienții tratați cu placebo). Procentul pacienților tratați cu Enbrel care au dezvoltat anticorpi anticardiolipină a crescut similar cu cel observat la pacienții tratați cu placebo. Nu se cunoaște impactul tratamentului pe termen lung cu Enbrel asupra dezvoltării bolilor autoimune.
Dezvoltarea altor autoanticorpi în asociere cu un sindrom asemănător lupusului sau reacții cutanate compatibile clinic și biopsic cu lupus sau lupus cutanat subacut a fost rar raportată la unii pacienți, inclusiv la cei cu factor reumatoid pozitiv.
Panitopenie și anemie aplastică
Au fost raportate după punerea pe piață a pancitopeniei și anemiei aplastice, dintre care unele au fost letale (vezi pct. 4.4).
Boli pulmonare interstițiale
Au fost raportate după punerea pe piață a bolilor pulmonare interstițiale (inclusiv pneumonie și fibroză pulmonară), dintre care unele au fost fatale.
Tratament simultan cu anakinra
În studiile în care pacienții adulți au fost tratați concomitent cu Enbrel plus anakinra, s-a observat o „incidență mai mare a infecțiilor grave decât cu Enbrel singur și 2% dintre pacienți (3/139) au dezvoltat neutropenie (număr absolut de neutrofile 3) Un pacient neutropenic a dezvoltat celulită care rezolvată după spitalizare (vezi pct. 4.4 și 4.5).
Populația pediatrică
Vezi mai sus, Rezumatul profilului de siguranță.
04.9 Supradozaj
Nu au fost observate doze limitate de toxicitate în studiile clinice la pacienții cu poliartrită reumatoidă. Cea mai mare doză evaluată a fost o doză de încărcare intravenoasă de 32 mg / m2, urmată de o doză subcutanată de 16 mg / m2 administrată de două ori pe săptămână. Un pacient cu poliartrită reumatoidă a administrat în mod greșit 62 mg de Enbrel subcutanat de două ori pe săptămână timp de 3 săptămâni, fără a prezenta efecte secundare. Antidotul pentru Enbrel este necunoscut.
05.0 PROPRIETĂȚI FARMACOLOGICE
05.1 Proprietăți farmacodinamice
Grupa farmacoterapeutică: imunosupresoare, inhibitori ai factorului de necroză tumorală α (TNF-α).
Codul ATC: L04AB01.
Factorul de necroză tumorală (TNF) este o citokină predominantă în procesul inflamator al artritei reumatoide. Niveluri ridicate de TNF au fost de asemenea găsite în sinoviile și plăcile psoriazice ale pacienților cu artrită psoriazică și în serul și țesutul sinovial al pacienților cu spondilită. În psoriazisul în plăci, infiltrarea celulelor inflamatorii, inclusiv a celulelor T, duce la creșterea nivelului de TNF în leziunile psoriazice față de nivelurile pielii neafectate. Etanercept este un inhibitor competitiv al legării TNF de receptorii săi de suprafață celulară și, prin urmare, inhibă activitatea biologică a TNF.
TNF și limfotoxina sunt citokine pro-inflamatorii care se leagă de doi receptori distincti ai suprafeței celulare: receptorii factorului de necroză tumorală (TNFR) de 55 kilodalton (p55) și 75 kilodalton (p75). Ambele TNFR există în mod natural în forme solubile și legate de membrană.
Se consideră că TNFR sub formă solubilă reglează activitatea biologică a TNF.
TNF și limfotoxina există predominant ca homotrimeri cu activitatea lor biologică dependentă de reticulare cu TNFR de suprafață celulară. Receptorii dimerici solubili, cum ar fi etanerceptul, au o afinitate de legare mai mare pentru TNF decât receptorii monomerici și sunt inhibitori competitivi semnificativ mai puternici ai legării TNF de receptorii săi celulari.
Mai mult, utilizarea unei regiuni Fc a imunoglobulinei ca element de fuziune în construcția unui receptor dimeric conferă un timp de înjumătățire plasmatică mai lung.
Mecanism de acțiune
Cea mai mare parte a bolii articulare în artrita reumatoidă și spondilita anchilozantă și boala pielii în psoriazisul în plăci este mediată de molecule pro-inflamatorii care sunt legate într-o rețea controlată de TNF. Răspunsuri celulare mediate de TNF, făcând TNF biologic inactiv.Etanercept poate modula, de asemenea, răspunsurile biologice controlate de molecule de cascadă suplimentare (de exemplu, citokine, adeziune molecule sau proteinază) care sunt induse sau reglate de TNF.
Eficacitate și siguranță clinică
Această secțiune prezintă date din trei studii privind artrita idiopatică juvenilă, un studiu la copii și adolescenți cu psoriazis în plăci, patru studii la adulți cu poliartrită reumatoidă și patru studii la adulți cu psoriazis în plăci.
Populația pediatrică
Artrita idiopatică juvenilă
Siguranța și eficacitatea Enbrel au fost evaluate într-un studiu în două părți care a implicat 69 de copii cu artrită idiopatică juvenilă cu curs poliarticular care au prezentat diferite tipuri de debut al artritei idiopatice juvenile (poliartrită, pauciartrită, debut sistemic). Au fost înrolați pacienți cu vârste cuprinse între 4 și 17 ani cu artrită idiopatică juvenilă poliarticulară moderată până la severă în faza activă, refractari sau intoleranți la metotrexat; pacienții au rămas pe o doză stabilă de un singur medicament antiinflamator nesteroidian și / sau prednison (articulații active, limitarea mișcării, evaluarea generală a medicului și pacientul / părinții, evaluarea funcțională și rata de sedimentare a eritrocitelor (VSH). boala a fost definită ca ≥ 30% se agravează în trei din cele șase criterii de bază JRA, ≥ 30% îmbunătățire în cel mult unul dintre cele șase criterii de bază JRA și un minim de două articulații active.
În partea 1 a studiului, 51 din 69 (74%) pacienți au prezentat un răspuns clinic și au intrat în partea 2. %) primind placebo (p = 0,007).
De la începutul părții 2, timpul mediu până la exacerbare a fost ≥ 116 zile pentru pacienții care au primit Enbrel și 28 de zile pentru pacienții cărora li s-a administrat placebo.2 din studiu, unii dintre cei care au rămas pe Enbrel au continuat să se îmbunătățească de la 3 la 7 luni, în timp ce cei care au primit placebo nu s-au îmbunătățit.
Într-un studiu de siguranță cu extensie deschisă, 58 de pacienți copii și adolescenți din studiul anterior (de la vârsta de 4 ani până la momentul înscrierii) au continuat să primească Enbrel timp de până la 10 ani. Rata evenimentelor adverse grave și a infecțiilor grave nu a crescut odată cu expunerea pe termen lung.
Siguranța pe termen lung a monoterapiei cu Enbrel (n = 103), Enbrel cu metotrexat (n = 294) sau monoterapia cu metotrexat (n = 197) a fost evaluată timp de până la 3 ani într-un registru de 594 copii cu vârste între 2 și 18 ani cu artrita idiopatică juvenilă, dintre care 39 aveau vârsta de 2 până la 3 ani. În general, infecțiile au fost raportate mai frecvent la pacienții tratați cu etanercept decât la cei tratați numai cu metotrexat (3,8 față de 2%), iar infecțiile asociate cu utilizarea etanerceptului au fost mai severe .
Într-un alt studiu deschis, cu un singur braț, 60 de pacienți cu oligoartrită extinsă (15 pacienți cu vârsta cuprinsă între 2-4 ani, 23 de pacienți cu vârsta cuprinsă între 5 și 11 ani și 22 de pacienți cu vârsta cuprinsă între 12 și 17 ani), 38 de pacienți cu entezită de artrită înrudită (12 -17 ani) și 29 de pacienți cu artrită psoriazică (12-17 ani) au fost tratați cu Enbrel în doză de 0,8 mg / kg (până la maximum 50 mg per doză), administrată săptămânal timp de 12 săptămâni. fiecare dintre subtipurile JIA, majoritatea pacienților au îndeplinit criteriile ACR Pedi 30 și au demonstrat îmbunătățirea clinică a obiectivelor secundare, cum ar fi numărul articulațiilor sensibile și evaluarea generală a medicului. Profilul de siguranță a fost în concordanță cu cel observat în alte studii JIA.
Nu au fost efectuate studii la pacienți cu artrită idiopatică juvenilă pentru a evalua efectele terapiei continue cu Enbrel la pacienții care nu au răspuns în termen de trei luni de la începerea terapiei.
În mod similar, nu au fost efectuate studii pentru a evalua efectele opririi sau reducerii dozei recomandate de Enbrel după utilizarea sa pe termen lung la pacienții cu AIJ.
Pacienți copii cu psoriazis în plăci
Eficacitatea Enbrel a fost evaluată într-un studiu randomizat, dublu-orb, controlat cu placebo, efectuat pe 211 de copii și adolescenți cu vârsta cuprinsă între 4 și 17 ani cu psoriazis în plăci moderat până la sever (definit printr-un scor sPGA ≥ 3, implicând 10% sau mai mult din BSA, și PASI ≥ 12) Pacienții eligibili au avut antecedente de tratament cu fototerapie sau terapie sistemică sau au fost controlați inadecvat prin terapie topică.
Pacienții au primit Enbrel 0,8 mg / kg (până la 50 mg) sau placebo o dată pe săptămână timp de 12 săptămâni. În săptămâna 12, mai mulți pacienți au avut răspunsuri de eficacitate pozitive (adică PASI 75) în grupul randomizat cu Enbrel comparativ cu grupul randomizat cu placebo.
Abrevieri: Evaluare globală a medicului static sPGA.
pe p
După perioada de tratament dublu-orb de 12 săptămâni, toți pacienții au primit Enbrel 0,8 mg / kg (până la 50 mg) o dată pe săptămână pentru încă 24 de săptămâni. Răspunsurile observate în perioada deschisă au fost similare cu cele observate în perioada dublu-orb.
În timpul unei perioade de întrerupere randomizată, numărul pacienților care au avut recidivă a bolii (pierderea răspunsului PASI 75) a fost semnificativ mai mare în grupul de pacienți re-randomizați la placebo decât în grupul de pacienți re-randomizați la Enbrel. Cu tratamentul continuu, răspunsurile au fost menținute până la 48 de săptămâni.
Siguranța și eficacitatea pe termen lung a Enbrel 0,8 mg / kg (până la maximum 50 mg) o dată pe săptămână au fost evaluate într-un studiu de extensie deschis, care a implicat 181 de copii și adolescenți cu psoriazis în plăci, prin administrarea produsului timp de cel mult 2 ani cele 48 de săptămâni menționate mai sus. Experiența pe termen lung cu Enbrel a fost în general comparabilă cu cea observată în studiul inițial de 48 de săptămâni și nu au apărut noi probleme de siguranță.
Pacienți adulți cu poliartrită reumatoidă
Eficacitatea Enbrel a fost evaluată într-un studiu randomizat, dublu-orb, controlat cu placebo.
Studiul a evaluat 234 de pacienți adulți cu artrită reumatoidă activă care nu au reușit să răspundă la terapie cu cel puțin unul, dar nu mai mult de patru medicamente antireumatice (DMARD) care modifică boala. Doze de 10 mg sau 25 mg de Enbrel sau placebo au fost administrate subcutanat de două ori pe săptămână timp de 6 luni consecutive. Rezultatele acestui studiu clinic controlat au fost exprimate ca procent de îmbunătățire a artritei reumatoide utilizând criteriul de răspuns al Colegiului American de Reumatologie (ACR).
Răspunsurile ACR 20 și 50 au fost mai mari la pacienții tratați cu Enbrel la 3 și 6 luni decât la pacienții tratați cu placebo (ACR 20: Enbrel 62% și 59%, placebo 23% și 11% la trei și respectiv 6 luni, respectiv: ACR 50 : Enbrel 41% și 40%, placebo 8% și 5% la trei și respectiv șase luni; p
Aproximativ 15% dintre pacienții care au primit Enbrel au obținut un răspuns ACR 70 la 3 și 6 luni, comparativ cu mai puțin de 5% dintre subiecții din brațul placebo. Dintre pacienții care au primit Enbrel, răspunsurile clinice au fost observate în general între 1 și 2 săptămâni după inițierea terapiei și aproape toate au avut loc în decurs de 3 luni. A fost observat un răspuns la doză: rezultatele obținute cu 10 mg sunt stări intermediare între placebo și 25 mg. semnificativ mai bun decât placebo în toți parametrii criteriilor ACR, precum și în alte evaluări ale activității bolii artritei reumatoide care nu au fost incluse în criteriile de răspuns ACR, cum ar fi, de exemplu, rigiditatea dimineții. Un chestionar de evaluare a sănătății (HAQ) a fost administrat la fiecare 3 luni în timpul studiului, care a inclus dizabilitate, vitalitate, sănătate mintală, condiții generale de sănătate și subdomenii privind condițiile de sănătate legate de artrită Toate subdomeniile HAQ s-au îmbunătățit la pacienții tratați cu Enbrel comparativ cu controalele la 3 și 6 luni.
După oprirea Enbrel, simptomele artritei revin de obicei în decurs de o lună.
Reluarea tratamentului cu Enbrel după o întrerupere de până la 24 de luni are ca rezultat aceeași amplitudine de răspunsuri ca și pacienții care au primit Enbrel fără întreruperea terapiei pe baza rezultatelor studiilor deschise. Răspunsuri durabile susținute până la 48 de luni au fost observate în extinderea terapiei în cadrul studiilor clinice deschise când pacienții au primit Enbrel fără întrerupere; experiențele pe termen lung nu sunt disponibile.
Eficacitatea Enbrel a fost comparată cu metotrexatul într-un al treilea studiu randomizat, controlat activ, cu evaluare radiografică orbită ca obiectiv principal la 632 pacienți adulți cu poliartrită reumatoidă activă (prezentă din
În acest studiu, daunele articulare structurale au fost evaluate prin metoda radiografică și exprimate ca o modificare a scorului total ascuțit (TSS), care include rata de eroziune și rata de reducere a spațiului articular (JSN).
Radiografiile mâinilor / încheieturilor mâinilor și picioarelor au fost citite la inițierea studiului și la 6, 12 și 24 luni. Doza de 10 mg de Enbrel a avut un efect constant mai redus asupra deteriorării structurale decât doza de 25 mg. 25 mg de Enbrel au avut un efect semnificativ mai mare cu privire la rata de eroziune atât la 12, cât și la 24 de luni, comparativ cu metotrexatul. Diferențele dintre TSS și JSN nu au fost semnificative statistic între metotrexat și Enbrel 25 mg.
Într-un studiu clinic randomizat dublu-orb, controlat activ, eficacitatea clinică, siguranța și progresia radiografică la pacienții cu poliartrită reumatoidă tratați cu Enbrel singur (25 mg de două ori pe săptămână), cu metotrexat singur (de la 7, 5 la 20 mg pe săptămână , doza medie de 20 mg) și combinația de Enbrel și metotrexat, inițiată în același timp, au fost comparate la 682 de pacienți adulți cu poliartrită reumatoidă activă de la 6 luni la 20 de ani (medie 5 ani) care au prezentat un răspuns inadecvat la cel puțin un medicament antireumatic care modifică boala (DMARD), altul decât metotrexatul.
Pacienții din Enbrel în combinație cu grupul de tratament cu metotrexat au avut un răspuns semnificativ mai mare ACR 20, ACR 50, ACR 70 și ameliorarea scorurilor DAS și HAQ atât la 24, cât și la 52 săptămâni, comparativ cu pacienții din ambele grupuri tratați în monoterapie (rezultatele sunt prezentate în tabelul de mai jos). Au fost observate beneficii semnificative după 24 de luni pentru Enbrel în asociere cu metotrexat comparativ cu Enbrel singur și metotrexat singur.
Progresia radiografică la 12 luni a fost semnificativ mai mică în grupul Enbrel decât în grupul cu metotrexat, în timp ce combinația celor două a fost semnificativ mai bună decât ambele monoterapii în încetinirea progresiei radiografice.
Au fost observate beneficii semnificative după 24 de luni pentru Enbrel în asociere cu metotrexat comparativ cu Enbrel singur și metotrexat singur. În mod similar, au fost observate avantaje semnificative pentru Enbrel singur față de metotrexat singur după 24 de luni.
Într-o analiză în care toți pacienții care au renunțat la studiu din orice motiv au fost considerați că au avut o progresie radiologică, procentul pacienților fără progresie (modificarea TSS ≤ 0,5) la 24 de luni a fost mai mare în grupul tratat cu Enbrel în asociere cu metotrexat. comparativ cu grupul tratat cu Enbrel singur și cu metotrexat singur (62%, 50%, respectiv 36%; p
Siguranța și eficacitatea Enbrel 50 mg (două injecții SC de 25 mg) administrate o dată pe săptămână au fost evaluate într-un studiu dublu-orb controlat pe 420 de pacienți cu artrită reumatoidă activă. În acest studiu, 53 de pacienți au primit placebo., 214 de pacienți au primit Enbrel 50 mg o dată pe săptămână și 153 pacienți au primit Enbrel 25 mg de două ori pe săptămână. Profilul de siguranță și eficacitate al celor două scheme de tratament cu Enbrel au fost comparabile în săptămâna 8, pentru efectele lor asupra semnelor și simptomelor artritei reumatoide; datele din săptămâna 16 nu au arătat comparabilitatea (non-inferioritatea) între cele două regimuri.
Pacienți adulți cu psoriazis în plăci
Utilizarea Enbrel la pacienți este recomandată așa cum este descris în secțiunea 4.1. La populația studiată, pacienții la care „nu au răspuns” au fost definiți prin răspuns insuficient (PASIPGA mai puțin decât bun) sau agravarea bolii în timpul tratamentului și care au fost tratați în mod adecvat pentru o perioadă de timp suficient de lungă pentru a evalua răspunsul la cel puțin fiecare dintre cele trei terapii sistemice majore în funcție de disponibilitate.
Eficacitatea Enbrel împotriva altor terapii sistemice la pacienții cu psoriazis moderat până la sever (care răspund la alte terapii sistemice) nu a fost evaluată în studii de comparație directă între Enbrel și alte terapii sistemice. În schimb, siguranța și eficacitatea Enbrel au fost evaluate în patru cazuri randomizate , studii dublu-orb, controlate cu placebo.
Obiectivul principal de eficacitate în toate cele patru studii a fost proporția pacienților din fiecare grup de tratament care au atins PASI 75 în săptămâna 12 (adică o îmbunătățire de cel puțin 75% față de valoarea inițială a scorului zonei de psoriazis și a indicelui de severitate [PASI]).
Studiul 1 a fost un studiu de fază 2 la pacienți cu vârsta ≥ 18 ani cu psoriazis activ, dar clinic stabil, care afectează o „suprafață corporală ≥ 10%. O sută doisprezece pacienți au fost randomizați pentru a primi o doză de 25 mg. Enbrel (n = 57) sau placebo (n = 55) de două ori pe săptămână timp de 24 de săptămâni.
Studiul 2 a evaluat 652 de pacienți cu psoriazis cronic în plăci utilizând aceleași criterii de incluziune ca și studiul 1, cu adăugarea unui indice de zonă și severitate a psoriazisului (PASI) de cel puțin 10 la screening. Enbrel a fost administrat la o doză de 25 mg. O dată pe săptămână, 25 mg de două ori pe săptămână sau 50 mg de două ori pe săptămână timp de 6 luni consecutive. În primele 12 săptămâni ale perioadei de tratament dublu-orb, pacienții au primit placebo sau unul dintre cele trei puncte forte ale Enbrel menționate mai sus. După 12 săptămâni de tratament, pacienții din grupul placebo a început tratamentul cu Enbrel orbit (25 mg de două ori pe săptămână); pacienții din grupurile de tratament activ au continuat până în săptămâna 24 cu doza la care erau. au fost inițial randomizați.
Studiul 3 a evaluat 583 de pacienți și a avut aceleași criterii de incluziune ca și studiul 2. Pacienții din acest studiu au primit 25 mg sau 50 mg de Enbrel sau placebo de două ori pe săptămână timp de 12 săptămâni, după care toți pacienții au primit 25 mg de Enbrel deschisă de două ori pe zi săptămână pentru încă 24 de săptămâni.
Studiul 4 a evaluat 142 de pacienți și a avut criterii de incluziune similare cu studiile 2 și 3.
Pacienții din acest studiu au primit fie 50 mg Enbrel, fie placebo o dată pe săptămână timp de 12 săptămâni, după care toți pacienții au primit 50 mg Enbrel o dată pe săptămână o dată pe săptămână timp de încă 12 săptămâni.
În studiul 1, grupul Enbrel a avut o proporție semnificativ mai mare de pacienți cu răspuns PASI 75 în săptămâna 12 (30%) decât grupul placebo (2%) (p
Răspunsurile pacienților cu psoriazis în studiile 2, 3 și 4
* p ≤ 0,0001 comparativ cu placebo
la. Nu s-au făcut comparații statistice cu placebo în săptămâna 24 în studiile 2 și 4, deoarece grupul inițial cu placebo a început să primească Enbrel 25 mg o dată pe săptămână sau 50 mg o dată pe săptămână în săptămâna 13 până în săptămâna 24.
b. Dermatolog Static Global Assessment. „Clear” sau „Near clear” definit ca 0 sau 1 pe o scară de la 0 la 5.
Dintre pacienții cu psoriazis în plăci care au primit Enbrel, răspunsurile semnificative în raport cu placebo au fost evidente în momentul primei vizite (2 săptămâni) și au fost menținute pe parcursul a 24 de săptămâni de tratament.
Studiul 2 a inclus, de asemenea, o perioadă de întrerupere a tratamentului în timpul căreia pacienții care au obținut o îmbunătățire PASI de cel puțin 50% în săptămâna 24 au întrerupt tratamentul.
În timpul perioadei de întrerupere, pacienții au fost monitorizați pentru apariția evenimentelor de „revenire” (PASI ≥150% din valoarea inițială) și pentru timpul de recidivă (definit ca o pierdere de cel puțin jumătate din îmbunătățirea realizată între momentul inițial și săptămâna 24). În timpul perioadei de întrerupere, simptomele psoriazisului au recidivat treptat, cu un timp mediu până la recidiva de 3 luni. Nu au fost observate recăderi de revenire și nu au fost observate evenimente adverse grave legate de psoriazis. Au existat unele dovezi care să susțină beneficiul unui nou tratament cu Enbrel la pacienții care au fost inițial receptivi la tratament.
În studiul 3, majoritatea pacienților (77%) care au fost inițial randomizați la 50 mg de două ori pe săptămână și care au primit o doză redusă de 25 mg Enbrel de două ori pe săptămână în săptămâna 12. PASI 75 până în săptămâna 36. Pentru pacienții care au primit 25 mg de două ori pe săptămână pe tot parcursul studiului, răspunsul PASI 75 a continuat să se îmbunătățească între săptămânile 12 și 36.
În studiul 4, grupul Enbrel a avut o proporție mai mare de pacienți cu PASI 75 în săptămâna 12 (38%) decât grupul placebo (2%) (p
Într-un studiu deschis pe termen lung (până la 34 de luni) în care Enbrel a fost administrat fără întrerupere, răspunsul clinic a fost menținut, iar siguranța a fost comparabilă cu cea din studiile pe termen scurt.
O analiză a datelor studiilor clinice nu a constatat caracteristici ale bolii la momentul inițial care să poată ajuta clinicianul să aleagă cea mai adecvată opțiune de dozare (intermitentă sau continuă). În consecință, alegerea terapiei continue sau intermitente trebuie să se bazeze pe judecata medicului și pe nevoile individuale ale pacientului.
Anticorpi împotriva Enbrel
Au fost detectați anticorpi împotriva etanerceptului în serul unor subiecți tratați cu etanercept. Acești anticorpi nu au fost neutralizați și sunt în general tranzitorii. Se pare că nu există nicio corelație între dezvoltarea anticorpilor și răspunsul clinic sau evenimentele adverse.
În timpul studiilor clinice la subiecți tratați cu doze aprobate de etanercept timp de până la 12 luni, cantitățile cumulative de anticorpi anti-etanercept au fost de aproximativ 6% la subiecții cu artrită reumatoidă, 7,5% la subiecții cu artrită psoriazică, 2% la subiecții cu spondilită alchilozantă, 7% la subiecții cu psoriazis, 9,7 la subiecții cu psoriazis pediatric și 4,8% la subiecții cu artrită idiopatică juvenilă.
Proporția subiecților care au dezvoltat anticorpi împotriva etanerceptului în studii pe termen lung (până la 3,5 ani) crește cu timpul, așa cum era de așteptat.Cu toate acestea, datorită naturii lor tranzitorii, incidența anticorpilor detectați la fiecare punct de evaluare a fost în general mai mică de 7% la subiecții cu poliartrită reumatoidă și la subiecții cu psoriazis.
Într-un studiu pe termen lung asupra psoriazisului, în care pacienții au primit 50 mg de două ori pe săptămână timp de 96 de săptămâni, incidența anticorpilor observați la fiecare punct de evaluare a fost de aproximativ 9%.
05.2 Proprietăți farmacocinetice
Valorile serice ale etanerceptului au fost evaluate prin metoda Testului imunosorbent enzimatic (ELISA), care poate detecta atât produsele de degradare care reacționează cu ELISA, cât și compusul părinte.
Populații speciale
Insuficiență renală
Deși există eliminarea radioactivității în urină după administrarea etanerceptului marcat radioactiv la pacienți și voluntari, nu a fost observată nicio creștere a concentrațiilor de etanercept la pacienții cu insuficiență renală acută. Prezența insuficienței renale nu trebuie să necesite nicio modificare a dozei.
Insuficiență hepatică
Nu s-au observat concentrații crescute de etanercept la pacienții cu insuficiență hepatică acută. Prezența insuficienței hepatice nu ar trebui să necesite modificarea dozei.
Populația pediatrică
Pacienți copii cu artrită idiopatică juvenilă
Într-un studiu poliarticular cu artrită idiopatică juvenilă cu Enbrel, 69 de pacienți (cu vârste cuprinse între 4 și 17 ani) au primit 0,4 mg / kg de Enbrel, de două ori pe săptămână timp de trei luni.
Modelul concentrațiilor serice a fost similar cu cel observat la pacienții adulți cu poliartrită reumatoidă. Copiii mai mici (vârsta de 4 ani) au clearance-ul redus (clearance crescut atunci când este normalizat pentru greutate) în comparație cu copiii mai mari (vârsta de 12 ani) și adulții A simularea dozelor sugerează că, în timp ce copiii mai mari (10-17 ani) ar avea niveluri serice apropiate de cele observate la adulți, copiii mai mici ar avea niveluri semnificativ mai mici.
Pacienți copii cu psoriazis în plăci
Pacienții copii cu psoriazis în plăci (cu vârste cuprinse între 4 și 17 ani) au primit 0,8 mg pe kilogram de etanercept (până la o doză maximă de 50 mg pe săptămână) o dată pe săptămână timp de 48 de săptămâni. Concentrațiile serice medii la starea de echilibru au variat de la 1,6 la 2,1 mcg / ml la săptămânile 12, 24 și 48.
Aceste concentrații serice medii la pacienții cu psoriazis în plăci pediatrice sunt similare cu cele observate la pacienții cu artrită idiopatică juvenilă (tratați cu 0,4 mg pe kilogram de etanercept, de două ori pe săptămână, până la o doză maximă de 50 mg pe săptămână).
Aceste concentrații medii sunt similare cu cele observate la pacienții adulți cu psoriazis în plăci tratați cu etanercept 25 mg o dată pe săptămână.
Adulți
Absorbţie
Etanercept se absoarbe încet de la locul injectării subcutanate, atingând concentrația maximă la aproximativ 48 de ore după administrarea unei doze unice. după o singură doză subcutanată de 25 mg de Enbrel, concentrația plasmatică maximă medie observată la voluntarii sănătoși a fost de 1,65 ± 0,66 μg / ml, iar aria de sub curbă a fost de 235 ± 96,6 mcg • oră / ml.
La pacienții tratați cu RA, profilurile concentrației serice medii la starea de echilibru au fost Cmax 2,4 mg / l față de 2,6 mg / l, Cmin 1,2 mg / l față de 1,4 mg / l și ASC parțială 297 mgh / l față de 316 mgh / l, respectiv pentru 50 mg Enbrel o dată pe săptămână (n = 21) vs 25 mg Enbrel de două ori pe săptămână (n = 16). Într-un studiu deschis, cu doză unică, cu două tratamente, încrucișat la voluntari sănătoși, etanerceptul administrat ca injecție cu doză unică de 50 mg / ml a fost bioechivalent cu două injecții simultane de 25 mg / ml.
Într-o analiză farmacocinetică populațională la pacienții cu spondilită anchilozantă, ASC ale etanerceptului la starea de echilibru au fost de 466 mcg • oră / ml și 474 mcg • oră / ml, pentru Enbrel 50 mg o dată pe săptămână, respectiv (N = 154) și 25 mg de două ori pe săptămână (N = 148).
Distribuție
Este necesară o curbă bi-exponențială pentru a descrie curba concentrație-timp a etanerceptului. Volumul central de distribuție al etanercept este de 7,6 litri, în timp ce volumul de distribuție la starea de echilibru este de 10,4 litri.
Eliminare
Etanercept este eliminat încet din corp. Are un timp de înjumătățire lung de aproximativ 70 de ore. Clearance-ul este de aproximativ 0,066 litri / oră la pacienții cu poliartrită reumatoidă, oarecum mai mic decât valoarea de 0,11 litri / oră observată la voluntarii sănătoși.
Nu există nicio diferență aparentă în farmacocinetică între bărbați și femei.
Linearitatea
Proporționalitatea dozei nu a fost evaluată formal, dar nu există o saturație aparentă a clearance-ului în intervalul de doze.
05.3 Date preclinice de siguranță
În timpul studiilor de toxicologie cu Enbrel nu a apărut nicio toxicitate limitativă a dozei sau a organelor țintă. În mai multe studii s-a constatat că Enbrel nu este genotoxic in vitro și in vivo.
Datorită apariției anticorpilor neutralizanți la rozătoare, studiile de carcinogenitate și evaluarea standard a fertilității și toxicității postnatale nu au fost efectuate cu Enbrel. Enbrel nu a cauzat mortalitate detectabilă sau semne de toxicitate la șoareci sau șobolani după o singură doză subcutanată de 2.000 mg / kg sau o doză intravenoasă unică de 1.000 mg / kg. Enbrel nu a cauzat toxicitate limitativă a dozei sau organe țintă la maimuțele cynomolgus după administrarea subcutanată de două ori pe săptămână timp de 4 sau 26 săptămâni consecutive la o doză (15 mg / kg), rezultând concentrații serice de medicamente pe bază de ASC, care au fost de peste 27 de ori mai mari decât cele obținute la bărbați la doza recomandată de 25 mg.
06.0 INFORMAȚII FARMACEUTICE
06.1 Excipienți
Praf:
Manitol (E421)
Zaharoza
Trometamol
Solvent:
Apă pentru preparate injectabile
Alcool benzilic
06.2 Incompatibilitate
În absența studiilor de compatibilitate, medicamentul nu trebuie amestecat cu alte medicamente.
06.3 Perioada de valabilitate
3 ani
După reconstituire, stabilitatea chimică și fizică la utilizare a fost demonstrată timp de 14 zile la 2 ° C - 8 ° C.
Din punct de vedere microbiologic, medicamentul reconstituit poate fi păstrat până la 14 zile la 2 ° C - 8 ° C. Alte perioade și condiții de păstrare înainte de utilizare sunt responsabilitatea utilizatorului.
06.4 Precauții speciale pentru depozitare
A se păstra la frigider (între 2 ° C și 8 ° C). Nu înghețați.
Enbrel poate fi păstrat la o temperatură maximă de 25 ° C timp de până la 4 săptămâni, pentru o singură dată; după această perioadă nu mai poate fi pus la loc în frigider. Dacă nu este utilizat în decurs de 4 săptămâni în afara frigiderului, Enbrel trebuie aruncat.
Pentru condițiile de păstrare a medicamentului reconstituit, vezi pct. 6.3.
06.5 Natura ambalajului imediat și conținutul ambalajului
Flacoane din sticlă transparentă (4 ml, sticlă tip I) cu dopuri din cauciuc, garnituri din aluminiu și capace detașabile din plastic.
Enbrel vine cu seringi preumplute care conțin apă bacteriostatică pentru preparate injectabile. Seringile sunt compuse din sticlă tip I cu ace din oțel inoxidabil.
Pachetele conțin 4 flacoane de Enbrel cu 4 seringi preumplute cu solvent, 8 seringi goale din plastic, 20 ace din oțel inoxidabil și 24 tampoane cu alcool.
06.6 Instrucțiuni de utilizare și manipulare
Instrucțiuni de utilizare și manipulare
Enbrel se reconstituie în 1 ml de apă bacteriostatică pentru preparate injectabile înainte de utilizare și se administrează subcutanat. Soluția trebuie să fie limpede și incoloră sau galben pal, fără bulgări, floculate sau particule. Unele bule albe pot rămâne în flacon. - acest lucru este normal. Enbrel nu trebuie utilizat dacă toată pulberea din flacon nu se dizolvă în decurs de 10 minute de la reconstituire. Dacă da, repetați procesul cu un alt flacon.
Instrucțiunile detaliate pentru prepararea, administrarea și reutilizarea flaconului reconstituit cu Enbrel sunt furnizate în prospect, secțiunea 7, „Instrucțiuni pentru prepararea și administrarea unei„ injecții cu Enbrel ”.
Medicamentele neutilizate și deșeurile derivate din acest medicament trebuie eliminate în conformitate cu reglementările locale.
07.0 DEȚINĂTORUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
Pfizer Limited
Ramsgate Road
Sandwich
Kent CT13 9NJ
Regatul Unit
08.0 NUMĂRUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
EU / 1/99/126/012
034675165
09.0 DATA PRIMEI AUTORIZAȚII SAU REÎNNOIREA AUTORIZAȚIEI
Data primei autorizații: 3 februarie 2000
Data ultimei reînnoiri: 3 februarie 2010